早教吧作业答案频道 -->化学-->
某实验小组用废铁屑(含少量S等元素)为原料制备三草酸合铁(Ⅲ)酸钾晶体[K3Fe(C2O4)3•3H2O]并测定其组成.实验一制备硫酸亚铁铵[(NH4)2SO4•FeSO4•6H2O]小组同学设计如图装置(夹持
题目详情
某实验小组用废铁屑(含少量S等元素)为原料制备三草酸合铁(Ⅲ)酸钾晶体[K3Fe(C2O4)3•3H2O]并测定其组成.
实验一 制备硫酸亚铁铵[(NH4)2SO4•FeSO4•6H2O]
小组同学设计如图装置(夹持仪器略去),称取一定量废铁屑于锥形瓶中,加入适量稀硫酸,在通风橱中置于50~60℃热水浴中加热,充分反应.待锥形瓶中溶液冷却后加入氨水,搅拌使其反应完全,制得浅绿色悬浊液.
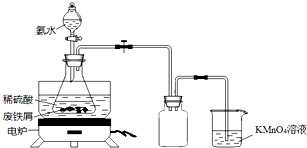
(1)实验室保存浓氨水的方法是___.
(2)烧杯中高锰酸钾溶液的作用是___.
(3)写出锥形瓶中发生中和反应的离子方程式:___.
(4)若要确保获得浅绿色悬浊液,实验过程应注意的是___(填序号).
a.保持铁屑过量 b.控制溶液呈强酸性 c.持续升高温度
实验二 制备三草酸合铁(Ⅲ)酸钾晶体
实验小组用实验一锥形瓶中的悬浊液设计以下实验流程制备三草酸合铁(Ⅲ)酸钾晶体.

已知:25℃时,[Fe(C2O4)3]3-(aq)+SCN-(aq)⇌[Fe(SCN)]2+(aq)+3C2O42-(aq) K=10-16.2
(5)写出步骤Ⅰ生成黄色沉淀(FeC2O4•2H2O)的化学方程式:___.
(6)步骤Ⅱ水浴加热需控制40℃的理由是___.
(7)小组同学欲检验晶体中含有Fe(Ⅲ),取少量晶体放入试管中,用蒸馏水充分溶解,向试管中滴入几滴0.1mol•L-1KSCN溶液.请判断上述实验方案是否可行并说明理由.___.
实验三 测定三草酸合铁(Ⅲ)酸钾晶体中C2O42-的含量
小组同学准确称取m g晶体配制成250mL溶液,取25mL该溶液于锥形瓶中,加入3mol•L-1硫酸溶液10mL,滴入二苯胺磺酸钠作指示剂,用c mol•L-1K2Cr2O7标准液滴定至紫红色,平行实验三次,平均消耗标准液V mL.已知:Cr2O72-在酸性介质中被还原为Cr3+.
(8)晶体中C2O42-质量分数的表达式为___.
实验一 制备硫酸亚铁铵[(NH4)2SO4•FeSO4•6H2O]
小组同学设计如图装置(夹持仪器略去),称取一定量废铁屑于锥形瓶中,加入适量稀硫酸,在通风橱中置于50~60℃热水浴中加热,充分反应.待锥形瓶中溶液冷却后加入氨水,搅拌使其反应完全,制得浅绿色悬浊液.

(1)实验室保存浓氨水的方法是___.
(2)烧杯中高锰酸钾溶液的作用是___.
(3)写出锥形瓶中发生中和反应的离子方程式:___.
(4)若要确保获得浅绿色悬浊液,实验过程应注意的是___(填序号).
a.保持铁屑过量 b.控制溶液呈强酸性 c.持续升高温度
实验二 制备三草酸合铁(Ⅲ)酸钾晶体
实验小组用实验一锥形瓶中的悬浊液设计以下实验流程制备三草酸合铁(Ⅲ)酸钾晶体.

已知:25℃时,[Fe(C2O4)3]3-(aq)+SCN-(aq)⇌[Fe(SCN)]2+(aq)+3C2O42-(aq) K=10-16.2
(5)写出步骤Ⅰ生成黄色沉淀(FeC2O4•2H2O)的化学方程式:___.
(6)步骤Ⅱ水浴加热需控制40℃的理由是___.
(7)小组同学欲检验晶体中含有Fe(Ⅲ),取少量晶体放入试管中,用蒸馏水充分溶解,向试管中滴入几滴0.1mol•L-1KSCN溶液.请判断上述实验方案是否可行并说明理由.___.
实验三 测定三草酸合铁(Ⅲ)酸钾晶体中C2O42-的含量
小组同学准确称取m g晶体配制成250mL溶液,取25mL该溶液于锥形瓶中,加入3mol•L-1硫酸溶液10mL,滴入二苯胺磺酸钠作指示剂,用c mol•L-1K2Cr2O7标准液滴定至紫红色,平行实验三次,平均消耗标准液V mL.已知:Cr2O72-在酸性介质中被还原为Cr3+.
(8)晶体中C2O42-质量分数的表达式为___.
▼优质解答
答案和解析
(1)由于氨水不稳定,见光受热易分解,故实验室保存氨水的方法为密封保存,置于冷暗处,故答案为:密封保存,置于冷暗处;
(2)由于废铁屑中含有含S元素的物质,加入稀硫酸,会产生硫化氢等有毒气体,不能向空气中排放,高锰酸钾溶液的作用是吸收H2S等尾气,防止污染空气,故答案为:吸收H2S等尾气,防止污染空气;
(3)锥形瓶中是冷切后的溶液中稀硫酸与氨水的反应,生成硫酸铵和水,氨水为弱碱,不能拆,离子方程式为NH3•H2O+H+=NH4++H2O,故答案为:NH3•H2O+H+=NH4++H2O;
(4)由于Fe2+有较强的还原性,实验过程中要防止二价铁被氧气氧化,保持铁屑过量就是防止亚铁离子被氧化;二价铁离子在溶液中要水解,故需抑制其水解,加入稀硫酸可以增大氢离子浓度,抑制亚铁离子的水解,因此要确保获得浅绿色悬浊液,可选择ab,故答案为:ab;
(5)步骤Ⅰ为硫酸亚铁铵晶体与饱和草酸溶液反应生成黄色沉淀(FeC2O4•2H2O),化学方程式为(NH4)2SO4•FeSO4•6H2O+H2C2O4=FeC2O4•2H2O↓+(NH4)2SO4+H2SO4+4H2O,故答案为:(NH4)2SO4•FeSO4•6H2O+H2C2O4=FeC2O4•2H2O↓+(NH4)2SO4+H2SO4+4H2O;
(6)温度太高,H2O2分解;温度太低,Fe2+氧化速度太慢,故水浴加热控制在40℃是防止过氧化氢分解和确保二价铁被氧化为三价铁的反应速率,故答案为:温度太高,H2O2分解;温度太低,Fe2+氧化速度太慢;
(7)因为25℃时,[Fe(C2O4)3]3-(aq)+SCN-(aq)⇌[Fe(SCN)]2+(aq)+3C2O42-(aq) K=10-16.2,平衡常数小于10-5,离子浓度太小,观察不到明显现象,所以无法检验,故答案为:否,因为[Fe(C2O4)3]3-转化为[Fe(SCN)]2+反应的平衡常数小于10-5,观察不到明显现象,所以无法检验;
(8)根据反应,25mL标准液消耗c mol•L-1K2Cr2O7V mL,物质的量为cV×10-3mol,设有C2O42-的质量为x,根据方程式
3C2O42-+14H++Cr2O72-=2Cr3++6CO2↑+7H2O
3×88g 1mol
x cV×10-3mol
x=264cV×10-3g,故250mL中含有的质量为264cV×10-2g,晶体中C2O42-质量分数的表达式为=
%,故答案为:
%.
(2)由于废铁屑中含有含S元素的物质,加入稀硫酸,会产生硫化氢等有毒气体,不能向空气中排放,高锰酸钾溶液的作用是吸收H2S等尾气,防止污染空气,故答案为:吸收H2S等尾气,防止污染空气;
(3)锥形瓶中是冷切后的溶液中稀硫酸与氨水的反应,生成硫酸铵和水,氨水为弱碱,不能拆,离子方程式为NH3•H2O+H+=NH4++H2O,故答案为:NH3•H2O+H+=NH4++H2O;
(4)由于Fe2+有较强的还原性,实验过程中要防止二价铁被氧气氧化,保持铁屑过量就是防止亚铁离子被氧化;二价铁离子在溶液中要水解,故需抑制其水解,加入稀硫酸可以增大氢离子浓度,抑制亚铁离子的水解,因此要确保获得浅绿色悬浊液,可选择ab,故答案为:ab;
(5)步骤Ⅰ为硫酸亚铁铵晶体与饱和草酸溶液反应生成黄色沉淀(FeC2O4•2H2O),化学方程式为(NH4)2SO4•FeSO4•6H2O+H2C2O4=FeC2O4•2H2O↓+(NH4)2SO4+H2SO4+4H2O,故答案为:(NH4)2SO4•FeSO4•6H2O+H2C2O4=FeC2O4•2H2O↓+(NH4)2SO4+H2SO4+4H2O;
(6)温度太高,H2O2分解;温度太低,Fe2+氧化速度太慢,故水浴加热控制在40℃是防止过氧化氢分解和确保二价铁被氧化为三价铁的反应速率,故答案为:温度太高,H2O2分解;温度太低,Fe2+氧化速度太慢;
(7)因为25℃时,[Fe(C2O4)3]3-(aq)+SCN-(aq)⇌[Fe(SCN)]2+(aq)+3C2O42-(aq) K=10-16.2,平衡常数小于10-5,离子浓度太小,观察不到明显现象,所以无法检验,故答案为:否,因为[Fe(C2O4)3]3-转化为[Fe(SCN)]2+反应的平衡常数小于10-5,观察不到明显现象,所以无法检验;
(8)根据反应,25mL标准液消耗c mol•L-1K2Cr2O7V mL,物质的量为cV×10-3mol,设有C2O42-的质量为x,根据方程式
3C2O42-+14H++Cr2O72-=2Cr3++6CO2↑+7H2O
3×88g 1mol
x cV×10-3mol
x=264cV×10-3g,故250mL中含有的质量为264cV×10-2g,晶体中C2O42-质量分数的表达式为=
| 264cV |
| m |
| 264cV |
| m |
看了 某实验小组用废铁屑(含少量S...的网友还看了以下:
紫草素是紫草细胞的代谢产物,可作为生产治疗烫伤药物的原料.研究人员欲用植物组织培养技术通过培养紫草 2020-05-14 …
在农业生产中,常用一定浓度的生长素类似物除去单子叶农作物中的双子叶杂草。如图所示是单子叶农作物、双 2020-06-11 …
乙酰紫草素具有抗菌、抗炎、抗病毒、抗肿瘤等作用,它的结构简式如图所示,下列有关乙酰紫草素的说法正确 2020-06-23 …
研究发现紫草素和乳酸菌素(小分子蛋白质)均有抑菌作用,两者的提取及应用如图所示.请回答:(1)配制 2020-06-25 …
(2013•洛阳二模)紫草药膏是一种治疗烧伤的特效药,其有效成分主要是紫草素.研究发现紫草素和乳酸 2020-07-06 …
紫草素食制造治疗烫伤和割伤的药物以及燃料和化妆品的原料,广泛用于制药业、化妆品业等领域.紫草素的获得 2020-11-04 …
实际生产中,农户常用一定浓度的生长素类似物除去与单子叶农作物混生的双子叶杂草.如图表示不同浓度的生长 2020-11-05 …
紫草素是一种重要的工业原料,广泛运用于染料、高档化妆品、医药等领域.紫草素通常存在于紫草植株的花中. 2020-11-20 …
紫草具有抗癌、抗炎、抗菌等作用,其主要的抗癌有效成分是紫草素.下面是工厂化生产紫草素的流程图.请回答 2020-12-07 …
紫草素具有抗菌、消炎效果.在工业化生产中,取紫草植株部分组织诱导形成紫草愈伤组织,再转入紫草素形成培 2021-01-08 …