早教吧作业答案频道 -->化学-->
理论上任何一个自发的氧化还原反应均可以设计成原电池,根据氧化还原反应:Fe+2Fe3+=2Fe2+设计的原电池如图所示,其中盐桥内盛装有含KNO3饱和溶液的琼脂.请回答下列问题:(1)电解质
题目详情
理论上任何一个自发的氧化还原反应均可以设计成原电池,根据氧化还原反应:Fe+2Fe3+=2Fe2+设计的原电池如图所示,其中盐桥内盛装有含KNO3饱和溶液的琼脂.
请回答下列问题:
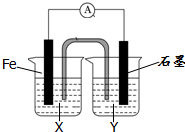
(1)电解质溶液X是___;电解质溶液Y是___.
(2)写出两电极反应式:铁电极___;石墨电极___.
(3)外电路中的电子书是从___(填名称,下同)电极流向___电极.
(4)盐桥中向X溶液中迁移的离子是___(填编号).
A.K+ B.NO
C.Ag+ D.SO
.
请回答下列问题:

(1)电解质溶液X是___;电解质溶液Y是___.
(2)写出两电极反应式:铁电极___;石墨电极___.
(3)外电路中的电子书是从___(填名称,下同)电极流向___电极.
(4)盐桥中向X溶液中迁移的离子是___(填编号).
A.K+ B.NO
| - 3 |
| 2- 4 |
▼优质解答
答案和解析
Fe+2Fe3+=2Fe2+设计的原电池中,负极上失电子发生氧化反应,正极上得电子发生还原反应,该反应中Fe元素化合价由0价、+3价变为+2价,则Fe是负极,正极材料为石墨,
(1)电解质溶液X是含有亚铁离子的盐溶液,如氯化亚铁溶液,和金属铁之间不会发生反应,电解质溶液Y是含有铁离子的盐溶液,可以是氯化铁溶液,故答案为:FeCl2;FeCl3;
(2)该反应中Fe元素化合价由0价、+3价变为+2价,则Fe是负极,极上失电子发生氧化反应,Fe-2e═Fe2+,正极材料为石墨,正极反应式为2Fe3++2e═2Fe2+,
故答案为:Fe-2e═Fe2+;2Fe3++2e═2Fe2+.
(3)原电池中电子负极流向正极,即从铁电极流向石墨电极,故答案为:铁;石墨;
(4)原电池中阳离子移向正极,阴离子移向负极,铁是负极,溶液中的阴离子会移向负极,故选BD.
(1)电解质溶液X是含有亚铁离子的盐溶液,如氯化亚铁溶液,和金属铁之间不会发生反应,电解质溶液Y是含有铁离子的盐溶液,可以是氯化铁溶液,故答案为:FeCl2;FeCl3;
(2)该反应中Fe元素化合价由0价、+3价变为+2价,则Fe是负极,极上失电子发生氧化反应,Fe-2e═Fe2+,正极材料为石墨,正极反应式为2Fe3++2e═2Fe2+,
故答案为:Fe-2e═Fe2+;2Fe3++2e═2Fe2+.
(3)原电池中电子负极流向正极,即从铁电极流向石墨电极,故答案为:铁;石墨;
(4)原电池中阳离子移向正极,阴离子移向负极,铁是负极,溶液中的阴离子会移向负极,故选BD.
看了 理论上任何一个自发的氧化还原...的网友还看了以下:
弱碱和电解质难溶的一些氢氧化物,比如氢氧化亚铁,氢氧化铁等不都不溶吗,不溶的不是强电解质吗问题是强 2020-04-10 …
下列说法正确的是()A.物质不是电解质就是非电解质B.酸性氧化物不一定都是非金属氧化物,而非金属氧 2020-05-02 …
根据要求回答下列各题(1)下列说法正确的是①纯碱,烧碱,碱式碳酸铜都是碱类物质②电解质都能导电③碱 2020-05-02 …
使用氧化性酸进行溶解沉淀时,通常需要加热,其原因是A增加难溶电解质的溶度积B增加氧化性酸的电离度C 2020-05-16 …
设计出燃料电池使汽油(设其成分为C5H12)氧化直接产生电流是21世纪最富有挑战性的课题之一.最近 2020-07-09 …
氢氧燃料电池(电解质为Na2SO4)电极方程式写电极方程式和总方程式1、氢氧燃料电池(电解质为Na 2020-07-16 …
强极性键为何熔融状态下是分子状态,不导电,但是却是强电解质如题,电解质是指在水溶液里或熔融状态下能 2020-07-29 …
铜锌原电池的问题,电解质为稀硫酸.那么解释一下为什么电解一段时间后,阴阳两极的SO42-浓度基本保持 2020-12-07 …
一个关于水解的题电解质溶液:(1)Na2CO3(2)NaHCO3(3)Na[Al(OH)4](4)C 2020-12-13 …
关于电解质溶于水的问题电解质溶于水,电解质中的离子键或共价键在水分子的作用下断裂,是化学变化,而这个 2020-12-31 …