早教吧作业答案频道 -->化学-->
已知氢氧化钙和钨酸钙(CaWO4)都是微溶电解质,两者的溶解度均随温度升高而减小.在钨冶炼工艺中,将氢氧化钙加入钨酸钠碱性溶液中得到钨酸钙,发生反应Ⅰ:WO42-(aq)+Ca(OH)2(s)
题目详情
已知氢氧化钙和钨酸钙(CaWO4)都是微溶电解质,两者的溶解度均随温度升高而减小.在钨冶炼工艺中,将氢氧化钙加入钨酸钠碱性溶液中得到钨酸钙,发生反应
Ⅰ:WO42-(aq)+Ca(OH)2(s)⇌CaWO4(s)+2OH-(aq).
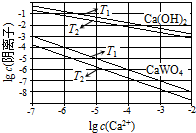
(1)如图为不同温度下Ca(OH)2、CaWO4的沉淀溶解平衡曲线.
①计算T1时KSP(CaWO4)=___.
②T1___ T2(填“>”“=”或“<”).
(2)反应Ⅰ的平衡常数K理论值如表:
①该反应平衡常数K的表达式为___.
②该反应的△H___0(填“>”“=”或“<”).
(3)常温下向较浓AlCl3的溶液中不断通入HCl气体,可析出大量AlCl3•6H2O晶体,结合化学平衡移动原理解释析出晶体的原因:___.
Ⅰ:WO42-(aq)+Ca(OH)2(s)⇌CaWO4(s)+2OH-(aq).

(1)如图为不同温度下Ca(OH)2、CaWO4的沉淀溶解平衡曲线.
①计算T1时KSP(CaWO4)=___.
②T1___ T2(填“>”“=”或“<”).
(2)反应Ⅰ的平衡常数K理论值如表:
| 温度/℃ | 25 | 50 | 90 | 100 |
| K | 79.96 | 208.06 | 222.88 | 258.05 |
②该反应的△H___0(填“>”“=”或“<”).
(3)常温下向较浓AlCl3的溶液中不断通入HCl气体,可析出大量AlCl3•6H2O晶体,结合化学平衡移动原理解释析出晶体的原因:___.
▼优质解答
答案和解析
(1)①T1时KSP(CaWO4)=c(Ca2+)•c(WO42-)=1×10-5×1×10-5=1×10-10,故答案为:1×10-10;
②沉淀的溶解平衡是吸热的过程,温度高,溶度积常数大,根据表中数据,可以看出下的Ksp较大,所以T12,故答案为:<;
(2)①反应平衡常数K等于生成物平衡浓度系数次方之积和反应物平衡浓度系数次方之积,即K=
,故答案为:
;
②根据表中温度和K之间的关系,可以看出温度高,K越大,所以反应是吸热的,故答案为:>;
(3)常温下向较浓AlCl3的溶液中不断通入HCl气体,可析出大量AlCl3•6H2O晶体,原因是AlCl3饱和溶液中存在溶解平衡:AlCl3•6H2O(s)═Al3+(aq)+3Cl-(aq)+6H2O(l),通入HCl气体,溶液中c(Cl-)增大,平衡向析出氯化铝固体的方向移动,则可析出晶体,
故答案为:AlCl3饱和溶液中存在溶解平衡:AlCl3•6H2O(s)═Al3+(aq)+3Cl-(aq)+6H2O(l),通入HCl气体使溶液中c(Cl-)增大,平衡向析出固体的方向移动从而析出AlCl3•6H2O晶体.
②沉淀的溶解平衡是吸热的过程,温度高,溶度积常数大,根据表中数据,可以看出下的Ksp较大,所以T1
(2)①反应平衡常数K等于生成物平衡浓度系数次方之积和反应物平衡浓度系数次方之积,即K=
| c2(OH-) |
| c(WO42-) |
| c2(OH-) |
| c(WO42-) |
②根据表中温度和K之间的关系,可以看出温度高,K越大,所以反应是吸热的,故答案为:>;
(3)常温下向较浓AlCl3的溶液中不断通入HCl气体,可析出大量AlCl3•6H2O晶体,原因是AlCl3饱和溶液中存在溶解平衡:AlCl3•6H2O(s)═Al3+(aq)+3Cl-(aq)+6H2O(l),通入HCl气体,溶液中c(Cl-)增大,平衡向析出氯化铝固体的方向移动,则可析出晶体,
故答案为:AlCl3饱和溶液中存在溶解平衡:AlCl3•6H2O(s)═Al3+(aq)+3Cl-(aq)+6H2O(l),通入HCl气体使溶液中c(Cl-)增大,平衡向析出固体的方向移动从而析出AlCl3•6H2O晶体.
看了 已知氢氧化钙和钨酸钙(CaW...的网友还看了以下:
含有弱酸HA和其钠盐NaA的混合溶液,在化学上用作缓冲溶液.向其中加入少量酸或碱时,溶液的酸碱性变 2020-05-13 …
含有弱酸HA和其钠盐NaA的混合溶液,在化学上用作缓冲溶液.向其中加入少量酸或碱时,溶液的酸碱性变 2020-05-13 …
钨氧化物中钨常显+5,+6价,问WO2.9中,+5价钨氧化物,+6价钨氧化物的原子个数比 2020-06-23 …
钨是我国丰产元素,也是熔点最高的金属,被誉为“光明使者”.用黑钨矿[FeWO4、MnWO4(W为+ 2020-07-08 …
用黑钨矿[FeWO4、MnWO4(W为+6价)]结合其它化工生产高纯钨的化工流程如图1.已知H2W 2020-07-16 …
钨酸钠(Na2WO4,W的最高价为+6价)常用于制造防火,防水材料等,现称取2.94g钨酸钠加水溶 2020-07-17 …
金属钨是熔点最高的金属,钨元素在自然界以钨酸盐的形式存在.白钨矿的主要成分是CaWO4,黑钨矿的主 2020-07-28 …
黑钨矿的主要成分是铁和锰的钨酸盐,化学式常写成FeWO4、MnWO4.黑钨矿传统冶炼工艺的第一阶段 2020-07-28 …
我国学者成功发现了新的一类水分解产氢催化剂:通过调控三氧化钨(WO3)局部原子结构,制备出的深蓝色 2020-07-28 …
我国钨矿储存十分丰富,在自然界中主要以钨酸盐的形式存在.其中有开采价值的黑钨矿(主要成分是铁和锰的 2020-07-28 …