早教吧作业答案频道 -->化学-->
3-丁酮酸乙酯在有机合成中用途很广,广泛用于药物合成,还用作食品的着香剂.其相对分子质量为130,常温下为无色液体,沸点181℃,受热温度超过95℃摄氏度时就会分解;易溶于水,与乙
题目详情
3-丁酮酸乙酯在有机合成中用途很广,广泛用于药物合成,还用作食品的着香剂.其相对分子质量为130,常温下为无色液体,沸点181℃,受热温度超过95℃摄氏度时就会分解;易溶于水,与乙醇、乙酸乙酯等有机试剂以任意比混溶;实验室可用以乙酸乙酯和金属钠为原料制备.乙酸乙酯相对分子质量为88,常温下为无色易挥发液体,微溶于水,沸点77℃.
【反应原理】
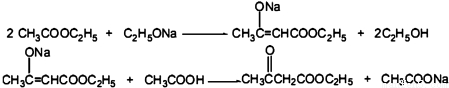
【实验装置】
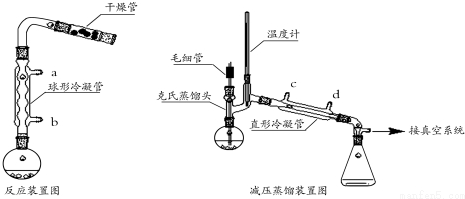
1、加热反应:向反应装置中加入32mL(28.5g,0.32mol)乙酸乙酯、少量无水乙醇、1.6g(0.07mol)切细的金属钠,微热回流1.5~3小时,直至金属钠消失.
2、产物后处理:冷却至室温,卸下冷凝管,将烧瓶浸在冷水浴中,在摇动下缓慢的加入32mL30%醋酸水溶液,使反应液分层.用分液漏斗分离出酯层.酯层用5%碳酸钠溶液洗涤,有机层放入干燥的锥形瓶中,加入无水碳酸钾至液体澄清.
3、蒸出未反应的乙酸乙酯:将反应液在常压下蒸馏至100℃.然后改用减压蒸馏,得到产品2.0g.
回答下列问题:
(1)写出实验室制备乙酸乙酯的化学方程式___.
(2)反应装置中加干燥管是为了___.两个装置中冷凝管的作用___(填“相同”或“不相同”),冷却水进水口分别为___和___(填图中的字母).
(3)产物后处理中,滴加稀醋酸的目的是___.用分液漏斗分离出酯层测操作叫___.碳酸钠溶液洗涤的目的是___.加碳酸钾的目的是___.
(4)采用减压蒸馏的原因是___.
(5)本实验所得到的3-丁酮酸乙酯产率是___(填正确答案标号).
A.10% B.22% C.19% D.40%
【反应原理】

【实验装置】

1、加热反应:向反应装置中加入32mL(28.5g,0.32mol)乙酸乙酯、少量无水乙醇、1.6g(0.07mol)切细的金属钠,微热回流1.5~3小时,直至金属钠消失.
2、产物后处理:冷却至室温,卸下冷凝管,将烧瓶浸在冷水浴中,在摇动下缓慢的加入32mL30%醋酸水溶液,使反应液分层.用分液漏斗分离出酯层.酯层用5%碳酸钠溶液洗涤,有机层放入干燥的锥形瓶中,加入无水碳酸钾至液体澄清.
3、蒸出未反应的乙酸乙酯:将反应液在常压下蒸馏至100℃.然后改用减压蒸馏,得到产品2.0g.
回答下列问题:
(1)写出实验室制备乙酸乙酯的化学方程式___.
(2)反应装置中加干燥管是为了___.两个装置中冷凝管的作用___(填“相同”或“不相同”),冷却水进水口分别为___和___(填图中的字母).
(3)产物后处理中,滴加稀醋酸的目的是___.用分液漏斗分离出酯层测操作叫___.碳酸钠溶液洗涤的目的是___.加碳酸钾的目的是___.
(4)采用减压蒸馏的原因是___.
(5)本实验所得到的3-丁酮酸乙酯产率是___(填正确答案标号).
A.10% B.22% C.19% D.40%
▼优质解答
答案和解析
(1)实验室制取乙酸乙酯的化学方程式为:CH3COOH+CH3CH2OH CH3COOCH2CH3+H2O,
CH3COOCH2CH3+H2O,
故答案为:CH3COOH+CH3CH2OH CH3COOCH2CH3+H2O;
CH3COOCH2CH3+H2O;
(2)空气中含有水蒸气,因此装置中加干燥管是为了防止空气中的水蒸汽进入反应体系中以保证反应体系干燥;
反应装置中冷凝管的作用是冷凝回流,挺高原料的利用率,减压装置中冷凝管的作用是冷却蒸发出的蒸汽便于得到产品,为充分冷凝,使冷水充满冷凝器,冷却水进水口分别为b和d,
故答案为:防止空气中的水蒸汽进入反应体系中以保证反应体系干燥;不相同;b、d;
(3)由于产物中含有钠盐,因此产物处理后,滴加稀醋酸的目的是中和生成的钠盐,使之变成产物,由于酸多了会增加产物在水中的溶解度,醋酸不能滴加的过多;
用分液漏斗分离出酯层的操作叫分液;
酯类在碳酸钠溶液中的溶解度小,除去酯中的醋酸,需要滴加碳酸钠溶液;
碳酸钾吸水,因此加碳酸钾的目的是干燥产品,
故答案为:中和生成的钠盐,使之变成产物;分液;除去酯中的醋酸;干燥产品;
(4)3-丁酮酸乙酯沸点高,而受热温度超过95℃摄氏度时就会分解,所以需要减压蒸馏,
故答案为:3-丁酮酸乙酯沸点高,而受热温度超过95℃摄氏度时就会分解,所以需要减压蒸馏;
(5)根据反应物的用量可知钠不足,因此理论上生成产品的物质的量是0.07mol,其质量是0.07mol×130g/mol=9.1g,所以产率是
×100%=22%,故选:B.
 CH3COOCH2CH3+H2O,
CH3COOCH2CH3+H2O,故答案为:CH3COOH+CH3CH2OH
 CH3COOCH2CH3+H2O;
CH3COOCH2CH3+H2O;(2)空气中含有水蒸气,因此装置中加干燥管是为了防止空气中的水蒸汽进入反应体系中以保证反应体系干燥;
反应装置中冷凝管的作用是冷凝回流,挺高原料的利用率,减压装置中冷凝管的作用是冷却蒸发出的蒸汽便于得到产品,为充分冷凝,使冷水充满冷凝器,冷却水进水口分别为b和d,
故答案为:防止空气中的水蒸汽进入反应体系中以保证反应体系干燥;不相同;b、d;
(3)由于产物中含有钠盐,因此产物处理后,滴加稀醋酸的目的是中和生成的钠盐,使之变成产物,由于酸多了会增加产物在水中的溶解度,醋酸不能滴加的过多;
用分液漏斗分离出酯层的操作叫分液;
酯类在碳酸钠溶液中的溶解度小,除去酯中的醋酸,需要滴加碳酸钠溶液;
碳酸钾吸水,因此加碳酸钾的目的是干燥产品,
故答案为:中和生成的钠盐,使之变成产物;分液;除去酯中的醋酸;干燥产品;
(4)3-丁酮酸乙酯沸点高,而受热温度超过95℃摄氏度时就会分解,所以需要减压蒸馏,
故答案为:3-丁酮酸乙酯沸点高,而受热温度超过95℃摄氏度时就会分解,所以需要减压蒸馏;
(5)根据反应物的用量可知钠不足,因此理论上生成产品的物质的量是0.07mol,其质量是0.07mol×130g/mol=9.1g,所以产率是
| 2.0g |
| 9.1g |
看了 3-丁酮酸乙酯在有机合成中用...的网友还看了以下:
用12moL·L-1浓盐酸配制250mi-0.1mol.L-1的盐酸溶液时,下列实验操作会使配得的 2020-04-12 …
配制250毫升0.1摩尔/升的盐酸溶液时,下列实验操作会使配制溶液浓度偏大的是A.用量筒制取所需的 2020-04-12 …
(2013•新余二模)(1)含有弱酸HA和其钠盐NaA的混合溶液,在化学上用作缓冲溶液.向其中加入 2020-05-13 …
(1)含有弱酸HA和其钠盐NaA的混合溶液,在化学上用作缓冲溶液.向其中加入少量酸或碱时,溶液的酸 2020-05-14 …
哪些蛋白质和浓硝酸作用时呈黄色 2020-05-16 …
在做碱式碳酸铜和盐酸作用时,是用倾倒的方法向试管中加入盐酸的.请你说明此操作的注意点及原理.瓶塞应 2020-06-02 …
有关Na2CO3和NaHCO3的叙述中正确的是()A.相同质量的Na2CO3和NaHCO3与足量盐 2020-06-24 …
将1.92g铜粉与一定量浓硝酸反应,当铜粉完全作用时收集到气体1.12L(标准状况),则所消耗硝酸物 2021-02-17 …
将1.92g铜粉与一定量浓硝酸反应,当铜粉完全作用时收集到气体1.12L(标准状况),则所消耗硝酸物 2021-02-17 …
将1.92g铜粉与一定量浓硝酸反应,当铜粉完全作用时收集到气体1.12L(标准状况).则所消耗硝酸的 2021-02-18 …