25℃时,二元弱酸H2R的pKa1=1.85,pKa2=7.45(已知pKa=-lgKa).在此温度下向20mL0.1mol•L-1H2R溶液中滴加0.1mol•L-1的NaOH溶液,溶液的pH随NaOH溶液体积的变化如图所示.下列有关说法正确的是()
25℃时,二元弱酸H2R的pKa1=1.85,pKa2=7.45(已知pKa=-lgKa).在此温度下向20mL0.1mol•L-1H2R溶液中滴加0.1mol•L-1的NaOH溶液,溶液的pH随NaOH溶液体积的变化如图所示.
下列有关说法正确的是( )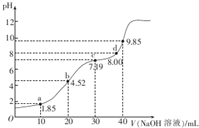
A. a点所示溶液中:c(H2R)+c(HR-)+c(R2-)=0.1mol•L-1
B. b点所示溶液中:c(Na+)>c(HR-)>c(H2R)>c(R2-)
C. c点所示溶液中:c(Na+)<3c(R2-)
D. d点所示溶液中:c(Na+)>c(R2-)>c(HR-)
| 2 |
| 3 |
| 1 |
| 15 |
B.b点二者恰好完全反应生成NaHR,溶液呈酸性,说明HR-的电离程度大于水解程度,但其水解和电离程度都较小,钠离子不水解,所以离子微粒浓度大小顺序是c(Na+)>c(HR-)>c(R2-)>c(H2R),故B错误;
C.c点溶液溶质为等物质的量的Na2R、NaHR,如果Na2R、NaHR不水解且NaHR也不电离,则存在c(Na+)=3c(R2-),实际上R2-水解且HR-的电离程度大于水解程度,钠离子不水解,所以存在c(Na+)>3c(R2-),故C错误;
D.d点溶液中溶质为Na2R,R2-水解但程度较小,所以存在c(Na+)>c(R2-)>c(HR-),故D正确;
故选D.
现有100ml溶质质量分数20%的稀硫酸,密度为1.14g/cm3,下列说法正确的是A.该溶液含溶 2020-04-09 …
常温下,0.1mol·L-1的HA溶液中c(OH-)/c(H+)=1×10-8,下列叙述中正确的是 2020-05-14 …
1、(1)少量NaHSO4与足量Ba(OH)2反应:(2)足量NaHSO4与少量Ba(OH)2反应 2020-06-21 …
对1mol•L-1的Na2SO4溶液的叙述中正确的是()A.溶液中含有1molNa2SO4B.1L 2020-07-18 …
将190gMgCl2溶于水配制成1L溶液.(1)该溶液中MgCl2的物质的量浓度为,溶液中Cl-的 2020-07-29 …
选字填空。1.熔溶融容()炼()炉()纳()合()剂()量()洽()液2.印应映()变()照()证( 2020-11-10 …
下列关于胶体的叙述中正确的是()A.液溶胶是一种液态混合物属于分散系的一种B.直径介于1nm~10n 2020-11-28 …
液压电梯(如图)是一项新枝术,它可以为十层以下的旧楼加设电梯而无需在楼顶增建悬挂轿箱用的机房。1.液 2020-12-13 …
目前我国液晶电视价格大幅度下跌,业内人士认为,液晶电视价格大幅度下跌是市场发展的必然。而到了2010 2020-12-28 …
(2014•东海县模拟)下列对20%的氯化钠溶液的理解无错误的是()A.该溶液中溶质与溶剂质量比为1 2021-01-22 …