早教吧作业答案频道 -->化学-->
氨气及其相关产品是基本化工原料,在化工领域中具有重要的作用.(1)以铁为催化剂,0.6mol氮气和1.8mol氢气在恒温、容积恒定为1L的密闭容器中反应生成氨气,20min后达到平衡,氮气的物
题目详情
氨气及其相关产品是基本化工原料,在化工领域中具有重要的作用.
(1)以铁为催化剂,0.6mol氮气和1.8mol氢气在恒温、容积恒定为1L的密闭容器中反应生成氨气,20min后达到平衡,氮气的物质的量为0.3mol.
该反应体系未达到平衡时,增大压强对逆反应速率的影响是___(填增大、减少或不变).
(2)①N2H4是一种高能燃料,有强还原性,可通过NH3和NaClO反应制得,写出该制备反应的化学方程式___
②N2H4的水溶液呈弱碱性,室温下其电离常数K1=1.0×10-6,则0.01mol•L-1 N2H4水溶液的pH等于___
(忽略N2H4的二级电离和H2O的电离).
③已知298K和101KPa条件下,32.0gN2H4在氧气中完全燃烧生成氮气和水,放出热量624kJ,则N2H4(l)的标准燃烧热的热化学方程式___
(3)科学家改进了NO2转化为HNO3的工艺(如虚框所示),在较高的操作压力下,提高N2O4/H2O的质量比和O2的用量,能制备出高浓度的硝酸.
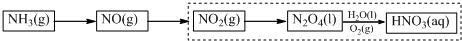
实际操作中,增大N2O4,对此请给出合理解释___.
(1)以铁为催化剂,0.6mol氮气和1.8mol氢气在恒温、容积恒定为1L的密闭容器中反应生成氨气,20min后达到平衡,氮气的物质的量为0.3mol.
该反应体系未达到平衡时,增大压强对逆反应速率的影响是___(填增大、减少或不变).
(2)①N2H4是一种高能燃料,有强还原性,可通过NH3和NaClO反应制得,写出该制备反应的化学方程式___
②N2H4的水溶液呈弱碱性,室温下其电离常数K1=1.0×10-6,则0.01mol•L-1 N2H4水溶液的pH等于___
(忽略N2H4的二级电离和H2O的电离).
③已知298K和101KPa条件下,32.0gN2H4在氧气中完全燃烧生成氮气和水,放出热量624kJ,则N2H4(l)的标准燃烧热的热化学方程式___
(3)科学家改进了NO2转化为HNO3的工艺(如虚框所示),在较高的操作压力下,提高N2O4/H2O的质量比和O2的用量,能制备出高浓度的硝酸.
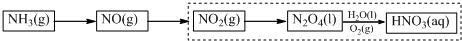
实际操作中,增大N2O4,对此请给出合理解释___.
▼优质解答
答案和解析
(1)对于有气体参加的反应,增大压强正逆反应速率都加快,所以增大压强逆反应速率加快,故答案为:增大;
(2)①该反应中,次氯酸钠被氨气含有生成氯化钠,氨气被氧化生成肼,同时还有水生成,所以该反应方程式为:NaClO+2NH3=N2H4+NaCl+H2O;
故答案为:NaClO+2NH3=N2H4+NaCl+H2O;
②电离方程式为N2H4+H2O⇌N2H5++OH-,室温下其电离常数K1≈1.0×10-6,则0.01mol•L-1N2H4水溶液中c(N2H5+)≈c(OH-),
K=
=
=1.0×10-6,所以c(OH-)=10-4mol/L,则c(H+)=10-10mol/L,则溶液的pH=10;
故答案为:10;
③32.0g肼的物质的量为1mol,1molN2H4在氧气中完全燃烧生成氮气放出热量624kJ,所以其热化学反应方程式为:N2H4(l)+O2(g)=N2(g)+2H2O(l)△H=-624KJ/mol,
故答案为:N2H4(l)+O2(g)=N2(g)+2H2O(l)△H=-624KJ/mol;
(3)2N2O4+2H2O+O2=4HNO3,则提高了N2O4的浓度,有利于平衡向正方向移动,得到高浓度的硝酸;
故答案为:提高了N2O4的浓度,有利于平衡向正方向移动,得到高浓度的硝酸.
(2)①该反应中,次氯酸钠被氨气含有生成氯化钠,氨气被氧化生成肼,同时还有水生成,所以该反应方程式为:NaClO+2NH3=N2H4+NaCl+H2O;
故答案为:NaClO+2NH3=N2H4+NaCl+H2O;
②电离方程式为N2H4+H2O⇌N2H5++OH-,室温下其电离常数K1≈1.0×10-6,则0.01mol•L-1N2H4水溶液中c(N2H5+)≈c(OH-),
K=
| c(N2H5+)×c(OH-) |
| c(N2H4) |
| c2(OH-) |
| 0.01 |
故答案为:10;
③32.0g肼的物质的量为1mol,1molN2H4在氧气中完全燃烧生成氮气放出热量624kJ,所以其热化学反应方程式为:N2H4(l)+O2(g)=N2(g)+2H2O(l)△H=-624KJ/mol,
故答案为:N2H4(l)+O2(g)=N2(g)+2H2O(l)△H=-624KJ/mol;
(3)2N2O4+2H2O+O2=4HNO3,则提高了N2O4的浓度,有利于平衡向正方向移动,得到高浓度的硝酸;
故答案为:提高了N2O4的浓度,有利于平衡向正方向移动,得到高浓度的硝酸.
看了 氨气及其相关产品是基本化工原...的网友还看了以下:
蛋白质是一类复杂的含氮化合物,每种蛋白质都有其恒定的含氮量,食品中蛋白质的含量测定常用凯氏定氮法. 2020-04-06 …
英语单词填空(组成单词)1)d.l.e.d.m.i2)l.e.p.o.i.ee3)u.y.g.o. 2020-04-25 …
凯氏定氮时暴沸的原因有哪些用凯氏定氮法测土壤中氮含量是蒸馏时突然暴沸是为什么啊?蒸馏瓶中的水没有暴 2020-06-19 …
I.氮是动植物生长不可缺少的元素,含氮化合物是重要的化工原料,研究CO、NOX等大气污染气体的处理 2020-07-08 …
推断题:现有如下反应(反应条件均不给),推断物质⑴A→B+C+D⑵C+E→C+F+D⑶D+G→H⑷ 2020-07-30 …
以O为外心,I为内心的三角形的三角形有几个?O,I为定点.以O为外心,I为内心的三角形有几个? 2020-07-30 …
O,I分别是锐角三角形ABC的外心,内心.O',I'分别是O,I关于BC的对称点.已知A、B、O' 2020-07-30 …
单词拼写。①brcc1A.o;o;iB.o;i;oC.o;o;y②cartA.roB.orC.re③ 2020-10-31 …
9个字母,已知有:c,o,t,l,n,u,o无顺序.是什么单词啊.急还有1个i,还有e,总共是:c, 2020-12-05 …
蛋白质是一类复杂的含氮化合物,每种蛋白质都有恒定的含氮量(约在14%-18%,质量分数),食品中蛋白 2020-12-22 …