早教吧作业答案频道 -->化学-->
汽车尾气中的NOx是大气污染物之一,用CH4催化还原NOx可以消除氮氧化物的污染.(1)已知:①CH4(g)+4NO2(g)催化剂4NO(g)+CO2(g)+2H2O(g)△H1=
题目详情
汽车尾气中的NOx是大气污染物之一,用CH4催化还原NOx可以消除氮氧化物的污染.
(1)已知:
①CH4(g)+4NO2(g)
4NO(g)+CO2(g)+2H2O(g)△H1=-574kJ•mol-1
②CH4(g)+4NO(g)
2N2(g)+CO2(g)+2H2O(g)△H2=-1160kJ•mol-1
③CH4(g)+2NO2(g)
N2(g)+CO2(g)+2H2O(g)
△H3=___.
(2)反应③在热力学上趋势很大,其原因是___.在固定容器中按一定比例混合CH4与NO2后,提高NO2转化率的反应条件是___
(3)在130℃和180℃时,分别将0.50mol CH4和a mol NO2充入1L的密闭容器中发生反应③,测得有关数据如表:
①开展实验1和实验2的目的是___.
②130℃时,反应到20分钟时,NO2的反应速率是___.
③180℃时达到平衡状态时,CH4的平衡转化率为___.
④已知130℃时该反应的化学平衡常数为6.4,试计算a=___.
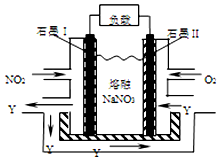
(4)NO2、O2和熔融NaNO3可制作燃料电池,其原理如图.该电池在使用过程中石墨I电极上生成氧化物Y,该电极反应为___.

(1)已知:
①CH4(g)+4NO2(g)
| 催化剂 |
| |
②CH4(g)+4NO(g)
| 催化剂 |
| |
③CH4(g)+2NO2(g)
| 催化剂 |
| |
△H3=___.
(2)反应③在热力学上趋势很大,其原因是___.在固定容器中按一定比例混合CH4与NO2后,提高NO2转化率的反应条件是___
(3)在130℃和180℃时,分别将0.50mol CH4和a mol NO2充入1L的密闭容器中发生反应③,测得有关数据如表:
| 实验编号 | 温度 | 0分钟 | 10分钟 | 20分钟 | 40分钟 | 50分钟 | |
| 1 | 130℃ | n(CH4)/mol | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
| 2 | 180℃ | n(CH4)/mol | 0.50 | 0.30 | 0.18 | 0.15 |
②130℃时,反应到20分钟时,NO2的反应速率是___.
③180℃时达到平衡状态时,CH4的平衡转化率为___.
④已知130℃时该反应的化学平衡常数为6.4,试计算a=___.
(4)NO2、O2和熔融NaNO3可制作燃料电池,其原理如图.该电池在使用过程中石墨I电极上生成氧化物Y,该电极反应为___.
▼优质解答
答案和解析
(1)①CH4(g)+4NO2(g)═4NO(g)+CO2(g)+2H2O(g)△H=-574kJ•mol-1
②CH4(g)+4NO(g)═2N2(g)+CO2(g)+2H2O(g)△H=-1160kJ•mol-1,(①+②)×
得CH4(g)+2NO2(g)
N2(g)+CO2(g)+2H2O(g))△H=-867kJ•mol-1,
故答案为:-867kJ•mol-1;
(2)反应③在热力学上趋势很大,该反应放出热热量大,即反应物和生成物的能量差大,因此热力学趋势大;该反应为气体体积增大的放热反应,所以降低温度、降低压强有利于提高NO2转化率;
故答案为:此反应放出的热量十分大;低温、低压;
(3)①实验中只有温度不同,所以实验目的是:研究温度对该化学平衡的影响,
故答案为:研究温度对该化学平衡的影响;
②v=
=
=0.0125mol/(L•min),
故答案为:0.0125mol/(L•min);
③甲烷的转化率=
=70%,
故答案为:70%;
④设二氧化氮的物质的量为a,
CH4(g)+2NO2(g)⇌N2(g)+CO2(g)+2H2O(g)
C0(mol/L):0.5 a 0 0 0
△C(mol/L):0.40 0.80 0.40 0.40 0.80
C平(mol/L):0.10 a-0.80 0.40 0.40 0.80
则:
,a=1.2,
故答案为:1.2;
(4)该原电池中通入二氧化氮的电极是负极、通入氧气的电极是正极,所以I是负极、II是正极,负极上生成氧化物,应该是二氧化氮失电子和硝酸根离子反应生成五氧化二氮,电极反应式为NO2+NO3--e-=N2O5,
故答案为:NO2+NO3--e-=N2O5.
②CH4(g)+4NO(g)═2N2(g)+CO2(g)+2H2O(g)△H=-1160kJ•mol-1,(①+②)×
| 1 |
| 2 |
| 催化剂 |
故答案为:-867kJ•mol-1;
(2)反应③在热力学上趋势很大,该反应放出热热量大,即反应物和生成物的能量差大,因此热力学趋势大;该反应为气体体积增大的放热反应,所以降低温度、降低压强有利于提高NO2转化率;
故答案为:此反应放出的热量十分大;低温、低压;
(3)①实验中只有温度不同,所以实验目的是:研究温度对该化学平衡的影响,
故答案为:研究温度对该化学平衡的影响;
②v=
| △c |
| △t |
| ||
| 20min |
故答案为:0.0125mol/(L•min);
③甲烷的转化率=
| (0.5-0.15)mol |
| 0.5mol |
故答案为:70%;
④设二氧化氮的物质的量为a,
CH4(g)+2NO2(g)⇌N2(g)+CO2(g)+2H2O(g)
C0(mol/L):0.5 a 0 0 0
△C(mol/L):0.40 0.80 0.40 0.40 0.80
C平(mol/L):0.10 a-0.80 0.40 0.40 0.80
则:
| 0.40×0.40×(0.80)2 |
| 0.10×(a-0.80) |
故答案为:1.2;
(4)该原电池中通入二氧化氮的电极是负极、通入氧气的电极是正极,所以I是负极、II是正极,负极上生成氧化物,应该是二氧化氮失电子和硝酸根离子反应生成五氧化二氮,电极反应式为NO2+NO3--e-=N2O5,
故答案为:NO2+NO3--e-=N2O5.
看了 汽车尾气中的NOx是大气污染...的网友还看了以下:
《化学反应的快慢和限度》在体积不变的密闭容器中,保持一定的温度发生下列反应:4A(g)+B(?)= 2020-05-12 …
根据下面的相关实验,请回答其中的问题:(1)实验A:用调节好的天平测出寿山石的质量为g,用量筒测出 2020-05-12 …
关于万有引力和重力加速度GM/r^2 = g我用这个公式算地球表面的重力加速度为什么是错的?引力常 2020-05-17 …
数据结构中关于图拓扑排序算法有个地方不太明白希望能得到解答我先把整个算法写下了吧StatusTop 2020-06-06 …
初学高数,求大神解答:x-+∞,limf(x)=+∞limg(x)=M<0,求证明limf(x)* 2020-06-06 …
杂技演员重力为G,用双手握住竖直的竹竿匀速上攀和匀速下滑,他所受的摩擦力分别是f1和f2,关于f1 2020-07-04 …
反比例函数导数如何求?那用(f/g)'=(f'g-g'f)/g^2用1/(X+2)举例说说吧 2020-07-30 …
随着汽车数量的逐年增多,汽车尾气污染已成为突出的环境问题之一。反应:2NO(g)+2CO(g)2CO 2020-11-11 …
根据如图所示仪器回答:(1)写出A、D、F仪器名称:A为;D为;F为.(2)说出E、G两种仪器的作用 2020-12-19 …
根据如图所示仪器回答:(1)写出A、D、F仪器名称:A为;D为;F为.(2)说出E、G两种仪器的作用 2020-12-19 …