在湿法炼锌的电解循环溶液中,较高浓度的Cl-会腐蚀阳极板而增大电解能耗.可向溶液中同时加入Cu和CuSO4,生成CuCl沉淀从而除去Cl-.根据溶液中平衡时相关离子浓度的关系图,下列说法错
在湿法炼锌的电解循环溶液中,较高浓度的Cl-会腐蚀阳极板而增大电解能耗.可向溶液中同时加入Cu和CuSO4,生成CuCl沉淀从而除去Cl-.根据溶液中平衡时相关离子浓度的关系图,下列说法错误的是( )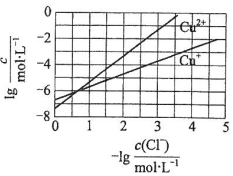
A. Ksp(CuCl)的数量级为10-7
B. 除Cl-.反应为Cu+Cu2++2Cl-=2CuCl
C. 加入Cu越多,Cu+浓度越高,除Cl-.效果越好
D. 2Cu+=Cu2++Cu平衡常数很大,反应趋于完全
B.涉及反应物为铜、硫酸铜以及氯离子,生成物为CuCl,反应的方程式为Cu+Cu2++2Cl-=2CuCl,故B正确;
C.发生Cu+Cu2++2Cl-=2CuCl,反应的效果取决于Cu2+的浓度,如Cu2+不足,则加入再多的Cu也不能改变效果,故C错误;
D.酸性条件下,Cu+不稳定,易发生2Cu+=Cu2++Cu,可知没有Cl-存在的情况下,2Cu+=Cu2++Cu趋向于完全,说明2Cu+=Cu2++Cu的平衡常数很大,故D正确.
故选C.
有关电路的一道二阶微分方程LCU''+LU'/R+U=C求U关于时间T的函数U是函数L,C,R,C 2020-04-26 …
电容器极板上的带电量Q能无限变大吗C=q/u电容量C的定义是升高单位极板所能容纳的电荷.可是如果q 2020-05-15 …
财务管理练习题,有关经济订货批量。(请附解题过程)C公司是一家冰箱生产企业,全年需要压缩机3600 2020-07-09 …
数学分析证明每个实数集的紧子集都是一个borel测度的支撑.支撑定义如下……一个定义在X集上的bo 2020-07-12 …
英语词典indicationn.1.指示;指点;表示[U][(+of)]2.征兆;迹象;暗示[C] 2020-07-20 …
∫dx/xlnxlnlnx(1)∫dx/[xlnxln(lnx)]=∫d(lnx)/[lnxln( 2020-08-01 …
以下哪项对RNA来说是正确的()A.(G+C)=(A+U)B.(G+A)=(C+U)C.(C+G)> 2020-11-06 …
不定积分初学者求助∫1/2x+1dx令u=2x+1,则du=2dx得∫1/2x+1dx=1/2∫du 2020-11-15 …
将两个电阻为R1和R2的电阻以某种方式连接后,两端加上电压U,R1消耗的功率是R2的3倍.若将R1与 2020-12-31 …
下列各项中字音不正确的一项是:()A.解剖(pōu)三昧(mèi)氛(fēn)围B.耗(hào)散瓦 2021-01-14 …