某溶液X中可能含有NO3-、Cl-、SO42-、CO32-、NH4+、Fe2+、Fe3+、Al3+和K+中的几种,且所含阴离子的物质的量相等.为确定该溶液X的成分,某学习小组做了如图实验,则下列说法正确的是()A.
某溶液X中可能含有NO3-、Cl-、SO42-、CO32-、NH4+、Fe2+、Fe3+、Al3+和K+中的几种,且所含阴离子的物质的量相等.为确定该溶液X的成分,某学习小组做了如图实验,则下列说法正确的是( )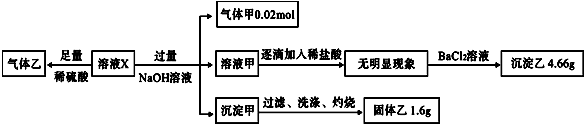
A. 气体甲、沉淀甲一定为纯净物
B. CO32-、Al3+、K+一定不存在
C. SO42-、NH4+一定存在,NO3-、Cl-可能不存在
D. 若含有Fe3+,则一定含有Cl-
溶液X与过量的NaOH溶液反应生成气体甲NH3为0.02mol,即溶液X中含0.02molNH4+;所得的溶液甲中逐滴加入稀盐酸,无现象,故溶液X中无Al3+;再继续加氯化钡溶液,生成沉淀乙,则乙为BaSO4,质量为4.66g,则物质的量为0.02mol,即溶液X中含0.02molSO42-;所得沉淀甲应为Fe(OH)2或Fe(OH)3或两者均有,经过滤、洗涤灼烧后所得的固体乙为Fe2O3,质量为1.6g,物质的量为0.01mol,故溶液X中含Fe2+或Fe3+或两者均有,且物质的量一定为0.02mol,由于Fe2+或Fe3+均能与CO32-发生双水解而不能共存,故溶液中无CO32-,则生成气体乙的反应只能是NO3-与Fe2+的氧化还原反应,故溶液中一定含Fe2+和NO3-,而所含阴离子的物质的量相等,即NO3-的物质的量也为0.02mol;
故现在溶液X中已经确定存在的离子是:阴离子:0.02molNO3-,0.02molSO42-,共带0.06mol负电荷;阳离子:0.02molNH4+,0.02molFe2+或Fe2+、Fe3+的混合物,所带的正电荷≥0.06mol,一定不含Al3+、CO32-,
根据溶液呈电中性可知,当 0.02mol全部是Fe2+时,阳离子所带正电荷为0.06mol,则Cl-可以存在,也可以不存在,若Cl-存在,则K+一定存在,若Cl-不存在,则K+一定不存在;
若溶液中含Fe3+,阳离子所带正电荷大于0.06mol,则溶液中一定存在Cl-,还可能存在K+.故溶液中可能含Cl-、K+.
A.气体甲为氨气,是纯净物,但沉淀甲可能是Fe(OH)2或Fe(OH)3或两者均有,不一定是纯净物,故A错误;
B.根据分析可知,K+可能存在,故b错误;
C.溶液中NO3-一定存在,故C错误;
D.由于溶液要保持电中性,故当溶液中含Fe3+时,则阳离子所带的正电荷>0.06mol,故溶液中一定含Cl-,故D正确;
故选D.
如曲线图表示血液中某种成分含量变化趋势,下列各项中,该曲线不能表示的是()A.血液流经肺部时氧气含 2020-04-07 …
某含苯环的化合物A因化学反应均能使酸性高锰酸钾溶液和溴水褪色,其相对分子质量为104,碳的质量分数 2020-05-12 …
下列关于双链DNA分子结构的叙述,正确的是()A.某DNA分子含有500个碱基,可能的排列方式有4 2020-05-13 …
1.已知某DNA分子含有1000个碱基对,其中一条链上A:G:T:C=1:2:3:4,该DNA分子 2020-05-14 …
通过粮食发酵可获得某含氧有机物X,其相对分子质量为46,其中碳的质量分数为52.2%,氢的质量分数 2020-05-14 …
matlab 求解微分方程组已知u1如何求u2i1=C1*du1/dt;%%含有微分i5=C3*d 2020-05-16 …
某含C、H、O三种元素的未知物A,经燃烧分析实验测定该未知物中碳的质量分数为52.16%,氢的质量 2020-05-16 …
现有三种合金,第一种含铜百分之60和含猛百分之40,第二种含猛百分之10和含镍百分之90,第三种含 2020-06-27 …
研宄者对某池塘中部分生物摄取的含物成分进行分析,并将结果记录在右表中.请回答问题.生物种类体内食物 2020-07-11 …
数学建模点菜问题(需要包含某些营养成份,又希望总价格最低)?点菜问题:我们在餐馆中点菜,需要包含某些 2020-11-28 …