早教吧作业答案频道 -->化学-->
某课外学习小组利用废旧铜箔电路板回收铜,并得到铁红(主要成分Fe2O3),其流程如图.请回答下列问题:(1)操作a和操作b都要用到玻璃棒,其作用是.(2)加入过量A的目的是,步
题目详情
某课外学习小组利用废旧铜箔电路板回收铜,并得到铁红(主要成分Fe2O3),其流程如图.
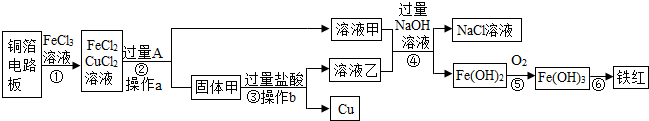
请回答下列问题:
(1)操作a和操作b都要用到玻璃棒,其作用是___.
(2)加入过量A的目的是___,步骤②的化学方程式为___,所得溶液甲的颜色是___.
(3)Fe(OH)2中铁元素的化合价是___.
(4)步骤①中发生反应的化学方程式为___.

请回答下列问题:
(1)操作a和操作b都要用到玻璃棒,其作用是___.
(2)加入过量A的目的是___,步骤②的化学方程式为___,所得溶液甲的颜色是___.
(3)Fe(OH)2中铁元素的化合价是___.
(4)步骤①中发生反应的化学方程式为___.
▼优质解答
答案和解析
由于目的是获得铜和铁红,所以需要在过程中铜离子转化为铜单质,根据流程可以看成铜应该出现在固体甲中,所以A就是转化铜离子用的铁粉,为使铜离子彻底转化,所以应该加入过量的铁粉.这样导致固体甲为生成的铜和剩余的铁粉.当加入过量盐酸时,使铁粉完全从铜粉中除掉,所以溶液乙为生成的氯化亚铁和剩余的盐酸.而溶液甲为氯化亚铁溶液.溶液甲和乙加入过量的氢氧化钠后生成氢氧化亚铁沉淀.因此:
(1)操作a和操作b都是将固体和液体的分离,因此操作a和操作b都为过滤,其中玻璃棒起引流作用;
故填:引流;
(2)加入过量的A是铁与氯化铜反应,把氯化铜中的铜全部置换出来,生成氯化亚铁和铜,氯化亚铁溶液为浅绿色;
故填:把氯化铜中的铜全部置换出来;Fe+CuCl2=FeCl2+Cu;浅绿色;
(3)氢氧根显-2价,设铁元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:x+(-1)×2=0,则x=+2价.
故填:+2价;
(4)步骤①中氯化铁与铜反应生成氯化铜和氯化亚铁,发生反应的化学方程式为2FeCl3+Cu═2FeCl2+CuCl2;
故答案为:2FeCl3+Cu═2FeCl2+CuCl2.
(1)操作a和操作b都是将固体和液体的分离,因此操作a和操作b都为过滤,其中玻璃棒起引流作用;
故填:引流;
(2)加入过量的A是铁与氯化铜反应,把氯化铜中的铜全部置换出来,生成氯化亚铁和铜,氯化亚铁溶液为浅绿色;
故填:把氯化铜中的铜全部置换出来;Fe+CuCl2=FeCl2+Cu;浅绿色;
(3)氢氧根显-2价,设铁元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:x+(-1)×2=0,则x=+2价.
故填:+2价;
(4)步骤①中氯化铁与铜反应生成氯化铜和氯化亚铁,发生反应的化学方程式为2FeCl3+Cu═2FeCl2+CuCl2;
故答案为:2FeCl3+Cu═2FeCl2+CuCl2.
看了 某课外学习小组利用废旧铜箔电...的网友还看了以下:
如图,PB切⊙O于B点,直线PO交⊙O于点E,F,过点B作PO的垂线BA,垂足为点D,交⊙O于点A 2020-05-17 …
无穷小运算证明:1o(x^2)+o(x^3)=o(x^2)2x·o(x^2)=o(x^3)说是用定 2020-06-03 …
概率条件概率条件概率的理解有点问题。做题是没什么问题。。比如有五个苹果3个红2个绿题目是:前2个苹 2020-06-13 …
一道关于矩形的题目O是矩形ABCD的对角线的交点,过O作EF垂直于AC分别交AD,BC于F,E,若 2020-06-18 …
发原色为红色,目标色为黄色,染出来的颜色是橙色吗?是不是就是三色原理中的红加黄等于橙?如果是的话! 2020-07-02 …
如图,AB是⊙O的切线,B为切点,BC是⊙O的弦,直线AC与⊙O交于D,角C=45°,DE⊥AB, 2020-07-11 …
求给以下算法复杂度排序增长速度由慢到快1)O(n^(3/4))O(log(n)^5)O(2^n)O 2020-07-23 …
请好心人帮我做下会计分录题目O(∩∩)O谢谢1、2011年6月24日,收到P公司交来的预付货款35, 2020-11-04 …
请在下列句子中选出字音有错误的一项A.屹立yì缜密zhěn渲染xuàn慰藉jiè熨帖yùB.红绡xi 2020-11-07 …
如图,O为△ABC内一点,∠A=80°,∠CBO=1/m∠CBA,∠BCO=1/m∠BCA(1)若m 2020-12-25 …