早教吧作业答案频道 -->化学-->
含铬(Ⅵ)废水能诱发致癌,对人类和自然环境有严重的破坏作用.利用Cu2O光催化可以处理含有Cr2O72-的废水.Ⅰ.制取Cu2O(1)电解法:利用铜和钛做电极,电解含有NaCl和NaOH的溶液时,反
题目详情
含铬(Ⅵ)废水能诱发致癌,对人类和自然环境有严重的破坏作用.利用Cu2O光催化可以处理含有Cr2O72-的废水.
Ⅰ.制取Cu2O
(1)电解法:利用铜和钛做电极,电解含有NaCl和NaOH的溶液时,反应只消耗了铜和水,体系pH及Cl-浓度维持不变(溶液体积变化忽略不计).
①阳极材料是___.
②阴极的电极反应式是;电解总反应为:___.
(2)还原法
①工业上可用肼(N2H4)与新制的Cu(OH)2反应制备纳米级Cu2O,同时放出N2,该反应的化学方程式为___.
②控制100℃、pH=5的条件时,利用亚硫酸钠与硫酸铜溶液反应可以制得Cu2O,同时产生SO2气体.反应过程中需要不断地加入烧碱,其原因是___.
Ⅱ.利用Cu2O光催化处理含有Cr2O72-的废水的研究.
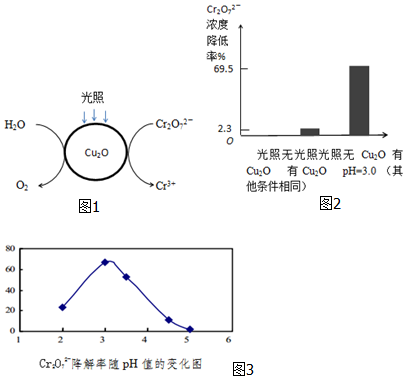
(1)光照射到Cu2O光催化剂上产生光催化反应,Cr2O72-和H2O分别在光催化反应中形成的微电极上发生电极反应,反应原理如图1所示.在图中用短线和箭头画出电子移动的方向,写出Cr2O72-转化Cr3+的电极反应.
(2)研究中对Cu2O的作用提出两种假设:
a.Cu2O作光催化剂;b.Cu2O 与Cr2O72-发生氧化还原反应.
已知:Cu2O的添加量是1.74×10-4mol/L,Cr2O72-的初始浓度是9.60×10-4mol/L;对比实验,反应1.5小时结果如图2所示.结合试剂用量数据和实验结果可得到的结论和依据是___.
(3)溶液的pH对Cr2O72-降解率的影响如3图所示.
已知:Cu2OCu+CuSO4;酸性越大,Cr2O72-被还原率越大.
①由图3可知,pH分别为2、3、4时,Cr2O72-的降解率最好的是___,其原因是___.
②已知pH=5时,会产生Cr(OH)3沉淀.pH=5时,Cr2O72-的降解率低的原因是___.
Ⅰ.制取Cu2O
(1)电解法:利用铜和钛做电极,电解含有NaCl和NaOH的溶液时,反应只消耗了铜和水,体系pH及Cl-浓度维持不变(溶液体积变化忽略不计).
①阳极材料是___.
②阴极的电极反应式是;电解总反应为:___.
(2)还原法
①工业上可用肼(N2H4)与新制的Cu(OH)2反应制备纳米级Cu2O,同时放出N2,该反应的化学方程式为___.
②控制100℃、pH=5的条件时,利用亚硫酸钠与硫酸铜溶液反应可以制得Cu2O,同时产生SO2气体.反应过程中需要不断地加入烧碱,其原因是___.
Ⅱ.利用Cu2O光催化处理含有Cr2O72-的废水的研究.
(1)光照射到Cu2O光催化剂上产生光催化反应,Cr2O72-和H2O分别在光催化反应中形成的微电极上发生电极反应,反应原理如图1所示.在图中用短线和箭头画出电子移动的方向,写出Cr2O72-转化Cr3+的电极反应.
(2)研究中对Cu2O的作用提出两种假设:
a.Cu2O作光催化剂;b.Cu2O 与Cr2O72-发生氧化还原反应.
已知:Cu2O的添加量是1.74×10-4mol/L,Cr2O72-的初始浓度是9.60×10-4mol/L;对比实验,反应1.5小时结果如图2所示.结合试剂用量数据和实验结果可得到的结论和依据是___.
(3)溶液的pH对Cr2O72-降解率的影响如3图所示.
已知:Cu2OCu+CuSO4;酸性越大,Cr2O72-被还原率越大.
①由图3可知,pH分别为2、3、4时,Cr2O72-的降解率最好的是___,其原因是___.
②已知pH=5时,会产生Cr(OH)3沉淀.pH=5时,Cr2O72-的降解率低的原因是___.

▼优质解答
答案和解析
Ⅰ、(1)①反应只消耗了铜和水,说明铜在阳极放电,所以阳极材料是铜,故答案为:Cu;
②反阴极发生还原反应,阴极的电极反应式是2H2O+2e-=H2↑+2OH-;电解总反应为:2Cu+H2O
H2↑+Cu2O,故答案为:2H2O+2e-=H2↑+2OH-;2Cu+H2O
H2↑+Cu2O;
(2)①根据反应物N2H4和Cu(OH)2,生成物是Cu20、H2O和N2,可得化学方程式为4Cu(OH)2+N2H4
N2↑+2Cu2O+6H2O,故答案为:4Cu(OH)2+N2H4
N2↑+2Cu2O+6H2O;
②亚硫酸钠与硫酸铜溶液反应可以制得Cu2O,同时产生SO2气体,反应方程式为:2CuSO4+3Na2SO3=Cu2O+2SO2↑+3Na2SO4,随反应的不断进行溶液的PH不断下降,所以加入氢氧化钠是调节溶液的PH的,故答案为:2CuSO4+3Na2SO3=Cu2O+2SO2↑+3Na2SO4反应过程中溶液的酸性不断地增强,为调节pH所以需要加入烧碱;
Ⅱ.(1)负极是水中-2价的氧失电子,而正极Cr2O72-转化Cr3+,电子的转移方向为: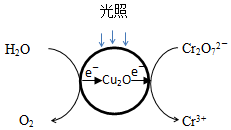 ,Cr2O72-转化Cr3+的电极反应为:Cr2O72-+14H++6e-=2Cr3++7H2O;故答案为:
,Cr2O72-转化Cr3+的电极反应为:Cr2O72-+14H++6e-=2Cr3++7H2O;故答案为: ;Cr2O72-+14H++6e-=2Cr3++7H2O;
;Cr2O72-+14H++6e-=2Cr3++7H2O;
(2)若发生氧化还原反应,则存在比例:3Cu2O-Cr2O72-,计算9.60×10-4×3×69.5%=2.00×10-3>1.74×10-4mol/L;实验可以看到只有氧化亚铜和只有光照时,Cr2O72-的转化率很低,说明反应条件是光照条件下和Cu2O同时存在,故答案为:Cu2O作光催化剂;3Cu2O-Cr2O72-,计算9.60×10-4×3×69.5%=2.00×10-3>1.74×10-4mol/L;实验可以看到只有氧化亚铜和只有光照时,Cr2O72-的转化率很低,说明反应条件是光照条件下和Cu2O同时存在;
(3)①由图可知:pH<2.5时Cu2O会歧化(转化)为Cu 和Cu2+,故答案为:pH=3;pH<2.5时Cu2O会歧化(转化)为Cu 和Cu2+,所以不选pH=2;酸性越大,Cr2O72-被还原率越大,pH=3酸性强于pH=4的溶液,所以选择pH=3;
②pH=5时,会产生Cr(OH)3沉淀覆盖在催化剂Cu2O表面,故答案为:pH=5时,会产生Cr(OH)3沉淀,沉淀覆盖在催化剂Cu2O表面,影响反应继续进行.
②反阴极发生还原反应,阴极的电极反应式是2H2O+2e-=H2↑+2OH-;电解总反应为:2Cu+H2O
| ||
| ||
(2)①根据反应物N2H4和Cu(OH)2,生成物是Cu20、H2O和N2,可得化学方程式为4Cu(OH)2+N2H4
| ||
| ||
②亚硫酸钠与硫酸铜溶液反应可以制得Cu2O,同时产生SO2气体,反应方程式为:2CuSO4+3Na2SO3=Cu2O+2SO2↑+3Na2SO4,随反应的不断进行溶液的PH不断下降,所以加入氢氧化钠是调节溶液的PH的,故答案为:2CuSO4+3Na2SO3=Cu2O+2SO2↑+3Na2SO4反应过程中溶液的酸性不断地增强,为调节pH所以需要加入烧碱;
Ⅱ.(1)负极是水中-2价的氧失电子,而正极Cr2O72-转化Cr3+,电子的转移方向为:
 ,Cr2O72-转化Cr3+的电极反应为:Cr2O72-+14H++6e-=2Cr3++7H2O;故答案为:
,Cr2O72-转化Cr3+的电极反应为:Cr2O72-+14H++6e-=2Cr3++7H2O;故答案为: ;Cr2O72-+14H++6e-=2Cr3++7H2O;
;Cr2O72-+14H++6e-=2Cr3++7H2O;(2)若发生氧化还原反应,则存在比例:3Cu2O-Cr2O72-,计算9.60×10-4×3×69.5%=2.00×10-3>1.74×10-4mol/L;实验可以看到只有氧化亚铜和只有光照时,Cr2O72-的转化率很低,说明反应条件是光照条件下和Cu2O同时存在,故答案为:Cu2O作光催化剂;3Cu2O-Cr2O72-,计算9.60×10-4×3×69.5%=2.00×10-3>1.74×10-4mol/L;实验可以看到只有氧化亚铜和只有光照时,Cr2O72-的转化率很低,说明反应条件是光照条件下和Cu2O同时存在;
(3)①由图可知:pH<2.5时Cu2O会歧化(转化)为Cu 和Cu2+,故答案为:pH=3;pH<2.5时Cu2O会歧化(转化)为Cu 和Cu2+,所以不选pH=2;酸性越大,Cr2O72-被还原率越大,pH=3酸性强于pH=4的溶液,所以选择pH=3;
②pH=5时,会产生Cr(OH)3沉淀覆盖在催化剂Cu2O表面,故答案为:pH=5时,会产生Cr(OH)3沉淀,沉淀覆盖在催化剂Cu2O表面,影响反应继续进行.
看了 含铬(Ⅵ)废水能诱发致癌,对...的网友还看了以下:
1、设有两个命题:1关于x的方程9∧x+(4+a)*3x+4=o有解2、函数f(x)=log2a∧ 2020-05-13 …
有一张厚度是0.1mm的纸,将它连续对折20次,会有多厚?有多少层楼高?(假设1层楼高3米)我知道 2020-05-16 …
微分方程(DifferentialEquations)1.是不是所有的微分方程都有解?2.微分方程 2020-05-17 …
高等代数的矩阵方程问题1、对任意矩阵A,求证XAX=A一定有解2、如果矩阵方程AY=C和ZB=C有 2020-06-10 …
1)已知两个数的和为4,积为-12,用韦达定理转化出一元二次方程求这两个数.(本题有解)(2分解因 2020-06-11 …
已知不等式|x+2|-|x+3|>m(1)若不等式有解(2)若不等式的解为R(3)若不等式解集为空 2020-07-31 …
二元一次方程组无解1.x+y=7,试确定a,c的值,使方程组:ax+2y=c(1)只有一个解(2) 2020-07-31 …
2^x=3这方程怎么解2的X次方=3这个方程怎么解?貌似解不出来的吧--、要在不能使用计算器的前提 2020-08-02 …
一道指数方程的题目lg(x-1)+lg(3-x)=lg(a-x)1)有解2)有两解3)有三解分别求 2020-08-02 …
对于一元一次方程、一元二次方程、二元一次方程组、三元一次方程组、分式,解的情况是不是都有两种情况? 2020-08-02 …