早教吧作业答案频道 -->化学-->
(1)已知H-H键能为436kJ•mol-1,H-N键键能为391kJ•mol-1,根据化学方程式:N2(g)+3H2(g)⇌2NH3(g)△H=-92.4kJ•mol-1.则N≡N键的键能是(2)事实证明,能设计成原电池的反应通常是放热反
题目详情
(1)已知H-H 键能为436kJ•mol-1,H-N键键能为391kJ•mol-1,根据化学方程式:N2(g)+3H2(g)⇌2NH3(g)△H=-92.4kJ•mol-1.则N≡N键的键能是___
(2)事实证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是___.
A.C(s)+H2O(g)═CO(g)+H2(g)△H>0
B.2H2(g)+O2(g)═2H2O(1)△H<0
C.NaOH(aq)+HC1(aq)=“NaC1(aq)“+H2O(1)△H<0
(3)以KOH溶液为电解质溶液,依据(2)所选反应设计一个原电池,其正极的电极反应式___.
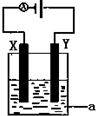
(4)电解原理在化学工业中有着广泛的应用.现将你设计的原电池通过导线与图中电解池相连,其中为 a电解液,X和Y均为惰性电极,则
①若a为CuSO4溶液,则电解时的化学反应方程式为___.
②若电解含有0.04molCuSO4和0.04molNaCl的混合溶液400ml,当阳极产生的气体672mL(标准状况下)时,溶液的pH=___(假设电解后溶液体积不变).
③若用此电解装置模拟工业精炼铜,则应将a改为___溶液,并将___极换成粗铜(填“X”或“Y”)
(2)事实证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是___.
A.C(s)+H2O(g)═CO(g)+H2(g)△H>0
B.2H2(g)+O2(g)═2H2O(1)△H<0
C.NaOH(aq)+HC1(aq)=“NaC1(aq)“+H2O(1)△H<0
(3)以KOH溶液为电解质溶液,依据(2)所选反应设计一个原电池,其正极的电极反应式___.
(4)电解原理在化学工业中有着广泛的应用.现将你设计的原电池通过导线与图中电解池相连,其中为 a电解液,X和Y均为惰性电极,则
①若a为CuSO4溶液,则电解时的化学反应方程式为___.
②若电解含有0.04molCuSO4和0.04molNaCl的混合溶液400ml,当阳极产生的气体672mL(标准状况下)时,溶液的pH=___(假设电解后溶液体积不变).
③若用此电解装置模拟工业精炼铜,则应将a改为___溶液,并将___极换成粗铜(填“X”或“Y”)

▼优质解答
答案和解析
(1)已知:H-H键能为436kJ/mol,H-N键能为391kJ/mol,令N≡N的键能为x,
对于反应N2(g)+3H2(g)=2NH3(g)△H=-92.4kJ/mol,
反应热=反应物的总键能-生成物的总键能,故x+3×436kJ/mol-2×3×391kJ/mol=-92.4kJ/mol,
解得:x=945.6 kJ/mol,故答案为:945.6 kJ/mol;
(2)能设计成原电池的反应通常是放热反应,且必须是能自发进行的氧化还原反应,
A.该反应是吸热反应,所以不能设计成原电池,故不选;
B.该反应是放热反应且能自发的进行氧化还原反应,所以能设计成原电池,故选;
C.该反应不是氧化还原反应,所以不能设计成原电池,故不选;
故选:B;
(3)以KOH溶液为电解质溶液的氢氧燃料电池中,正极上氧气得电子和水反应生成氢氧根离子,电极反应式为:O2+2H2O+4e-=4OH-,故答案为:O2+2H2O+4e-=4OH-;
(4)①电解硫酸铜溶液时,阳极上生成氧气,阴极上生成铜,同时溶液中生成硫酸,所以电池反应式为:2CuSO4+2H2O
2Cu+O2↑+2H2SO4,故答案为:2CuSO4+2H2O
2Cu+O2↑+2H2SO4;
②电解含有0.04molCuSO4和0.04molNaCl的混合溶液400ml,阳极上先生成氯气后生成氧气,阴极上先生成铜,后生成氢气,阳极上氯气完全析出时,氯气的体积=
=448mL<672mL,所以阳极上还有224mL氧气,阳极上转移电子的物质的量=0.04mol×1+
=0.08mol,阴极上铜完全析出时,需要电子的物质的量=0.04mol×2=0.08mol,所以阴极上不析出氢气,生成224mL氧气时,阳极附近同时生成C(H+)=
=0.1mol/L,所以溶液的pH=1,故答案为:1;
③工业精炼铜时,阳极是粗铜,电解液为含铜离子的溶液CuSO4或CuCl2,故答案为:CuSO4或CuCl2;Y.
对于反应N2(g)+3H2(g)=2NH3(g)△H=-92.4kJ/mol,
反应热=反应物的总键能-生成物的总键能,故x+3×436kJ/mol-2×3×391kJ/mol=-92.4kJ/mol,
解得:x=945.6 kJ/mol,故答案为:945.6 kJ/mol;
(2)能设计成原电池的反应通常是放热反应,且必须是能自发进行的氧化还原反应,
A.该反应是吸热反应,所以不能设计成原电池,故不选;
B.该反应是放热反应且能自发的进行氧化还原反应,所以能设计成原电池,故选;
C.该反应不是氧化还原反应,所以不能设计成原电池,故不选;
故选:B;
(3)以KOH溶液为电解质溶液的氢氧燃料电池中,正极上氧气得电子和水反应生成氢氧根离子,电极反应式为:O2+2H2O+4e-=4OH-,故答案为:O2+2H2O+4e-=4OH-;
(4)①电解硫酸铜溶液时,阳极上生成氧气,阴极上生成铜,同时溶液中生成硫酸,所以电池反应式为:2CuSO4+2H2O
| ||
| ||
②电解含有0.04molCuSO4和0.04molNaCl的混合溶液400ml,阳极上先生成氯气后生成氧气,阴极上先生成铜,后生成氢气,阳极上氯气完全析出时,氯气的体积=
| 0.04mol |
| 2 |
| 0.224L |
| 22.4L/mol |
| ||
| 0.4L |
③工业精炼铜时,阳极是粗铜,电解液为含铜离子的溶液CuSO4或CuCl2,故答案为:CuSO4或CuCl2;Y.
看了 (1)已知H-H键能为436...的网友还看了以下:
CO2和少量液体J反应生成KHCO3和白色难溶物L,L与NaOH溶液反应生成J溶液有部分物质及反应 2020-04-25 …
排列31524的逆序列是多少?a[j]等于在排列中先于j但大于j的整数的个数;它量度j反序程度.数 2020-06-12 …
“220V、5.5kW”的电动机,电阻为0.4Ω,它在正常工作时的电流为A,1s钟内产生的热量是J 2020-06-12 …
(2014•增城市一模)一块手机用的锂电池,上面标明电压为3.7V,容量为2000mAh.(1)该 2020-06-14 …
某电动自行车电瓶标有"48v40ah"等字样某电动车电瓶标有“48V40Ah”等字样,这个瓶正常时 2020-06-27 …
如图所示为手机电池,铭牌上标的正常工作的电压为3.7V,电池容量为800mA•h,如图甲.此电池在 2020-07-03 …
一台直流电动机运转时,线圈电阻为1Ω,接在电动机两端的电压为12V,干路中的电流为0.5A.求(1 2020-07-15 …
一台电风扇正常工作时,电机两端的电压为220V,线圈电阻为1.5Ω,通过线圈的电流为0.2A,这台 2020-07-15 …
小王家中的电能表如图所示,从表盘信息可知,他家接入的用电器总功率不能超过W.当家里只有电磁炉工作时, 2020-11-29 …
”220V,5.5KW“的电动.电阻0.4.求它在正常工作时的电流——,1秒产生的热量——,1秒有多 2020-12-13 …