早教吧作业答案频道 -->化学-->
异丙苯()氧化法是工业生产苯酚和丙酮最主要的方法.其反应和流程如下:氧化:+O→(异丙苯过氧氢)分H+50-60℃(丙嗣)物质丙酮
题目详情
异丙苯 (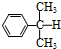 )氧化法是工业生产苯酚和丙酮最主要的方法.其反应和流程如下:
)氧化法是工业生产苯酚和丙酮最主要的方法.其反应和流程如下:
氧化: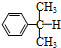 +O→
+O→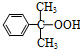 (异丙苯过氧氢)
(异丙苯过氧氢)
分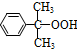
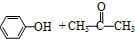 (丙嗣)
(丙嗣)
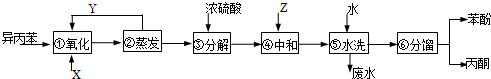
已知:
完成下列填空:
(1)X物质是___;Y物质是___.
(2)浓硫酸的作用是___,其优点是用量少,可能的缺点是___(写一条).
(3)Z物质最适宜选择___(选填编号).
a.NaOH b.Na2CO3 c.NaHCO3 d.CaCO3
(4)步骤⑥分馏,工业上在分馏塔中进行,如图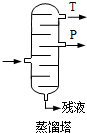 ,产品T是___,
,产品T是___,
请说明理由___.废水中苯酚的含量,可根据苯酚与溴水的反应,用以下方法测定:
①把20.00mL废水、20mLKBrO3和KBr混合溶液[其中:
c(KBrO3)=0.0100mol/L,c(KBr)=0.0600mol/L]置于锥形瓶中,再加入10mL6mol/L的盐酸,迅速盖好盖子,摇动锥形瓶.
②充分反应后,稍松开瓶塞,从瓶塞和瓶壁间缝隙迅速加入10%KI溶液10mL(过量),迅速加盖,充分摇匀.加入少许淀粉溶液.
③用0.0250mol/LNa2S2O3标准溶液滴定至终点.用去Na2S2O3溶液22.48mL.
(5)已知:BrO3-+5Br-+6H+→3Br2+3H2O;写出苯酚与浓溴水反应的化学方程式___;第1加盐酸、第②步加KI溶液,要迅速盖好盖子的原因是___.
(6)已知:I2+2Na2S2O3→2NaI+Na2S4O6;滴定终点的现象是___;该废水中苯酚的浓度是___mol/L(保留4位小数).
 )氧化法是工业生产苯酚和丙酮最主要的方法.其反应和流程如下:
)氧化法是工业生产苯酚和丙酮最主要的方法.其反应和流程如下:氧化:
 +O→
+O→ (异丙苯过氧氢)
(异丙苯过氧氢)分

| H+ |
| |
| 50-60℃ |
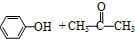 (丙嗣)
(丙嗣)
| 物质 | 丙酮 | 苯酚 | 异丙苯 |
| 密度(g/mL) | 0.7898 | 1.0722 | 0.8640 |
| 沸点/°C | 56.5 | 182 | 153 |
完成下列填空:
(1)X物质是___;Y物质是___.
(2)浓硫酸的作用是___,其优点是用量少,可能的缺点是___(写一条).
(3)Z物质最适宜选择___(选填编号).
a.NaOH b.Na2CO3 c.NaHCO3 d.CaCO3
(4)步骤⑥分馏,工业上在分馏塔中进行,如图
 ,产品T是___,
,产品T是___,请说明理由___.废水中苯酚的含量,可根据苯酚与溴水的反应,用以下方法测定:
①把20.00mL废水、20mLKBrO3和KBr混合溶液[其中:
c(KBrO3)=0.0100mol/L,c(KBr)=0.0600mol/L]置于锥形瓶中,再加入10mL6mol/L的盐酸,迅速盖好盖子,摇动锥形瓶.
②充分反应后,稍松开瓶塞,从瓶塞和瓶壁间缝隙迅速加入10%KI溶液10mL(过量),迅速加盖,充分摇匀.加入少许淀粉溶液.
③用0.0250mol/LNa2S2O3标准溶液滴定至终点.用去Na2S2O3溶液22.48mL.
(5)已知:BrO3-+5Br-+6H+→3Br2+3H2O;写出苯酚与浓溴水反应的化学方程式___;第1加盐酸、第②步加KI溶液,要迅速盖好盖子的原因是___.
(6)已知:I2+2Na2S2O3→2NaI+Na2S4O6;滴定终点的现象是___;该废水中苯酚的浓度是___mol/L(保留4位小数).
▼优质解答
答案和解析
用异丙苯氧化法生产苯酚和丙酮,由给予的反应信息,异丙苯与氧气在反应器①中发生氧化反应生成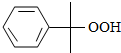 ,在②中蒸发分离出
,在②中蒸发分离出 ,未反应的异丙苯进行循环利用,
,未反应的异丙苯进行循环利用, 在③中在浓硫酸作催化剂条件下分解得到
在③中在浓硫酸作催化剂条件下分解得到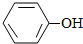 、
、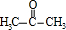 ,在④中加入Z,目的是中和硫酸,且不能与苯酚反应,可以是碳酸氢钠,然后⑤中水洗涤,再经过⑥分馏得丙酮、苯酚,
,在④中加入Z,目的是中和硫酸,且不能与苯酚反应,可以是碳酸氢钠,然后⑤中水洗涤,再经过⑥分馏得丙酮、苯酚,
(1)根据上面的分析可知,X物质是 氧气(或空气);Y物质是 异丙苯,
故答案为:氧气(或空气);异丙苯;
(2) 在③中在浓硫酸作催化剂条件下分解得到
在③中在浓硫酸作催化剂条件下分解得到 、
、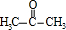 ,所以浓硫酸的作用是 催化剂,其优点是用量少,可能的缺点是 浓硫酸会使有机物发生脱水等副反应(浓硫酸与有机物混合放出大量热,使反应温度过高,不利于反应进行;或浓硫酸会腐蚀设备等),
,所以浓硫酸的作用是 催化剂,其优点是用量少,可能的缺点是 浓硫酸会使有机物发生脱水等副反应(浓硫酸与有机物混合放出大量热,使反应温度过高,不利于反应进行;或浓硫酸会腐蚀设备等),
故答案为:催化剂;浓硫酸会使有机物发生脱水等副反应(浓硫酸与有机物混合放出大量热,使反应温度过高,不利于反应进行;或浓硫酸会腐蚀设备等);
(3)根据上面的分析可知,Z可以是碳酸氢钠,故选c;
(4)步骤⑥分馏中,由于丙酮的沸点低于苯酚,则T为丙酮、P为苯酚,
故答案为:丙酮; 丙酮的沸点低;
(5)苯酚与浓溴水反应的化学方程式为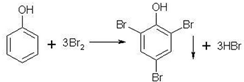 ,由于溴易挥发,所以第1加盐酸、第②步加KI溶液,要迅速盖好盖子,防止溴挥发,
,由于溴易挥发,所以第1加盐酸、第②步加KI溶液,要迅速盖好盖子,防止溴挥发,
故答案为: ;溴易挥发;
;溴易挥发;
(6)溶液中有淀粉,当达到滴定终点时,碘反应完全,所以滴定终点的现象是 由蓝色变为无色(或白色浑浊)且半分钟内不变色;
20mLKBrO3和KBr混合溶液[其中:c(KBrO3)=0.0100mol/L,c(KBr)=0.0600mol/L]置于锥形瓶中,再加入10mL6mol/L的盐酸,根据方程式BrO3-+5Br-+6H+→3Br2+3H2O可知,生成的溴的物质的量为3×0.0100mol/L×0.02L=6×10-4 mol,根据反应I2+2Na2S2O3→2NaI+Na2S4O6可知,由溴与碘化钾反应生成的碘的物质的量为0.0250mol/L×0.02248L×
=2.81×10-4 mol,所以与苯酚反应的溴的物质的量为6×10-4 mol-2.81×10-4 mol=3.19×10-4 mol,根据反应 可知,苯酚的物质的量为3.19×10-4 mol×
可知,苯酚的物质的量为3.19×10-4 mol×
=1.06×10-4 mol,所以废水中苯酚的浓度是
=0.0053mol/L,
故答案为:由蓝色变为无色(或白色浑浊)且半分钟内不变色;0.0053.
 ,在②中蒸发分离出
,在②中蒸发分离出 ,未反应的异丙苯进行循环利用,
,未反应的异丙苯进行循环利用, 在③中在浓硫酸作催化剂条件下分解得到
在③中在浓硫酸作催化剂条件下分解得到 、
、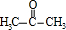 ,在④中加入Z,目的是中和硫酸,且不能与苯酚反应,可以是碳酸氢钠,然后⑤中水洗涤,再经过⑥分馏得丙酮、苯酚,
,在④中加入Z,目的是中和硫酸,且不能与苯酚反应,可以是碳酸氢钠,然后⑤中水洗涤,再经过⑥分馏得丙酮、苯酚,(1)根据上面的分析可知,X物质是 氧气(或空气);Y物质是 异丙苯,
故答案为:氧气(或空气);异丙苯;
(2)
 在③中在浓硫酸作催化剂条件下分解得到
在③中在浓硫酸作催化剂条件下分解得到 、
、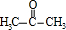 ,所以浓硫酸的作用是 催化剂,其优点是用量少,可能的缺点是 浓硫酸会使有机物发生脱水等副反应(浓硫酸与有机物混合放出大量热,使反应温度过高,不利于反应进行;或浓硫酸会腐蚀设备等),
,所以浓硫酸的作用是 催化剂,其优点是用量少,可能的缺点是 浓硫酸会使有机物发生脱水等副反应(浓硫酸与有机物混合放出大量热,使反应温度过高,不利于反应进行;或浓硫酸会腐蚀设备等),故答案为:催化剂;浓硫酸会使有机物发生脱水等副反应(浓硫酸与有机物混合放出大量热,使反应温度过高,不利于反应进行;或浓硫酸会腐蚀设备等);
(3)根据上面的分析可知,Z可以是碳酸氢钠,故选c;
(4)步骤⑥分馏中,由于丙酮的沸点低于苯酚,则T为丙酮、P为苯酚,
故答案为:丙酮; 丙酮的沸点低;
(5)苯酚与浓溴水反应的化学方程式为
 ,由于溴易挥发,所以第1加盐酸、第②步加KI溶液,要迅速盖好盖子,防止溴挥发,
,由于溴易挥发,所以第1加盐酸、第②步加KI溶液,要迅速盖好盖子,防止溴挥发,故答案为:
 ;溴易挥发;
;溴易挥发;(6)溶液中有淀粉,当达到滴定终点时,碘反应完全,所以滴定终点的现象是 由蓝色变为无色(或白色浑浊)且半分钟内不变色;
20mLKBrO3和KBr混合溶液[其中:c(KBrO3)=0.0100mol/L,c(KBr)=0.0600mol/L]置于锥形瓶中,再加入10mL6mol/L的盐酸,根据方程式BrO3-+5Br-+6H+→3Br2+3H2O可知,生成的溴的物质的量为3×0.0100mol/L×0.02L=6×10-4 mol,根据反应I2+2Na2S2O3→2NaI+Na2S4O6可知,由溴与碘化钾反应生成的碘的物质的量为0.0250mol/L×0.02248L×
| 1 |
| 2 |
 可知,苯酚的物质的量为3.19×10-4 mol×
可知,苯酚的物质的量为3.19×10-4 mol×| 1 |
| 3 |
| 1.06×10-4mol |
| 0.02L |
故答案为:由蓝色变为无色(或白色浑浊)且半分钟内不变色;0.0053.
看了 异丙苯()氧化法是工业生产苯...的网友还看了以下:
过氧化氢制取氧气二氧化锰可以做过氧化氢的的催化剂,制取氧气.H可代替二氧化锰做过氧化氢溶液分解反应 2020-05-13 …
如图1是高等生物细胞有氧呼吸过程的图解,图2表示大气中氧的浓度对植物组织内二氧化碳产生的影响;据图 2020-05-14 …
稀H2SO4为什么是非氧化性酸?一般情况下,S(+6)变成(+4)吗?我看的那些答案都说,主要体现 2020-05-14 …
化合物H是合成植物生长调节剂赤霉酸的重要中间体,其合成路线如下:(1)化合物H的含氧官能团为和(填 2020-07-10 …
(14分)A、B、C、D、G都是含有同一种短周期元素的化合物,E是氧化物,H是单质。根据下图转化关 2020-07-24 …
(2019•吉林模拟)1923年以前,甲醇一般是用木材或其废料h分解蒸馏来生产h.现在工业上合成甲醇 2020-11-12 …
工业上以黄铁矿为原料生产硫酸,其中重要的一步是催化氧化(生产中保持恒温恒容条件):2SO2(g)+O 2020-12-22 …
下列四个推断中,正确的是()A.氧化物都含有氧元素,所以含有氧元素的化合物一定是氧化物B.氧化反应中 2020-12-28 …
氨催化氧化是硝酸工业的基础,在某催化剂作用下只发生主反应①和副反应②,有关物质产率与温度的关系如图4 2021-02-16 …
氨催化氧化是硝酸工业的基础,在某催化剂作用下只发生主反应①和副反应②,有关物质产率与温度的关系如图. 2021-02-16 …