早教吧作业答案频道 -->化学-->
实验室需用230mL0.46mol•L-1的稀硫酸,用质量分数为98%的浓硫酸(密度为1.84g•cm-3)来配制,则:(1)需要量取该浓硫酸的体积为mL;(2)实验所用到的玻璃仪器除烧杯、玻璃棒外,还有
题目详情
实验室需用230mL0.46mol•L-1的稀硫酸,用质量分数为98%的浓硫酸(密度为1.84g•cm-3)来配制,则:
(1)需要量取该浓硫酸的体积为___mL;
(2)实验所用到的玻璃仪器除烧杯、玻璃棒外,还有___;
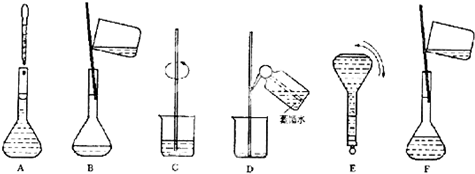
(3)配制过程中部分步骤和操作如下图所示:将上述实验步骤A-F按实验过程先后次序排列___.操作ABE用到了一种共同仪器,该仪器上标有:①温度、②浓度、③规格、④压强、⑤刻度线这五项中的___.(填数字符号)
(4)该同学实际配制得到的浓度为0.45mol•L-1,可能的原因是___
A.量取浓H2SO4时仰视刻度 B.容量瓶洗净后未经干燥处理
C.没有将洗涤液转入容量瓶 D.定容时仰视刻度.
(1)需要量取该浓硫酸的体积为___mL;
(2)实验所用到的玻璃仪器除烧杯、玻璃棒外,还有___;
(3)配制过程中部分步骤和操作如下图所示:将上述实验步骤A-F按实验过程先后次序排列___.操作ABE用到了一种共同仪器,该仪器上标有:①温度、②浓度、③规格、④压强、⑤刻度线这五项中的___.(填数字符号)

(4)该同学实际配制得到的浓度为0.45mol•L-1,可能的原因是___
A.量取浓H2SO4时仰视刻度 B.容量瓶洗净后未经干燥处理
C.没有将洗涤液转入容量瓶 D.定容时仰视刻度.
▼优质解答
答案和解析
(1)由于实验室无230mL容量瓶,故应选择250mL的容量瓶,故配制出250mL溶液. 由于浓硫酸的物质的量浓度为c=
=
=18.4mol/L,设需要的浓硫酸的体积为VmL,根据溶液稀释定律C浓V浓=C稀V稀可知:18.4mol/L×VmL=0.46mol/L×250mL,解得V=6.3mL,故答案为:6.3;
(2)根据配制步骤是计算、量取、稀释、冷却、移液、洗涤、定容、摇匀、装瓶可知所需的仪器为10mL量筒、烧杯、玻璃棒、250mL容量瓶和胶头滴管,故所需的玻璃仪器除烧杯、玻璃棒外,还有10mL量筒、250mL容量瓶和胶头滴管,故答案为:10mL量筒、250mL容量瓶和胶头滴管;
(3)根据配制步骤是计算、量取、稀释、冷却、移液、洗涤、定容、摇匀、装瓶可知正确的操作顺序是CBDFAE或CBDBFAE;操作ABE用到了一种共同仪器为250mL容量瓶,容量瓶上标有温度、容积和一条刻度线,即①③⑤,故答案为:CBDFAE或CBDBFAE;①③⑤;
(4)A.量取浓H2SO4时仰视刻度,则浓硫酸的体积偏大,故配制出的稀硫酸的浓度偏高,故A错误;
B.容量瓶洗净后未经干燥处理,对溶液浓度无影响,故B错误;
C.没有将洗涤液转入容量瓶,会导致溶质的损失,则浓度偏低,故C正确;
D.定容时仰视刻度,则溶液体积偏大,浓度偏低,故D正确.
故选CD.
| 1000ρω% |
| M |
| 1000×1.84×98% |
| 98 |
(2)根据配制步骤是计算、量取、稀释、冷却、移液、洗涤、定容、摇匀、装瓶可知所需的仪器为10mL量筒、烧杯、玻璃棒、250mL容量瓶和胶头滴管,故所需的玻璃仪器除烧杯、玻璃棒外,还有10mL量筒、250mL容量瓶和胶头滴管,故答案为:10mL量筒、250mL容量瓶和胶头滴管;
(3)根据配制步骤是计算、量取、稀释、冷却、移液、洗涤、定容、摇匀、装瓶可知正确的操作顺序是CBDFAE或CBDBFAE;操作ABE用到了一种共同仪器为250mL容量瓶,容量瓶上标有温度、容积和一条刻度线,即①③⑤,故答案为:CBDFAE或CBDBFAE;①③⑤;
(4)A.量取浓H2SO4时仰视刻度,则浓硫酸的体积偏大,故配制出的稀硫酸的浓度偏高,故A错误;
B.容量瓶洗净后未经干燥处理,对溶液浓度无影响,故B错误;
C.没有将洗涤液转入容量瓶,会导致溶质的损失,则浓度偏低,故C正确;
D.定容时仰视刻度,则溶液体积偏大,浓度偏低,故D正确.
故选CD.
看了 实验室需用230mL0.46...的网友还看了以下:
设f(x)=[g(x)-e^(-x)]/x(x不等于0)0(x=0),其中g(x)是有二阶连续函数 2020-05-17 …
有三个函数f(x)=tan(x+pi/4),g(x)=(1+tanx)(1-tanx),h(x)= 2020-05-17 …
如图所示,是一次实验情况的记录,请根据图示填写下表:玻璃杯和液体总质量/g玻璃杯和剩余液体的质量/ 2020-06-13 …
某同学用NaCl固体配制100mL2mol/L的NaCl溶液,请回答下列问题:(1)配制上述溶液所 2020-06-27 …
有人说G(X+1)=X(X>0)和G(X)=X-1(X>1)的定义域是一样的都是X>1,但是有些题 2020-07-04 …
在观察蚯蚓的实验中,我们发现()A.蚯蚓在玻璃板上运动比在糙纸上速度要快B.蚯蚓在玻璃板上运动比在 2020-07-11 …
对于正整数k,记g(k)表示k的最大奇数因数,例如g(1)=1,g(2)=1,g(10)=5.设Sn 2020-12-23 …
已知一函数满足x>0时,有g′(x)=2x2>g(x)x,则下列结论一定成立的是()A.g(2)2- 2020-12-23 …
以下几种材料:A.玻璃B.棉线C.玻璃钢D.尼龙E.有机玻璃F.钛合金G.麻布H.机动车轮胎I.铜导 2021-01-01 …
分段函数求导已知g(x)具有二阶连续导函数,且g(0)=1在计算某步时:当x=o时,f'(0)=li 2021-02-10 …