早教吧作业答案频道 -->化学-->
锡(Sn)在自然界中主要以锡石(SnO2)存在,锡石与焦炭在高温条件下可制得金属锡,锡的化合物广泛应用于汽车尾气催化剂,印染媒染剂、色料载体和电镀工业中,锡在化合物中主要以+2
题目详情
锡(Sn)在自然界中主要以锡石(SnO2)存在,锡石与焦炭在高温条件下可制得金属锡,锡的化合物广泛应用于汽车尾气催化剂,印染媒染剂、色料载体和电镀工业中,锡在化合物中主要以+2、+4价存在,某化学兴趣小组设计的由锡石制备SnSO4的合成路线如下:
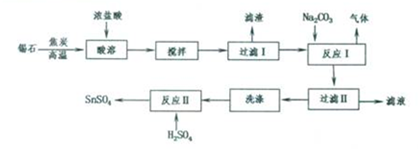
回答下列问题:
(1)Sn2+有强还原性,在酸性条件先易被空气中的O2氧化,反应的离子方程式为:___.
(2)过滤Ⅱ得到的沉淀时SnO,反应Ⅰ的化学方程式是:___;
(3)在洗涤后,检验沉淀是否洗涤干净的方法是:___.
(4)现欲在铁制品表面镀锡,以SnSO4溶液为电解液进行电镀,铁制品应该作___极,该电极反应式为:___.
(5)已知Ksp(SnS)=1×10-25,Ksp(SnS2)=2×10-27,若向含等浓度Sn2+、Sn4+的混合溶液中通入足量的H2S,___先沉淀(填Sn2+或Sn4+),待SnS、SnS2沉淀完全后,溶液中c(S2-)=c mol•L-1,此时
=___.
(6)该兴趣小组通过下列方法测定某金属锡样品的纯度(杂质不参与反应);
①向样品中加入过量的盐酸:Sn+2H+=Sn2++H2↑
②向反应完成的溶液中加入过量的FeCl3:Sn2++2Fe3+=Sn4++2Fe2+;
③用已知浓度的重铬酸钾溶液滴定生成的Fe2+:6Fe2++Cr2O72-+14H+=6Fe3++2Cr3++7H2O
现有金属锡样品0.8000g,经上述各步反应后共用去0.1000mol•L-1 K2Cr2O7溶液20.00mL.则样品中锡的质量分数是___.

回答下列问题:
(1)Sn2+有强还原性,在酸性条件先易被空气中的O2氧化,反应的离子方程式为:___.
(2)过滤Ⅱ得到的沉淀时SnO,反应Ⅰ的化学方程式是:___;
(3)在洗涤后,检验沉淀是否洗涤干净的方法是:___.
(4)现欲在铁制品表面镀锡,以SnSO4溶液为电解液进行电镀,铁制品应该作___极,该电极反应式为:___.
(5)已知Ksp(SnS)=1×10-25,Ksp(SnS2)=2×10-27,若向含等浓度Sn2+、Sn4+的混合溶液中通入足量的H2S,___先沉淀(填Sn2+或Sn4+),待SnS、SnS2沉淀完全后,溶液中c(S2-)=c mol•L-1,此时
| c(Sn2+) |
| c(Sn4+) |
(6)该兴趣小组通过下列方法测定某金属锡样品的纯度(杂质不参与反应);
①向样品中加入过量的盐酸:Sn+2H+=Sn2++H2↑
②向反应完成的溶液中加入过量的FeCl3:Sn2++2Fe3+=Sn4++2Fe2+;
③用已知浓度的重铬酸钾溶液滴定生成的Fe2+:6Fe2++Cr2O72-+14H+=6Fe3++2Cr3++7H2O
现有金属锡样品0.8000g,经上述各步反应后共用去0.1000mol•L-1 K2Cr2O7溶液20.00mL.则样品中锡的质量分数是___.
▼优质解答
答案和解析
SnO2粉末在高温度下与焦炭反应得到金属锡,加浓盐酸进行溶解并过滤得到SnCl2溶液,向其中加碳酸钠,将Sn元素以SnO形式沉淀,过滤洗涤得纯净的SnO,加稀硫酸,得SnSO4溶液,加热浓缩、冷却结晶、过滤、洗涤,制得SnSO4晶体;
(1)在酸性条件Sn2+被空气中的O2氧化成Sn4+,发生反应的离子反应方程式为:2Sn2++O2+4H+=2Sn4++2H2O;故答案为:2Sn2++O2+4H+=2Sn4++2H2O;
(2)反应Ⅰ得到沉淀是SnO,Sn元素化合价为变化,属于非氧化还原反应,同时生成气体,该气体为二氧化碳,离子方程式为:Sn2++CO32-═SnO↓+CO2↑,
故答案为:Sn2++CO32-═SnO↓+CO2↑;
(3)取最后一次洗涤液适量于试管中并滴加稀硝酸酸化,然后滴加硝酸银溶液,无白色沉淀,证明沉淀洗涤干净,若有白色沉淀生成,可证明洗涤液里含有Cl-,沉淀洗涤不干净;故答案为:取最后一次洗涤液适量于试管中并滴加稀硝酸酸化,然后滴加硝酸银溶液,无白色沉淀,证明沉淀洗涤干净;
(4)在铁制品表面镀锡时,阴极为铁,发生电极反应为Sn2++2e-=Sn,故答案为:阴;Sn2++2e-=Sn;
(5)设浓度均为1mol/L的Sn2+、Sn4+的混合溶液中,根据Ksp(SnS)=1×10-25,Ksp(SnS2)=2×10-27,可知SnS开始沉淀时所需要c(S2-)=1×10-25mol/L,SnS2开始沉淀时所需要c(S2-)=
mol/L,故Sn2+最先沉淀;当溶液中c(S2-)=c mol•L-1时,溶液中c(Sn2+)=
;c(Sn4+)=
,则
=
=50c,故答案为:Sn2+;50c;
(6)0.1000mol•L-1 K2Cr2O7溶液20.00mL中Cr2O72-的物质的量为0.1000mol•L-1×0.02L=0.002mol;根据关系式3Sn~6Fe2+~Cr2O72-可知Sn的物质的量为0.002mol×3=0.006mol,则样品的质量分数为
×100%=89.25%,故答案为:89.25%.
(1)在酸性条件Sn2+被空气中的O2氧化成Sn4+,发生反应的离子反应方程式为:2Sn2++O2+4H+=2Sn4++2H2O;故答案为:2Sn2++O2+4H+=2Sn4++2H2O;
(2)反应Ⅰ得到沉淀是SnO,Sn元素化合价为变化,属于非氧化还原反应,同时生成气体,该气体为二氧化碳,离子方程式为:Sn2++CO32-═SnO↓+CO2↑,
故答案为:Sn2++CO32-═SnO↓+CO2↑;
(3)取最后一次洗涤液适量于试管中并滴加稀硝酸酸化,然后滴加硝酸银溶液,无白色沉淀,证明沉淀洗涤干净,若有白色沉淀生成,可证明洗涤液里含有Cl-,沉淀洗涤不干净;故答案为:取最后一次洗涤液适量于试管中并滴加稀硝酸酸化,然后滴加硝酸银溶液,无白色沉淀,证明沉淀洗涤干净;
(4)在铁制品表面镀锡时,阴极为铁,发生电极反应为Sn2++2e-=Sn,故答案为:阴;Sn2++2e-=Sn;
(5)设浓度均为1mol/L的Sn2+、Sn4+的混合溶液中,根据Ksp(SnS)=1×10-25,Ksp(SnS2)=2×10-27,可知SnS开始沉淀时所需要c(S2-)=1×10-25mol/L,SnS2开始沉淀时所需要c(S2-)=
| 2×10-27 |
| 1×10-25 |
| cmol/L |
| 2×10-27 |
| c2(mol/L) |
| Sn2+ |
| Sn4+ |
| ||
|
(6)0.1000mol•L-1 K2Cr2O7溶液20.00mL中Cr2O72-的物质的量为0.1000mol•L-1×0.02L=0.002mol;根据关系式3Sn~6Fe2+~Cr2O72-可知Sn的物质的量为0.002mol×3=0.006mol,则样品的质量分数为
| 0.006mol×119g/mol |
| 0.800g |
看了 锡(Sn)在自然界中主要以锡...的网友还看了以下:
为防止汽车尾气对环境的污染需在汽车排气管上安装“催化转化器”在催化剂的作用下使为其中的一氧化碳和一 2020-04-11 …
将7×7的棋盘中的2个方格染成黄色,其余的染成绿色.若一种染色法经过在棋盘的平面中旋转而得到,那么 2020-05-21 …
下列与实验操作相关的叙述正确的是()A.用苏丹Ⅲ染液将花生子叶切片染色后,需要用显微镜才能看到染成 2020-07-14 …
锡(Sn)在自然界中主要以锡石(SnO2)存在,锡石与焦炭在高温条件下可制得金属锡,锡的化合物广泛 2020-07-16 …
正四面体顶角染色若在一个正四面体的四个顶角用兵19种颜色染色,染的颜色可重复,共有几种染法?(1) 2020-07-16 …
下列关于染色体的叙述中,不正确的是()A.染色体是细胞核中容易被碱性染料染成深色的物质B.染色体和 2020-11-10 …
在图所示的质粒PZHZ11(总长为3.6kb,1kb=1000对碱基因)中,lacZ基因编码β-半乳 2020-11-10 …
染色观察是生物实验常用的方法,下列有关染色的描述正确的是()。A.观察低温诱导染色体数目加倍,可用卡 2020-12-23 …
下列关于染色体的叙述,不正确的是()A.蓝藻细胞在进行有丝分裂时也能形成染色体B.严格地说,只有在细 2020-12-26 …
下列对染色质和染色体的说法中错误的是()A.染色质是细胞核内易被碱性染料染成深色的物质B.染色质和染 2021-01-12 …