早教吧作业答案频道 -->化学-->
氯化铁是实验室中的重要试剂.某同学用mg含有铁锈(Fe2O3)的废铁屑来制取FeCl3•6H2O晶体,同时测定废铁屑中铁的质量分数,为此设计了如下装置(夹持装置略,气密性已检验):操作步
题目详情
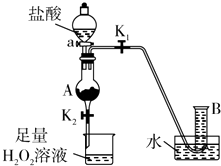
氯化铁是实验室中的重要试剂.某同学用m g含有铁锈(Fe2O3)的废铁屑来制取FeCl3•6H2O晶体,同时测定废铁屑中铁的质量分数,为此设计了如下装置(夹持装置略,气密性已检验):
操作步骤如下:
Ⅰ.打开弹簧夹K1、关闭弹簧夹K2,并打开活塞a,缓慢滴加盐酸.
Ⅱ.当…时,关闭弹簧夹K1、打开弹簧夹K2,当A中溶液完全进入烧杯后关闭活塞a.
Ⅲ.将烧杯中溶液蒸发浓缩、冷却结晶、过滤后得到FeCl3•6H2O晶体.
请回答:
(1)A中发生的置换反应的化学方程式是___.
(2)操作Ⅱ中“…”的内容是___,烧杯中的现象是___,相应的离子方程式和化学方程式是___、___.
(3)操作Ⅲ不采用直接加热制FeCl3•6H2O晶体的原因是___(用简要文字并结合离子方程式解释).
(4)测得B中所得的气体是VmL(标准状况时),由此计算出该废铁屑中铁的质量分数是
,该数值比实际数值偏低,若实验过程操作无误,偏低的原因是___.
(5)为了准确测定铁的质量分数,可以另取mg废铁屑和某种常见的还原性气体在加热时充分反应到恒重,测得实验后剩余固体质量是wg由此求出铁的准确质量分数是___(用含m和w的式子表示).
操作步骤如下:
Ⅰ.打开弹簧夹K1、关闭弹簧夹K2,并打开活塞a,缓慢滴加盐酸.
Ⅱ.当…时,关闭弹簧夹K1、打开弹簧夹K2,当A中溶液完全进入烧杯后关闭活塞a.
Ⅲ.将烧杯中溶液蒸发浓缩、冷却结晶、过滤后得到FeCl3•6H2O晶体.
请回答:

(1)A中发生的置换反应的化学方程式是___.
(2)操作Ⅱ中“…”的内容是___,烧杯中的现象是___,相应的离子方程式和化学方程式是___、___.
(3)操作Ⅲ不采用直接加热制FeCl3•6H2O晶体的原因是___(用简要文字并结合离子方程式解释).
(4)测得B中所得的气体是VmL(标准状况时),由此计算出该废铁屑中铁的质量分数是
| V |
| 400m |
(5)为了准确测定铁的质量分数,可以另取mg废铁屑和某种常见的还原性气体在加热时充分反应到恒重,测得实验后剩余固体质量是wg由此求出铁的准确质量分数是___(用含m和w的式子表示).
▼优质解答
答案和解析
(1)铁与盐酸反应的方程式是:Fe+2HCl=FeCl2+H2↑,故答案是:Fe+2HCl=FeCl2+H2↑;
(2)当A中固体完全消失,铁完全和盐酸反应后,反应结束;当A中溶液完全进入烧杯,生成的氯化亚铁被氧化成黄色的氯化铁,生成的氯化铁作催化剂,使双氧水分解,反应的方程式为2Fe2++H2O2+2H+=2Fe3++2H2O,2H2O2
2H2O+O2↑,
故答案是:当A中固体完全消失;无色溶液逐渐变黄,有气泡产生;2Fe2++H2O2+2H+=2Fe3++2H2O,2H2O2
2H2O+O2↑;
(3)由于氯化铁溶液中存在反应Fe3++3H2O⇌Fe(OH)3+3H+,该反应吸热,加入会促进水解,生成了氢氧化铁沉淀,无法制取氯化铁晶体,
故答案是:Fe3++3H2O⇌Fe(OH)3+3H+,加热会促进FeCl3水解,产生Fe(OH)3;
(4)由于废铁屑中含有氧化铁,和盐酸反应生成的三价铁离子能够和铁反应,导致铁减少,置换的氢气体积减少,
故答案是:Fe3+和Fe发生反应消耗部分Fe,使与盐酸反应的Fe相应减少;
(5)mg废铁屑中的氧化铁被还原后质量变成wg铁,质量差(m-w)g就是氧化铁中氧元素的质量,n(O)=
mol,n(Fe2O3)=
×n(O)=
mol,
铁的质量分数为
=
,
故答案是:
.
(2)当A中固体完全消失,铁完全和盐酸反应后,反应结束;当A中溶液完全进入烧杯,生成的氯化亚铁被氧化成黄色的氯化铁,生成的氯化铁作催化剂,使双氧水分解,反应的方程式为2Fe2++H2O2+2H+=2Fe3++2H2O,2H2O2
| ||
故答案是:当A中固体完全消失;无色溶液逐渐变黄,有气泡产生;2Fe2++H2O2+2H+=2Fe3++2H2O,2H2O2
| ||
(3)由于氯化铁溶液中存在反应Fe3++3H2O⇌Fe(OH)3+3H+,该反应吸热,加入会促进水解,生成了氢氧化铁沉淀,无法制取氯化铁晶体,
故答案是:Fe3++3H2O⇌Fe(OH)3+3H+,加热会促进FeCl3水解,产生Fe(OH)3;
(4)由于废铁屑中含有氧化铁,和盐酸反应生成的三价铁离子能够和铁反应,导致铁减少,置换的氢气体积减少,
故答案是:Fe3+和Fe发生反应消耗部分Fe,使与盐酸反应的Fe相应减少;
(5)mg废铁屑中的氧化铁被还原后质量变成wg铁,质量差(m-w)g就是氧化铁中氧元素的质量,n(O)=
| (m-w) |
| 16 |
| 1 |
| 3 |
| m-w |
| 46 |
铁的质量分数为
m-
| ||
| m |
m-
| ||
| m |
故答案是:
m-
| ||
| m |
看了 氯化铁是实验室中的重要试剂....的网友还看了以下:
同温同压下,某容器充满氧气重16克,充满C二氧化碳重22克,现在充满某气体重44克,则某气体的摩尔质 2020-03-30 …
CO和CO2性质不同,尤其是化学性质的不同,原因是()A.CO不溶于水B.CO2比空气重C.二者分 2020-05-13 …
同温同压下,某容器充满氧气重16g,若充满二氧化碳重22g,现充满某气体重44g,则某气体的摩尔质 2020-05-20 …
同温同压下,某容器充满O2重16g,若充满CO2重22g,现充满某气体重44g,则某气体的摩尔质量 2020-05-20 …
为了应对日益严重的气候问题,某气象仪器科研单位研究出一种新的“弹射型”气象仪器,这种仪器可以弹射到 2020-06-11 …
同温同压下,某容器充满氧气重116g,若充满二氧化碳重112g,现充满某气体重114g,则某气体的 2020-06-13 …
同温、同压下,某瓶充满O2时重116g,充满CO2时重122g,充满某气体时重114g,则某气体可 2020-06-13 …
归纳推理是学习化学的重要方法之一.下列推理正确的是()A.某气体能使燃着的木条熄灭,该气体一定是二 2020-07-05 …
1.同温同压下,具有相同体积的任何气体中含有的分子数相同.在一定温度和压强下,10体积气体A2跟30 2020-11-20 …
气体密度同温同压,某容器充满N2重114克,若充满氦气重102克,现充满某气体重创116克,则某气体 2020-12-02 …