早教吧作业答案频道 -->化学-->
空气吹出法是目前海水提溴的最主要方法之一.其工艺流程如图所示:(1)步骤④利用了SO2的还原性,反应的离子方程式为.(2)步骤⑧中溴蒸气冷凝后得到液溴与溴水的混合物,可利
题目详情
空气吹出法是目前海水提溴的最主要方法之一.其工艺流程如图所示:
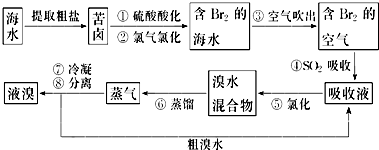
(1)步骤④利用了SO2的还原性,反应的离子方程式为___.
(2)步骤⑧中溴蒸气冷凝后得到液溴与溴水的混合物,可利用它们的相对密度相差较大的特点进行分离.所用分离仪器的名称是___.
(3)步骤①、②之后并未直接用“含Br2的海水”进行蒸馏得到液溴,而是经过空气吹出、SO2吸收、氯化后再蒸馏,这样操作的意义是___.
(4)根据上述反应判断SO2、Cl2、Br2三种物质氧化性由强到弱的顺序是___.

(1)步骤④利用了SO2的还原性,反应的离子方程式为___.
(2)步骤⑧中溴蒸气冷凝后得到液溴与溴水的混合物,可利用它们的相对密度相差较大的特点进行分离.所用分离仪器的名称是___.
(3)步骤①、②之后并未直接用“含Br2的海水”进行蒸馏得到液溴,而是经过空气吹出、SO2吸收、氯化后再蒸馏,这样操作的意义是___.
(4)根据上述反应判断SO2、Cl2、Br2三种物质氧化性由强到弱的顺序是___.
▼优质解答
答案和解析
苦卤中含有溴,在酸性条件下通入氯气,可发生置换反应生成溴单质,吹入空气,将溴分离出来,然后溴与二氧化硫发生反应生成HBr和硫酸,再通入氯气,生成溴,然后分液、蒸馏和得到液溴,
(1)SO2和氯气、水反应生成硫酸和氢溴酸,反应的离子方程式为:Br2+SO2+2H2O=2HBr+H2SO4,
故答案为:Br2+SO2+2H2O=4H++2Br-+SO42-;
(2)由于液溴与溴水不相溶,可用分液漏斗分离,
故答案为:分液漏斗;
(3)在溴水中,溴的沸点是58.5°C,水的是100°C,温度过高,大量水蒸气随之排出,溴气中水分增加;温度过低,溴不能完全蒸出,产率低,故答案为:温度过高,大量水蒸气随之排出,溴气中水分增加;温度过低,溴不能完全蒸出,产率低;
(4)根据以上分析可知,氯气能够将溴离子氧化成溴单质,溴单质能够氧化二氧化硫,则说明氧化性强弱为:Cl2>Br2>SO2,
故答案为:Cl2>Br2>SO2.
(1)SO2和氯气、水反应生成硫酸和氢溴酸,反应的离子方程式为:Br2+SO2+2H2O=2HBr+H2SO4,
故答案为:Br2+SO2+2H2O=4H++2Br-+SO42-;
(2)由于液溴与溴水不相溶,可用分液漏斗分离,
故答案为:分液漏斗;
(3)在溴水中,溴的沸点是58.5°C,水的是100°C,温度过高,大量水蒸气随之排出,溴气中水分增加;温度过低,溴不能完全蒸出,产率低,故答案为:温度过高,大量水蒸气随之排出,溴气中水分增加;温度过低,溴不能完全蒸出,产率低;
(4)根据以上分析可知,氯气能够将溴离子氧化成溴单质,溴单质能够氧化二氧化硫,则说明氧化性强弱为:Cl2>Br2>SO2,
故答案为:Cl2>Br2>SO2.
看了 空气吹出法是目前海水提溴的最...的网友还看了以下:
计算外加剂的减水率.某一高效减水剂,在减水率测定中测得混凝土用水量为200kg/m³,坍落度80m 2020-05-16 …
要详细的计算过程谢谢已知混凝土试拌调整后,各组成材料的用量分别为:水泥4.6kg、水2.6kg、砂 2020-06-23 …
3、某混凝土经计算得初步配合比,每方混凝土材料用量为:水=195kg,水泥=390kg,砂=588 2020-06-23 …
大学土木工程材料一道题,已知混凝土试拌调整后,各组成材料的用量分别为:水泥4.6Kg、水2.6kg 2020-06-23 …
按初步计算配合比,各组成材料的用量分别为水泥4.5砂9.9Kg石子20.25水2.34.经实验发现 2020-06-29 …
未初凝的混凝土重量?我今天用电子称称了一下,我称了3个0.1m的立方体,总重量为7.485kg,推 2020-07-05 …
如何算配制1立方米混凝土时各材料的用量某工程用42.5的普通水泥配制C20混凝土,已知水灰比为0. 2020-07-22 …
水泥混凝土配合比初步设计算题体积法在进行水泥混凝土初步设计时,若已求出水泥用量为360kg/m3, 2020-07-30 …
混凝土的级配问题试配少量混凝土,其组成材料用量水泥4.5kg,水2.7kg,砂9.9kg,碎石18. 2020-11-11 …
做sds-page电泳时有一步是要将样本煮沸低温离心的,请问这一步有什么用另外,我这里没有一些配料, 2020-12-24 …