早教吧作业答案频道 -->化学-->
某城市实时空气质量检测报告中标明空气中包含多种气体污染物,如CO、氮氧化物(NOx)、SO2等.(1)CO的检测.①粉红色的PdCl2溶液可以检验空气中少量的CO.若空气中含CO,则溶液中会产
题目详情
某城市实时空气质量检测报告中标明空气中包含多种气体污染物,如CO、氮氧化物(NOx)、SO2等.
(1)CO的检测.
①粉红色的PdCl2溶液可以检验空气中少量的CO.若空气中含CO,则溶液中会产生黑色的Pd沉淀,每生成5.3gPd沉淀,反应转移电子数为___.
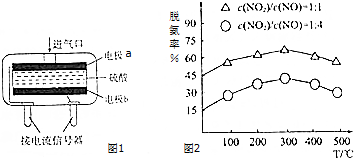
②使用电化学一氧化碳气体传感器定量检测空气中CO含量,其模型如图1所示,这种传感器利用了燃料电池原理.则该电池的负极反应式为___.
(2)活性炭可处理大气污染物NO.在2L密闭容器中加入NO和活性炭(无杂质),生成气体E和F.当温度分别在T1和T2时,测得各物质平衡时物质的量如表:
①上述反应T1℃时的平衡常数为K=___.
②根据上述信息判断,温度T1和T2的关系是(填序号)___.
a.T1>T2 b.T1<T2 c.无法比较
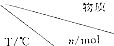
(3)NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术,反应原理为NO(g)+NO2(g)+2NH3(g)⇌2N2(g)+3H2O,△<0在氨气足量的情况下,不同
、不同温度对脱氨率的影响如图2所示.请回答温度对脱氨率的影响___,给出合理的解释___.
(4)硫酸厂尾气中的SO2可催化氧化生成SO3,再合成硫酸.在某温度时,向10L的密闭容器中加入4.0molSO2和10.0molO2,反应达到平衡,改变下列条件,再次达到平衡时,能使O2的新平衡浓度和原来平衡浓度相同的是___(填序号)
A.在其他条件不变时,减少容器的容积
B.保持温度和容器内压强不变,再充入2.0mol SO2和5.0mol O2
C.保持温度和容器体积不变,再充入SO2和SO3,使之浓度扩大为原来的两倍.

(1)CO的检测.
①粉红色的PdCl2溶液可以检验空气中少量的CO.若空气中含CO,则溶液中会产生黑色的Pd沉淀,每生成5.3gPd沉淀,反应转移电子数为___.
②使用电化学一氧化碳气体传感器定量检测空气中CO含量,其模型如图1所示,这种传感器利用了燃料电池原理.则该电池的负极反应式为___.
(2)活性炭可处理大气污染物NO.在2L密闭容器中加入NO和活性炭(无杂质),生成气体E和F.当温度分别在T1和T2时,测得各物质平衡时物质的量如表:
 | 活性炭 | NO | E | F |
| 初始 | 2.030 | 0.10 | 0 | 0 |
| T1 | 2.000 | 0.040 | 0.030 | 0.030 |
| T2 | 2.005 | 0.050 | 0.025 | 0.025 |
②根据上述信息判断,温度T1和T2的关系是(填序号)___.
a.T1>T2 b.T1<T2 c.无法比较
(3)NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术,反应原理为NO(g)+NO2(g)+2NH3(g)⇌2N2(g)+3H2O,△<0在氨气足量的情况下,不同
| c(NO2) |
| c(NO) |
(4)硫酸厂尾气中的SO2可催化氧化生成SO3,再合成硫酸.在某温度时,向10L的密闭容器中加入4.0molSO2和10.0molO2,反应达到平衡,改变下列条件,再次达到平衡时,能使O2的新平衡浓度和原来平衡浓度相同的是___(填序号)
A.在其他条件不变时,减少容器的容积
B.保持温度和容器内压强不变,再充入2.0mol SO2和5.0mol O2
C.保持温度和容器体积不变,再充入SO2和SO3,使之浓度扩大为原来的两倍.
▼优质解答
答案和解析
(1)①粉红色的PdCl2溶液可以检验空气中少量的CO.若空气中含CO,则溶液中会产生黑色的Pd沉淀.每生成5.3gPd沉淀,物质的量=
=0.05mol,依据PdCl2~Pd~2e-,转移电子数为0.05mol×2×NA=0.1NA,
故答案为:0.1NA ;
②测定一氧化碳气体含量,使一氧化碳发生氧化还原反应生成二氧化碳,原电池的负极是失电子发生氧化反应,酸性介质中负极电极反应为CO+H2O-2e-=CO2+2H+,
故答案为:CO+H2O-2e-=CO2+2H+;
(2)①平衡时c(NO)=
=0.02mol/L,c(N2)=c(CO2)=
=0.015mol/L,故T1℃时该反应的平衡常数为K1=
=
,
故答案为:
;
②由表中数据可知,温度由T1变为T2,平衡向逆反应移动,由于正反应是吸热,还是放热不确定,无法判断温度变化,
故选:c;
(3)根据图示信息得到:300℃之前,温度升高脱氮率逐渐增大;300℃之后,温度升高脱氮率逐渐减小,这是因为:300℃之前,反应未平衡,反应向右进行,脱氮率增大;300℃时反应达平衡,后升温平衡逆向移动,脱氮率减小,
故答案为:300℃之前,温度升高脱氮率逐渐增大,而300℃之后,温度升高脱氮率逐渐减小;300℃之前,反应未平衡,反应向右进行,脱氮率增大;300℃时反应达平衡,后升温平衡逆向移动,脱氮率减小.
(4)在某温度时,向10L的密闭容器中加入4.0mol SO2和10.0mol O2,反应达到平衡,改变下列条件,再次达到平衡时,能使O2的新平面浓度和原来平衡浓度相同,分析选项可知
A.在其他条件不变时,减少容器的容积,压强增大,平衡正向进行,体积减小氧气浓度增大,故A错误;
B.保持温度和容器内压强不变,再充入2.0mol SO2和5.0mol O2,为保持压强不变,体积增大,最后达到相同平衡状态,氧气浓度不变,故B正确;
C.保持温度和容器体积不变,温度不变平衡常数不变,K=
,再充入SO2和SO3,使之浓度扩大为原来的两倍,平衡常数不变,氧气浓度不变,故C正确;
故答案为:BC.
| 5.3mol |
| 106g/mol |
故答案为:0.1NA ;
②测定一氧化碳气体含量,使一氧化碳发生氧化还原反应生成二氧化碳,原电池的负极是失电子发生氧化反应,酸性介质中负极电极反应为CO+H2O-2e-=CO2+2H+,
故答案为:CO+H2O-2e-=CO2+2H+;
(2)①平衡时c(NO)=
| 0.04mol |
| 2L |
| 0.03mol |
| 2L |
| 0.015×0.015 |
| 0.022 |
| 9 |
| 16 |
故答案为:
| 9 |
| 16 |
②由表中数据可知,温度由T1变为T2,平衡向逆反应移动,由于正反应是吸热,还是放热不确定,无法判断温度变化,
故选:c;
(3)根据图示信息得到:300℃之前,温度升高脱氮率逐渐增大;300℃之后,温度升高脱氮率逐渐减小,这是因为:300℃之前,反应未平衡,反应向右进行,脱氮率增大;300℃时反应达平衡,后升温平衡逆向移动,脱氮率减小,
故答案为:300℃之前,温度升高脱氮率逐渐增大,而300℃之后,温度升高脱氮率逐渐减小;300℃之前,反应未平衡,反应向右进行,脱氮率增大;300℃时反应达平衡,后升温平衡逆向移动,脱氮率减小.
(4)在某温度时,向10L的密闭容器中加入4.0mol SO2和10.0mol O2,反应达到平衡,改变下列条件,再次达到平衡时,能使O2的新平面浓度和原来平衡浓度相同,分析选项可知
A.在其他条件不变时,减少容器的容积,压强增大,平衡正向进行,体积减小氧气浓度增大,故A错误;
B.保持温度和容器内压强不变,再充入2.0mol SO2和5.0mol O2,为保持压强不变,体积增大,最后达到相同平衡状态,氧气浓度不变,故B正确;
C.保持温度和容器体积不变,温度不变平衡常数不变,K=
| c2(SO3) |
| c2(SO2)c(O2) |
故答案为:BC.
看了 某城市实时空气质量检测报告中...的网友还看了以下:
已知:如图1,点P在⊙O外,PC是⊙O的切线、切点为C,直线PO与⊙O相交于点A、B.(1)试探求 2020-04-12 …
已知:如图1,点P在⊙O外,PC是⊙O的切线、切点为C,直线PO与⊙O相交于点A、B.(1)试探求 2020-04-12 …
已知:如图1,点P在⊙O外,PC是⊙O的切线、切点为C,直线PO与⊙O相交于点A、B.(1)试探求 2020-04-12 …
有机物A与B只由C、H、O中的2种或3种元素组成有机物A与B只由C,H,O中的2种或3种元素组成, 2020-05-16 …
镁条在空气中点燃,反应结束后生成物全部收回称量,为什么所称得的质量比反应前质量增加了?但是根据质量 2020-05-20 …
已知圆O经过坐标原点,且与直线x-y+2=0相切,切点为(2,4)①求圆O的方程,并指出圆心与半径 2020-06-14 …
这是同位素吗O=C=O(1个O质量数为161个O质量数为18)O=O=O(1个O质量数为161个O 2020-07-18 …
dS=nCln(T2/T1)S是熵n是物质的量C是摩尔比热容ln自然对数T温度上面这个式子是怎么推 2020-08-01 …
如图二次函数y等于负mx方+4m(m不等o)的图象的顶点坐标为(o,2)矩形ABcD的顶点B、cx 2020-08-01 …
一般情况下,在“比、占、是、相当于、等于”等等后的量就是什么 2020-11-08 …