早教吧作业答案频道 -->化学-->
在一堂化学实验课上,老师为每组同学分别提供了一瓶氢氧化钠溶液,让他们用1%的稀盐酸来测定其溶质的质量分数.以下是几组同学的设想及做法:(1)甲组同学的实验如图1所示:在烧杯
题目详情
在一堂化学实验课上,老师为每组同学分别提供了一瓶氢氧化钠溶液,让他们用1%的稀盐酸来测定其溶质的质量分数.以下是几组同学的设想及做法:
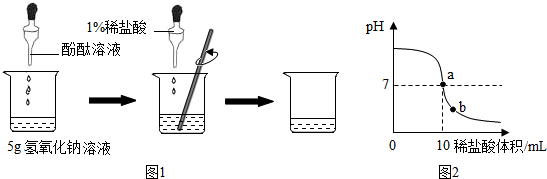
(1)甲组同学的实验如图1所示:在烧杯中加入5g氢氧化钠溶液,滴入几滴酚酞溶液,用滴管慢慢滴入1%的稀盐酸,并不断搅拌,至溶液颜色恰好变为无色为止.
请回答:①酚酞溶液的作用是___;②边滴加稀盐酸,边用玻璃棒不断搅拌的目的是___.
(2)乙组整个实验过程中溶液pH的变化阁象图象(简单表示为图2).请回答:
图2中a点表示的含义是___;b点溶液中含有的阳离子有___(填离子符号);乙组同学要计算出这瓶氢氧化钠溶液中溶质的质量分数,除了要用到已有数据外,你认为还需要的数据是___.
(3)丙组同学在滴加稀盐酸一段时间后,发现溶液中有少量气泡产生.这一“异常现象”激起了他们的探究欲望,通过实验证明:该组用的这瓶氢氧化钠溶液已经部分变质.请用化学方程式表示其变质的原因
___;若要除去溶液中变质生成的杂质,请简要写出你的实验方案:___.
(4)当甲组在5g氢氧化钠溶液中滴加稀盐酸,溶液顔色恰好变为无色时,共用去了稀盐酸7.3g.计算甲组这瓶氢氧化钠溶液中溶质的质量分数.

(1)甲组同学的实验如图1所示:在烧杯中加入5g氢氧化钠溶液,滴入几滴酚酞溶液,用滴管慢慢滴入1%的稀盐酸,并不断搅拌,至溶液颜色恰好变为无色为止.
请回答:①酚酞溶液的作用是___;②边滴加稀盐酸,边用玻璃棒不断搅拌的目的是___.
(2)乙组整个实验过程中溶液pH的变化阁象图象(简单表示为图2).请回答:
图2中a点表示的含义是___;b点溶液中含有的阳离子有___(填离子符号);乙组同学要计算出这瓶氢氧化钠溶液中溶质的质量分数,除了要用到已有数据外,你认为还需要的数据是___.
(3)丙组同学在滴加稀盐酸一段时间后,发现溶液中有少量气泡产生.这一“异常现象”激起了他们的探究欲望,通过实验证明:该组用的这瓶氢氧化钠溶液已经部分变质.请用化学方程式表示其变质的原因
___;若要除去溶液中变质生成的杂质,请简要写出你的实验方案:___.
(4)当甲组在5g氢氧化钠溶液中滴加稀盐酸,溶液顔色恰好变为无色时,共用去了稀盐酸7.3g.计算甲组这瓶氢氧化钠溶液中溶质的质量分数.
▼优质解答
答案和解析
(1)①酚酞溶液遇碱性溶液变红,酚酞溶液的作用是:判断反应是否恰好完成;
②在中和反应过程中,边滴加稀盐酸,边要用玻璃棒不断搅拌的目的是:使反应物充分接触,完全反应.
(2)由溶液pH的变化图象可知,在a点时,溶液的pH等于7,说明了氢氧化钠和盐酸恰好中和;在b点时,溶液呈酸性,氢氧化钠全部与盐酸反应生成了氯化钠,溶液中还有剩余的盐酸.所以溶液中的阳离子是:Na+、H+;要求氢氧化钠溶液的质量质量分数,须知盐酸的质量,由题中的条件可知,还需要的数据是稀盐酸的密度.
(3)氢氧化钠变质的原因是氢氧化钠与空气中的二氧化碳反应,反应的方程式是:CO2+2NaOH=Na2CO3+H2O.由于碳酸钠能与氢氧化钙反应生成了氢氧化钠和碳酸钙,既除去了杂质碳酸钠,又没有引入新的杂质.所以,要除去溶液中变质生成的杂质,实验方案是:加适量澄清石灰水,过滤.
(4)盐酸中溶质的质量为:7.3g×1%=0.073g
设氢氧化钠的质量为x
NaOH+HCl=NaCl+H2O
40 36.5
x 0.073g
=
解得:解得:x=0.08g
甲组这瓶氢氧化钠溶液中溶质的质量分数为:
×100%=1.6%.
故答为:(1)①判断反应是否恰好完成,②使反应物充分接触,完全反应;(2)完全反应恰好中和,Na+和H+,稀盐酸的密度;(3)CO2+2NaOH=Na2CO3+H2O,加适量澄清石灰水,过滤;(4)甲组这瓶氢氧化钠溶液中溶质的质量分数是1.6%.
②在中和反应过程中,边滴加稀盐酸,边要用玻璃棒不断搅拌的目的是:使反应物充分接触,完全反应.
(2)由溶液pH的变化图象可知,在a点时,溶液的pH等于7,说明了氢氧化钠和盐酸恰好中和;在b点时,溶液呈酸性,氢氧化钠全部与盐酸反应生成了氯化钠,溶液中还有剩余的盐酸.所以溶液中的阳离子是:Na+、H+;要求氢氧化钠溶液的质量质量分数,须知盐酸的质量,由题中的条件可知,还需要的数据是稀盐酸的密度.
(3)氢氧化钠变质的原因是氢氧化钠与空气中的二氧化碳反应,反应的方程式是:CO2+2NaOH=Na2CO3+H2O.由于碳酸钠能与氢氧化钙反应生成了氢氧化钠和碳酸钙,既除去了杂质碳酸钠,又没有引入新的杂质.所以,要除去溶液中变质生成的杂质,实验方案是:加适量澄清石灰水,过滤.
(4)盐酸中溶质的质量为:7.3g×1%=0.073g
设氢氧化钠的质量为x
NaOH+HCl=NaCl+H2O
40 36.5
x 0.073g
| 40 |
| 36.5 |
| x |
| 0.073g |
甲组这瓶氢氧化钠溶液中溶质的质量分数为:
| 0.08g |
| 5g |
故答为:(1)①判断反应是否恰好完成,②使反应物充分接触,完全反应;(2)完全反应恰好中和,Na+和H+,稀盐酸的密度;(3)CO2+2NaOH=Na2CO3+H2O,加适量澄清石灰水,过滤;(4)甲组这瓶氢氧化钠溶液中溶质的质量分数是1.6%.
看了 在一堂化学实验课上,老师为每...的网友还看了以下:
金属及其化合物变化多,用途广.请完成下列计算:(1)等物质的量的镁在氧气中充分灼烧,产物质量为ag 2020-04-11 …
三角函数与向量的题在△ABC中,角A的对边长等于2,向量M=(cosA/2+sinA/2,2)向量 2020-04-27 …
请详解化学上过量与少量的问题在网上看了一大堆以少量的为准的原则,我去.麻烦详细讲解怎样以少量为原则 2020-05-17 …
物理关于动量的题在足够长的斜面上有一质量为m的长方形木版A,木版上表面光滑.当木版获得初速度V0后 2020-05-21 …
有三道数学选择题(关于平面向量的)存在疑问,请大家详细解释一下1.已知|b向量|=3,a向量在b向 2020-06-06 …
金属及其化合物变化多,用途广。请完成下列计算:(1)等物质的量的镁在氧气中充分灼烧,产物质量为ag 2020-06-28 …
13.2g氮的氧化物(NxO)中氧原子物质的量为0.3mol,该质量的NxO在标况下的体积为L,x 2020-07-11 …
动量的题在线等1.质量为4kg的铅球和质量为0.1kg的皮球,以相同的速度运动,要使他们在相同的时间 2020-11-01 …
学霸们好。为什么大量的钡在容器内严格密封保,少量的钡却向容器内加煤油浸过钡并封口保存为什么钡的量 2020-11-04 …
一定质量的钠在一定条件下全部被氧化,测得产物中氧元素的含量为12/35,则参加反应的钠与氧气的物质的 2020-11-20 …