早教吧作业答案频道 -->化学-->
铅有+2和+4两种价态,铅的常见氧化物四氧化三铅(Pb2O4)和二氧化铅(PbO2)均常用于蓄电池中,回答下列问题:(l)已知镁橄榄石(Mg2SiO4)可表示为2MgO.SiO2,则Pb3O4可表示为.(2)工
题目详情
铅有+2和+4两种价态,铅的常见氧化物四氧化三铅(Pb2O4)和二氧化铅(PbO2)均常用于蓄电池中,回答下列问题:
(l)已知镁橄榄石(Mg2SiO4)可表示为2MgO.SiO2,则Pb3O4可表示为___.
(2)工业采用熔铅氧化法制取四氧化三铅,其反应为6PbO+O2═2Pb3O4,每生成1mol Pb3O4转移电子的物质的量为___;产物中含有的氧化铅杂质可用氢氧化钾溶液提纯,生成可溶性的钾盐{K[Pb(OH)3]},该反应的离子方程式为___.
(3)在Pb(NO3)2溶液中,加入(NH4)2S2O8溶液和氨水可制备PbO2,恰好完全反应后的溶液中,各离子浓度的大小顺序为___.
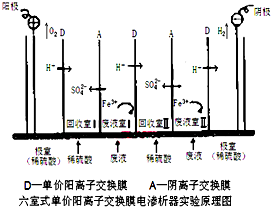
(4)铅蓄电池中的废液可用双膜电渗析法进行处理再生.
①电渗析后,回收室的产品是___.
②电渗析过程中,阳极的电极反应式为___.
(5)已知在硝酸溶液中,二氧化铅可氧化过氧化氢,今取二氧化铅样品(杂质不与过氧化氢反应)0.6000g于锥形瓶中,加入15.00mL稀硝酸和10mL0.3000mol/LH2O2溶液,使试样完全溶解,然后用0.02000mol/L的酸性KMnO4溶液滴定,消耗酸性KMnO4,标准溶液15.00mL.
①用酸性KMnO4溶液滴定时,确定反应达到滴定终点的现象是___.
②二氧化铅的质量分数为___.
(l)已知镁橄榄石(Mg2SiO4)可表示为2MgO.SiO2,则Pb3O4可表示为___.
(2)工业采用熔铅氧化法制取四氧化三铅,其反应为6PbO+O2═2Pb3O4,每生成1mol Pb3O4转移电子的物质的量为___;产物中含有的氧化铅杂质可用氢氧化钾溶液提纯,生成可溶性的钾盐{K[Pb(OH)3]},该反应的离子方程式为___.
(3)在Pb(NO3)2溶液中,加入(NH4)2S2O8溶液和氨水可制备PbO2,恰好完全反应后的溶液中,各离子浓度的大小顺序为___.
(4)铅蓄电池中的废液可用双膜电渗析法进行处理再生.
①电渗析后,回收室的产品是___.
②电渗析过程中,阳极的电极反应式为___.
(5)已知在硝酸溶液中,二氧化铅可氧化过氧化氢,今取二氧化铅样品(杂质不与过氧化氢反应)0.6000g于锥形瓶中,加入15.00mL稀硝酸和10mL0.3000mol/LH2O2溶液,使试样完全溶解,然后用0.02000mol/L的酸性KMnO4溶液滴定,消耗酸性KMnO4,标准溶液15.00mL.
①用酸性KMnO4溶液滴定时,确定反应达到滴定终点的现象是___.
②二氧化铅的质量分数为___.

▼优质解答
答案和解析
(1)由已知可知,按照金属氧化物、非金属氧化物顺序书写,并遵循原子守恒,Pb有+2、+4价,则Pb3O4可表示为2PbO.PbO2,故答案为:2PbO.PbO2;
(2)由6PbO+O2═2Pb3O4,可知O元素的化合价降低,每生成1mol Pb3O4,0.5mol氧气作氧化剂,转移电子的物质的量为0.5mol×2×(2-0)=2mol;氧化铅杂质可用氢氧化钾溶液提纯,生成可溶性的钾盐{K[Pb(OH)3]},离子反应为PbO+OH-+H2O=[Pb(OH)3]-,
故答案为:2mol;PbO+OH-+H2O=[Pb(OH)3]-;
(3)由电子守恒可知发生Pb(NO3)2+(NH4)2S2O8+4NH3.H2O→PbO2+2(NH4)2SO4+2NH4NO3,+2H2O,恰好完全反应后的溶液存在等量的(NH4)2SO4、NH4NO3,铵根离子浓度最大,且铵根离子水解显酸性,离子浓度大小为c(NH4+)>c(NO3-)=c(SO42-)>c(H+)>c(OH-),
故答案为:c(NH4+)>c(NO3-)=c(SO42-)>c(H+)>c(OH-);
(4)①由图可知,回收室中左侧进入氢离子,右侧进入硫酸根离子,则回收室的产品是硫酸,故答案为:硫酸;
②电渗析过程中,阳极上水失去电子生成氧气,电极反应为2H2O-4e-=4H++O2↑,故答案为:2H2O-4e-=4H++O2↑;
(5)①用酸性KMnO4溶液滴定时,确定反应达到滴定终点的现象是滴入最后一滴酸性高锰酸钾溶液呈淡紫红色,且半分钟内不褪色,
故答案为:滴入最后一滴酸性高锰酸钾溶液呈淡紫红色,且半分钟内不褪色;
②0.02000mol/L的酸性KMnO4溶液滴定,消耗酸性KMnO4标准溶液15.00mL,由2MnO4-+5H2O2+6H+═2Mn2++8H2O+5O2↑可知,则参与该反应的双氧水为0.02000×15.00×10-3×
=0.75×10-3mol,所以被二氧化铅氧化的双氧水为0.3000×10×10-3-0.75×10-3=2.25×10-3mol,再由PbO2+H2O2+2H+═Pb2++2H2O+O2↑,则二氧化铅的物质的量为2.25×10-3mol,所以二氧化铅的质量分数为
×100%=89.63%,
故答案为:89.63%.
(2)由6PbO+O2═2Pb3O4,可知O元素的化合价降低,每生成1mol Pb3O4,0.5mol氧气作氧化剂,转移电子的物质的量为0.5mol×2×(2-0)=2mol;氧化铅杂质可用氢氧化钾溶液提纯,生成可溶性的钾盐{K[Pb(OH)3]},离子反应为PbO+OH-+H2O=[Pb(OH)3]-,
故答案为:2mol;PbO+OH-+H2O=[Pb(OH)3]-;
(3)由电子守恒可知发生Pb(NO3)2+(NH4)2S2O8+4NH3.H2O→PbO2+2(NH4)2SO4+2NH4NO3,+2H2O,恰好完全反应后的溶液存在等量的(NH4)2SO4、NH4NO3,铵根离子浓度最大,且铵根离子水解显酸性,离子浓度大小为c(NH4+)>c(NO3-)=c(SO42-)>c(H+)>c(OH-),
故答案为:c(NH4+)>c(NO3-)=c(SO42-)>c(H+)>c(OH-);
(4)①由图可知,回收室中左侧进入氢离子,右侧进入硫酸根离子,则回收室的产品是硫酸,故答案为:硫酸;
②电渗析过程中,阳极上水失去电子生成氧气,电极反应为2H2O-4e-=4H++O2↑,故答案为:2H2O-4e-=4H++O2↑;
(5)①用酸性KMnO4溶液滴定时,确定反应达到滴定终点的现象是滴入最后一滴酸性高锰酸钾溶液呈淡紫红色,且半分钟内不褪色,
故答案为:滴入最后一滴酸性高锰酸钾溶液呈淡紫红色,且半分钟内不褪色;
②0.02000mol/L的酸性KMnO4溶液滴定,消耗酸性KMnO4标准溶液15.00mL,由2MnO4-+5H2O2+6H+═2Mn2++8H2O+5O2↑可知,则参与该反应的双氧水为0.02000×15.00×10-3×
| 5 |
| 2 |
| 2.25×10-3mol×239g/mol |
| 0.6000g |
故答案为:89.63%.
看了 铅有+2和+4两种价态,铅的...的网友还看了以下:
有一种合金的密度是11×10^3(10的3次方)千克/立方米.它是由下表中某两种金属组成的,根据密 2020-04-11 …
学校有一种铅球外面是铁,里面是铅.问:一个体积为500立方厘米,质量为4KG的铅球,含多少铁和铅? 2020-05-14 …
(2013•历下区二模)铅蓄电池是一种化学电源,它的正负极分别是浸在稀硫酸中的未知物质X和铅(Pb 2020-06-15 …
用十元钱可以买一个文具盒和两支铅笔,如果只买一个文具盒和一支铅笔一,还剩下伍角.一个文具盒多少钱? 2020-06-20 …
体积和质量相等的铁球、铜球和铅球,已知p铁小于p铜小于p铅p代表密度A.如果铁球是实心的,则铜球和 2020-06-30 …
钍核经过6次α衰变和4次β衰变后变成铅核,则[]A.铅核的符号为,它比少8个中子B.铅核的符号为, 2020-07-08 …
把一块铅和一块金的接触面磨平磨光后紧紧压在一起,若干年后发现金中有铅,铅中有金.对此现象说法正确的是 2020-11-01 …
商店有水彩笔和铅笔一共163支,如果水彩笔拿走19支后,水彩笔的支数就正好是铅笔的5倍.原有水彩笔支 2020-12-08 …
画笔和铅笔一共5盒,共72枝.一盒画笔比一盒铅笔多6枝,如果5盒都是画笔,一共有枝画笔,如果5盒都是 2020-12-09 …
五角和一元的硬币共有37枚,币值28元.一元的硬币比五角的硬币多多少枚?小明买2本笔记本和12支铅笔 2020-12-31 …