早教吧作业答案频道 -->化学-->
(1)一个国家乙烯工业的发展水平,已成为衡量这个国家石油化学工业水平的重要标志之一.请列举出乙烯的两种重要用途:①,②;(2)实验室可用如图所示装置制取乙烯,A中加入
题目详情
(1)一个国家乙烯工业的发展水平,已成为衡量这个国家石油化学工业水平的重要标志之一.请列举出乙烯的两种重要用途:①___,②___;
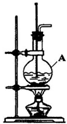
(2)实验室可用如图所示装置制取乙烯,A中加入的两种试剂是___,它们的体积比约为___.反应方程式为___;乙烯的收集方法为___;
(3)将反应产生的乙烯通入酸性高锰酸钾溶液中,观察到的现象是___;将反应产生的乙烯通入溴的四氯化碳溶液中,观察到的现象是___;
(4)反应进行一段时间后,A中混合液常变黑,并有刺激性气味的气体生成,它对乙烯性质的检验有干扰;请设计实验验证该气体的存在,并最后排除该气体对乙烯性质的干扰.(只要求画出装置图和标明各仪器中的药品,并标明气流的方向)
 (1)一个国家乙烯工业的发展水平,已成为衡量这个国家石油化学工业水平的重要标志之一.请列举出乙烯的两种重要用途:①___,②___;
(1)一个国家乙烯工业的发展水平,已成为衡量这个国家石油化学工业水平的重要标志之一.请列举出乙烯的两种重要用途:①___,②___;
(2)实验室可用如图所示装置制取乙烯,A中加入的两种试剂是___,它们的体积比约为___.反应方程式为___;乙烯的收集方法为___;
(3)将反应产生的乙烯通入酸性高锰酸钾溶液中,观察到的现象是___;将反应产生的乙烯通入溴的四氯化碳溶液中,观察到的现象是___;
(4)反应进行一段时间后,A中混合液常变黑,并有刺激性气味的气体生成,它对乙烯性质的检验有干扰;请设计实验验证该气体的存在,并最后排除该气体对乙烯性质的干扰.(只要求画出装置图和标明各仪器中的药品,并标明气流的方向)


(2)实验室可用如图所示装置制取乙烯,A中加入的两种试剂是___,它们的体积比约为___.反应方程式为___;乙烯的收集方法为___;
(3)将反应产生的乙烯通入酸性高锰酸钾溶液中,观察到的现象是___;将反应产生的乙烯通入溴的四氯化碳溶液中,观察到的现象是___;
(4)反应进行一段时间后,A中混合液常变黑,并有刺激性气味的气体生成,它对乙烯性质的检验有干扰;请设计实验验证该气体的存在,并最后排除该气体对乙烯性质的干扰.(只要求画出装置图和标明各仪器中的药品,并标明气流的方向)
 (1)一个国家乙烯工业的发展水平,已成为衡量这个国家石油化学工业水平的重要标志之一.请列举出乙烯的两种重要用途:①___,②___;
(1)一个国家乙烯工业的发展水平,已成为衡量这个国家石油化学工业水平的重要标志之一.请列举出乙烯的两种重要用途:①___,②___;(2)实验室可用如图所示装置制取乙烯,A中加入的两种试剂是___,它们的体积比约为___.反应方程式为___;乙烯的收集方法为___;
(3)将反应产生的乙烯通入酸性高锰酸钾溶液中,观察到的现象是___;将反应产生的乙烯通入溴的四氯化碳溶液中,观察到的现象是___;
(4)反应进行一段时间后,A中混合液常变黑,并有刺激性气味的气体生成,它对乙烯性质的检验有干扰;请设计实验验证该气体的存在,并最后排除该气体对乙烯性质的干扰.(只要求画出装置图和标明各仪器中的药品,并标明气流的方向)


▼优质解答
答案和解析
(1)乙烯是一种植物生长调节剂;乙烯能够聚合生成聚乙烯;
故答案为:①生产聚乙烯,②果实催熟;
(2)乙烯在浓硫酸做催化剂、脱水剂条件下,加热到170度发生消去反应生成乙烯,化学方程式:CH33CH22OH
CH2=CH2↑+H2O;浓硫酸与乙醇体积比为:3:1;乙烯密度与空气密度相差不大,难溶于水,应选择排水法收集;
故答案为:浓硫酸和乙醇;3:1;CH3CH2OH
CH2=CH2↑+H2O;排水集气法;
(3)乙烯含有碳碳双键具有还原性,能够被酸性高锰酸钾氧化使高锰酸钾褪色;
能够与溴发生加成反应,使溴的四氯化碳褪色;
故答案为:紫色高锰酸钾溶液褪色; 溴的四氯碳溶液褪色;
(4)依据题意可知生成的乙烯中含有二氧化硫,二氧化硫为酸性气体,可与碱反应,可使品红褪色,具有还原性,可与酸性高锰酸钾发生氧化还原反应,而乙烯含有碳碳双键可与酸性高锰酸钾发生氧化还原反应,所以应先用品红溶液检验二氧化硫的存在,然后用氢氧化钠溶液吸收二氧化硫,再通过品红溶液检验二氧化硫是否被除尽,最后通入酸性的高锰酸钾溶液,观察是否褪色,装置图为:
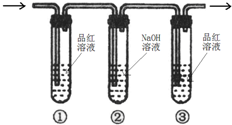 ;
;
故答案为: .
.
浓硫酸 170℃ 浓硫酸 浓硫酸 浓硫酸170℃ 170℃ 170℃CH22=CH22↑+H22O;浓硫酸与乙醇体积比为:3:1;乙烯密度与空气密度相差不大,难溶于水,应选择排水法收集;
故答案为:浓硫酸和乙醇;3:1;CH33CH22OH
CH2=CH2↑+H2O;排水集气法;
(3)乙烯含有碳碳双键具有还原性,能够被酸性高锰酸钾氧化使高锰酸钾褪色;
能够与溴发生加成反应,使溴的四氯化碳褪色;
故答案为:紫色高锰酸钾溶液褪色; 溴的四氯碳溶液褪色;
(4)依据题意可知生成的乙烯中含有二氧化硫,二氧化硫为酸性气体,可与碱反应,可使品红褪色,具有还原性,可与酸性高锰酸钾发生氧化还原反应,而乙烯含有碳碳双键可与酸性高锰酸钾发生氧化还原反应,所以应先用品红溶液检验二氧化硫的存在,然后用氢氧化钠溶液吸收二氧化硫,再通过品红溶液检验二氧化硫是否被除尽,最后通入酸性的高锰酸钾溶液,观察是否褪色,装置图为:
 ;
;
故答案为: .
.
浓硫酸 170℃ 浓硫酸 浓硫酸 浓硫酸170℃ 170℃ 170℃CH22=CH22↑+H22O;排水集气法;
(3)乙烯含有碳碳双键具有还原性,能够被酸性高锰酸钾氧化使高锰酸钾褪色;
能够与溴发生加成反应,使溴的四氯化碳褪色;
故答案为:紫色高锰酸钾溶液褪色; 溴的四氯碳溶液褪色;
(4)依据题意可知生成的乙烯中含有二氧化硫,二氧化硫为酸性气体,可与碱反应,可使品红褪色,具有还原性,可与酸性高锰酸钾发生氧化还原反应,而乙烯含有碳碳双键可与酸性高锰酸钾发生氧化还原反应,所以应先用品红溶液检验二氧化硫的存在,然后用氢氧化钠溶液吸收二氧化硫,再通过品红溶液检验二氧化硫是否被除尽,最后通入酸性的高锰酸钾溶液,观察是否褪色,装置图为:
 ;
;
故答案为: .
.
故答案为:①生产聚乙烯,②果实催熟;
(2)乙烯在浓硫酸做催化剂、脱水剂条件下,加热到170度发生消去反应生成乙烯,化学方程式:CH33CH22OH
| 浓硫酸 |
| 170℃ |
故答案为:浓硫酸和乙醇;3:1;CH3CH2OH
| 浓硫酸 |
| 170℃ |
(3)乙烯含有碳碳双键具有还原性,能够被酸性高锰酸钾氧化使高锰酸钾褪色;
能够与溴发生加成反应,使溴的四氯化碳褪色;
故答案为:紫色高锰酸钾溶液褪色; 溴的四氯碳溶液褪色;
(4)依据题意可知生成的乙烯中含有二氧化硫,二氧化硫为酸性气体,可与碱反应,可使品红褪色,具有还原性,可与酸性高锰酸钾发生氧化还原反应,而乙烯含有碳碳双键可与酸性高锰酸钾发生氧化还原反应,所以应先用品红溶液检验二氧化硫的存在,然后用氢氧化钠溶液吸收二氧化硫,再通过品红溶液检验二氧化硫是否被除尽,最后通入酸性的高锰酸钾溶液,观察是否褪色,装置图为:
 ;
;故答案为:
 .
. | 浓硫酸 |
| 170℃ |
故答案为:浓硫酸和乙醇;3:1;CH33CH22OH
| 浓硫酸 |
| 170℃ |
(3)乙烯含有碳碳双键具有还原性,能够被酸性高锰酸钾氧化使高锰酸钾褪色;
能够与溴发生加成反应,使溴的四氯化碳褪色;
故答案为:紫色高锰酸钾溶液褪色; 溴的四氯碳溶液褪色;
(4)依据题意可知生成的乙烯中含有二氧化硫,二氧化硫为酸性气体,可与碱反应,可使品红褪色,具有还原性,可与酸性高锰酸钾发生氧化还原反应,而乙烯含有碳碳双键可与酸性高锰酸钾发生氧化还原反应,所以应先用品红溶液检验二氧化硫的存在,然后用氢氧化钠溶液吸收二氧化硫,再通过品红溶液检验二氧化硫是否被除尽,最后通入酸性的高锰酸钾溶液,观察是否褪色,装置图为:
 ;
;故答案为:
 .
. | 浓硫酸 |
| 170℃ |
(3)乙烯含有碳碳双键具有还原性,能够被酸性高锰酸钾氧化使高锰酸钾褪色;
能够与溴发生加成反应,使溴的四氯化碳褪色;
故答案为:紫色高锰酸钾溶液褪色; 溴的四氯碳溶液褪色;
(4)依据题意可知生成的乙烯中含有二氧化硫,二氧化硫为酸性气体,可与碱反应,可使品红褪色,具有还原性,可与酸性高锰酸钾发生氧化还原反应,而乙烯含有碳碳双键可与酸性高锰酸钾发生氧化还原反应,所以应先用品红溶液检验二氧化硫的存在,然后用氢氧化钠溶液吸收二氧化硫,再通过品红溶液检验二氧化硫是否被除尽,最后通入酸性的高锰酸钾溶液,观察是否褪色,装置图为:
 ;
;故答案为:
 .
.
看了 (1)一个国家乙烯工业的发展...的网友还看了以下:
下列各组中两个变化所发生的反应,属于同一类型的是()①由甲苯制甲基环己烷、由乙烷制溴乙烷②乙烯使溴水 2020-03-30 …
实验室制乙烯制取乙烯的时候,那些实验现象说明发生了副反应?试讨论可能产生的副产物. 2020-04-08 …
写出下列反应并指明反应类型(有机物用结构简式表示)①由乙烯制乙醇②实验室制甲烷③乙烯使溴水褪色④由 2020-04-08 …
(1)某有机物的结构简式为HOOC-CH2=CHOH请你写出该有机物官能团的名称:(2)完成下列反 2020-05-04 …
下列有机反应类型的归属正确的是()①乙烷与Cl2反应制氯乙烷②丙烯与Cl2反应制3-氯-1-丙烯③ 2020-05-13 …
下列各组中两个变化所发生的反应,属于同一类型的是()①由乙烯制取乙烷,由乙烷制溴乙烷;②乙烯使溴水 2020-07-29 …
下列反应中有机物被氧化的是()A.乙烯使溴水褪色B.乙醇使高锰酸钾溶液褪色C.乙烯制聚乙烯D.乙醛 2020-07-29 …
(1)下列反应:①由乙烯制氯乙烷②氯乙烷在氢氧化钠的醇溶液中加热反应③乙醇发生分子间脱水生成乙醚④乙 2020-11-29 …
在一定条件下,乙烷和乙烯都能制备氯乙烷.(1)乙烷制氯乙烷的化学方程式是CH3CH3+Cl2光照CH 2020-11-29 …
用数字编号填空:在下述反应中,属于取代反应的是;属于氧化反应的是;属于加成反应的是.①由乙烯制氯乙烷 2020-11-29 …