早教吧作业答案频道 -->化学-->
稀硝酸和铜反应的化学方程式如下:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O(1)指出该氧化还原反应的氧化剂和还原剂,并用双线桥法表示出电子转移的方向和数目(在上面方程式中标出).(2)若生
题目详情
稀硝酸和铜反应的化学方程式如下:3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O
(1)指出该氧化还原反应的氧化剂和还原剂,并用双线桥法表示出电子转移的方向和数目(在上面方程式中标出).
(2)若生成标准状况下11.2LNO气体,计算参加反应的铜的质量以及反应中被还原的HNO3的物质的量.
(1)指出该氧化还原反应的氧化剂和还原剂,并用双线桥法表示出电子转移的方向和数目(在上面方程式中标出).
(2)若生成标准状况下11.2LNO气体,计算参加反应的铜的质量以及反应中被还原的HNO3的物质的量.
▼优质解答
答案和解析
(1)在反应3Cu+8HNO3=3Cu(NO3)2+2NO↑+4H2O中,Cu元素的化合价由0升高到+2价,Cu为还原剂,N元素的化合价由+5降低为+2价,硝酸为氧化剂,转移的电子为6e-,则双线桥法标出电子得失的方向和数目为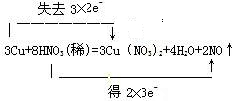 ,
,
答:氧化剂为硝酸,还原剂为Cu,双线桥法表示出电子转移的方向和数目为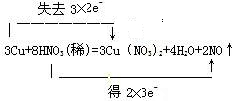 ;
;
(2)生成标准状况下11.2LNO气体,n(NO)=
=0.5mol,由电子守恒可知参加反应的铜的质量为
×64g/mol=48g,
由原子守恒可知被还原的HNO3的物质的量为0.5mol,
答:参加反应的铜的质量为48g,反应中被还原的HNO3的物质的量为0.5mol.
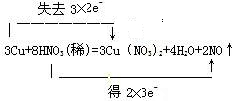 ,
,答:氧化剂为硝酸,还原剂为Cu,双线桥法表示出电子转移的方向和数目为
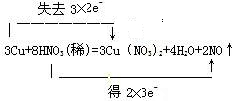 ;
;(2)生成标准状况下11.2LNO气体,n(NO)=
| 11.2L |
| 22.4L/mol |
| 0.5mol×(5-2) |
| (2-0) |
由原子守恒可知被还原的HNO3的物质的量为0.5mol,
答:参加反应的铜的质量为48g,反应中被还原的HNO3的物质的量为0.5mol.
看了稀硝酸和铜反应的化学方程式如下...的网友还看了以下:
铁与氧反应,如何生成四氧化三铁,如何生成三氧化二铁,如何生成氧化铁在线等啊2分钟一看是氧化亚铁,不 2020-04-06 …
下图所示是某种液态物质在冷却过程中温度随时间变化的曲线,图中bc段表示物质处在过程(填物态变化名称 2020-04-13 …
【高中化学在线等答案】某物质有醛基有碳碳双键,在用银氨溶液氧化醛基后,若没有调PH至中性,就直接加 2020-05-12 …
如图表示某植物幼根以葡萄糖为底物的细胞呼吸过程中O2的吸收量和CO2的释放量随环境中O2浓度的变化 2020-05-14 …
下图为我国长江三角洲地区某城市人口密度、土地价格、交通通达度、夏季平均气温变化图,其中表示夏季平均 2020-05-15 …
图1是甲、乙两种植物单位时间内吸收与释放CO2的量随光照强度变化的曲线.图2是甲植物在不同CO2浓 2020-05-15 …
如图是油菜种子在萌发成幼苗的过程中,根据其干重和鲜重的变化而绘制的两条曲线(X和Y),请分析回答: 2020-05-15 …
切线和法线问题?求圆的x平方-6x+y平方=3在点(1,2更号2)处的切线和法线方程.切线方程是x 2020-05-16 …
十进制数9用八进制数来表示是多少.又是怎么化的.在线等 2020-05-22 …
有1.3丁二烯和氢气,丙炔,总体体积为5升其中氢气和丙炔在混合气体中的体积分别为X和Y反应后体积为 2020-05-24 …