早教吧作业答案频道 -->化学-->
以氯化钾和硫酸亚铁为原料生产硫酸钾和氧化铁红颜料,其主要流程如下:已知:NH4HCO3溶液呈碱性,30℃以上NH4HCO3大量分解.(1)NH4HCO3溶液呈碱性的原因是.(2)写出沉淀池Ⅰ中反应的
题目详情
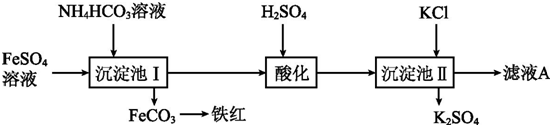
以氯化钾和硫酸亚铁为原料生产硫酸钾和氧化铁红颜料,其主要流程如下:已知:NH4HCO3溶液呈碱性,30℃以上NH4HCO3大量分解.
(1)NH4HCO3溶液呈碱性的原因是___.
(2)写出沉淀池Ⅰ中反应的化学方程式___,该反应必须控制的反应条件是___.
(3)煅烧FeCO3制铁红的方程式___,写出用K3[Fe(CN)6]溶液检验沉淀池Ⅰ中Fe2+沉淀是否完全的离子方程式:___.
(4)酸化的目的是___,反应的离子方程式为___.
(5)N、P、K、S都是植物生长所需的重要元素.滤液A可做复合肥料,因为其中含有___等元素.

(1)NH4HCO3溶液呈碱性的原因是___.
(2)写出沉淀池Ⅰ中反应的化学方程式___,该反应必须控制的反应条件是___.
(3)煅烧FeCO3制铁红的方程式___,写出用K3[Fe(CN)6]溶液检验沉淀池Ⅰ中Fe2+沉淀是否完全的离子方程式:___.
(4)酸化的目的是___,反应的离子方程式为___.
(5)N、P、K、S都是植物生长所需的重要元素.滤液A可做复合肥料,因为其中含有___等元素.
▼优质解答
答案和解析
(1)NH4HCO3为弱酸弱碱盐,NH4HCO3溶液中铵根离子水解显示酸性,碳酸氢根离子水解显示碱性,NH4+的水解程度小于HCO3-的水解程度,所以NH4HCO3溶液呈碱性,
故答案为:NH4+的水解程度小于HCO3-的水解程度;
(2)碳酸氢根离子和亚铁离子之间发生双水解反应生成碳酸亚铁沉淀,并放出二氧化碳,反应的原理方程式为:2NH4HCO3+FeSO4=FeCO3↓+(NH4 )2SO4+CO2↑+H2O,为防止较高温度下碳酸氢铵的分解(30℃以上NH4HCO3大量分解),要注意温度的选择,反应温度低于30℃,
故答案为:2NH4HCO3+FeSO4=FeCO3↓+(NH4 )2SO4+CO2↑+H2O;反应温度低于30℃;
(3)在空气中煅烧FeCO3生成氧化铁和二氧化碳,亚铁被氧化,方程式为4FeCO3+O2
2Fe2O3+4CO2,沉淀池Ⅰ中Fe2+未沉淀完全,用K3[Fe(CN)6]溶液检验,生成特征蓝色沉淀,反应的离子反应方程式为:3Fe2++2[Fe(CN)6]3-═Fe3[Fe(CN)6]2↓,
故答案为:4FeCO3+O2
2Fe2O3+4CO2;3Fe2++2[Fe(CN)6]3-═Fe3[Fe(CN)6]2↓;
(4)沉淀池Ⅰ中,除了生成的碳酸亚铁之外,溶液汇总会含有过量的碳酸氢铵,加入酸,酸化的目的是除去溶液中的HCO3-,反应为:H++HCO3-=H2O+CO2↑;,
故答案为:除去溶液中的HCO3-;H++HCO3-=H2O+CO2↑;
(5)滤液A的成分中含有(NH4 )2SO4以及KCl,即其中含有N、S、K元素,属于复合肥料,
故答案为:N、S、K.
故答案为:NH4+的水解程度小于HCO3-的水解程度;
(2)碳酸氢根离子和亚铁离子之间发生双水解反应生成碳酸亚铁沉淀,并放出二氧化碳,反应的原理方程式为:2NH4HCO3+FeSO4=FeCO3↓+(NH4 )2SO4+CO2↑+H2O,为防止较高温度下碳酸氢铵的分解(30℃以上NH4HCO3大量分解),要注意温度的选择,反应温度低于30℃,
故答案为:2NH4HCO3+FeSO4=FeCO3↓+(NH4 )2SO4+CO2↑+H2O;反应温度低于30℃;
(3)在空气中煅烧FeCO3生成氧化铁和二氧化碳,亚铁被氧化,方程式为4FeCO3+O2
| ||
故答案为:4FeCO3+O2
| ||
(4)沉淀池Ⅰ中,除了生成的碳酸亚铁之外,溶液汇总会含有过量的碳酸氢铵,加入酸,酸化的目的是除去溶液中的HCO3-,反应为:H++HCO3-=H2O+CO2↑;,
故答案为:除去溶液中的HCO3-;H++HCO3-=H2O+CO2↑;
(5)滤液A的成分中含有(NH4 )2SO4以及KCl,即其中含有N、S、K元素,属于复合肥料,
故答案为:N、S、K.
看了以氯化钾和硫酸亚铁为原料生产硫...的网友还看了以下:
数列{an}各项是1或3,且在第k个1和第k+1个1之间有2k-1个3,即1,3,1,3,3,3, 2020-05-16 …
1+2+3+n=2分之1n(n+1),n是正整数,研究1*2+2*3+你(n+1),观察1*2=3 2020-05-20 …
在曲面z=(x^2+y^2)^1/2上找一点使其与点(1,2^1/2,3*3^1/2)的距离最短我 2020-06-15 …
简便计算1÷(2÷3)÷(3÷4)÷(4÷5)(12.3+23.41+34.12+41.23)简便 2020-07-18 …
Tn=3×3+5×3^2+7×3^3+.+(2n-1)×3^n-1+(2n+1)×3^n(3^2表 2020-07-29 …
(5)设集合{1,2,3},下列关系R中不是等价关系的是().A.R={(1,1),(2,2),( 2020-08-02 …
1+2+3+4+5+.+n=0.5n^2+n1^2+2^2+3^2.+n^2=n(n+1)(2n+ 2020-08-03 …
求助JS二维数组从N个项取M个进行排列的组合算法函数如数组:arr1=[[1,2,3],[3,6], 2020-11-18 …
能简则简.(1)3/4+3/4÷3(2)1/3÷1/2-5/4x2/5(3)4/9÷[5/9-能简则 2020-11-26 …
观察下列等式:1/1*2=1-1/2,1/2*3=1/2-1/3,1/3*4=1/3-1/4.在线等 2020-12-05 …