早教吧作业答案频道 -->化学-->
某兴趣小组探究SO2气体还原Fe3+、I2,他们使用的药品和装置如图所示:(1)SO2气体还原Fe3+反应的产物是、(填离子符号).(2)下列实验方案可以用于在实验室制取所需SO2的是.A
题目详情
某兴趣小组探究SO2气体还原Fe3+、I2,他们使用的药品和装置如图所示:
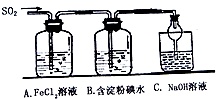
(1)SO2气体还原Fe3+反应的产物是___、___(填离子符号).
(2)下列实验方案可以用于在实验室制取所需SO2的是___.
A.Na2SO3溶液与HNO3 B.Na2SO3固体与70%浓硫酸
C.固体硫在纯氧中燃烧 D.铜与浓H2SO4共热
(3)装置C的作用是___.
(4)在上述装置中通入过量的SO2,为了验证A中SO2与Fe3+发生了氧化还原反应,他们取A中的溶液,分成三份,并设计了如下实验:
方案①:往第一份试液中加入KMnO4溶液,紫红色褪去.
方案②:往第一份试液加入KSCN溶液,不变红,再加入新制的氯水,溶液变红.
方案③:往第三份试液加入用稀盐酸酸化的BaCl2,产生白色沉淀.
上述方案不合理的是___,原因是___.
(5)能表明I-的还原性弱于SO2的现象是___,写出有关离子方程式:___.

(1)SO2气体还原Fe3+反应的产物是___、___(填离子符号).
(2)下列实验方案可以用于在实验室制取所需SO2的是___.
A.Na2SO3溶液与HNO3 B.Na2SO3固体与70%浓硫酸
C.固体硫在纯氧中燃烧 D.铜与浓H2SO4共热
(3)装置C的作用是___.
(4)在上述装置中通入过量的SO2,为了验证A中SO2与Fe3+发生了氧化还原反应,他们取A中的溶液,分成三份,并设计了如下实验:
方案①:往第一份试液中加入KMnO4溶液,紫红色褪去.
方案②:往第一份试液加入KSCN溶液,不变红,再加入新制的氯水,溶液变红.
方案③:往第三份试液加入用稀盐酸酸化的BaCl2,产生白色沉淀.
上述方案不合理的是___,原因是___.
(5)能表明I-的还原性弱于SO2的现象是___,写出有关离子方程式:___.
▼优质解答
答案和解析
(1)二氧化硫与铁离子反应的离子方程式为2Fe3++SO2+2H2O=2Fe2++SO42-+4H+,反应中铁离子被氧化成亚铁离子,所以还原产物为亚铁离子;氧化产物是SO42-,SO2气体还原Fe3+反应的产物是Fe2+、SO42-,故答案为:Fe2+;SO42-;
(2)A.硝酸具有强氧化性,能够将亚硫酸钠氧化成硫酸钠,无法得到二氧化硫气体,故A错误;
B.浓硫酸虽具有强酸性,且浓硫酸不挥发,亚硫酸钠溶液与浓硫酸能够反应生成二氧化硫气体,故B正确;
C.固体硫在纯氧中燃烧,操作不容易控制,且无法获得纯净的二氧化硫,故C错误;
D.Cu与浓硫酸在加热条件下生成二氧化硫、硫酸铜和水,可知制备二氧化硫,故D正确;
故答案为:BD;
(3)二氧化硫气体是酸性氧化物,具有刺激性气味,直接排放会污染大气,由于二氧化硫能和碱反应生成盐和水,可用碱液处理二氧化硫,所以装置C的作用为:吸收SO2尾气,防止污染空气,
故答案为:除去多余的SO2,防止污染大气;
(4)二氧化硫有还原性,高锰酸钾有强氧化性,二氧化硫能与高锰酸钾发生氧化还原反应使高锰酸钾溶液褪色,Fe2+也使高锰酸钾溶液褪色,所以方案①不合理,
故答案为:方案①;因为A的溶液中含有SO2,SO2也能使KMnO4溶液褪色;
(5)二氧化硫能使含有碘的淀粉溶液褪色,说明发生了氧化还原反应,碘是氧化剂,二氧化硫是还原剂,还原剂的还原性大于还原产物的还原性,其反应的离子方程式为:I2+SO2+2H2O=4H++2I-+SO42-;
故答案为:装置B中溶液蓝色褪去;I2+SO2+2H2O=4H++2I-+SO42-.
(2)A.硝酸具有强氧化性,能够将亚硫酸钠氧化成硫酸钠,无法得到二氧化硫气体,故A错误;
B.浓硫酸虽具有强酸性,且浓硫酸不挥发,亚硫酸钠溶液与浓硫酸能够反应生成二氧化硫气体,故B正确;
C.固体硫在纯氧中燃烧,操作不容易控制,且无法获得纯净的二氧化硫,故C错误;
D.Cu与浓硫酸在加热条件下生成二氧化硫、硫酸铜和水,可知制备二氧化硫,故D正确;
故答案为:BD;
(3)二氧化硫气体是酸性氧化物,具有刺激性气味,直接排放会污染大气,由于二氧化硫能和碱反应生成盐和水,可用碱液处理二氧化硫,所以装置C的作用为:吸收SO2尾气,防止污染空气,
故答案为:除去多余的SO2,防止污染大气;
(4)二氧化硫有还原性,高锰酸钾有强氧化性,二氧化硫能与高锰酸钾发生氧化还原反应使高锰酸钾溶液褪色,Fe2+也使高锰酸钾溶液褪色,所以方案①不合理,
故答案为:方案①;因为A的溶液中含有SO2,SO2也能使KMnO4溶液褪色;
(5)二氧化硫能使含有碘的淀粉溶液褪色,说明发生了氧化还原反应,碘是氧化剂,二氧化硫是还原剂,还原剂的还原性大于还原产物的还原性,其反应的离子方程式为:I2+SO2+2H2O=4H++2I-+SO42-;
故答案为:装置B中溶液蓝色褪去;I2+SO2+2H2O=4H++2I-+SO42-.
看了某兴趣小组探究SO2气体还原F...的网友还看了以下:
关于量子力学的用角动量量子化J=n*(hbar)推rn和En的过程中:圆轨道给出mv^2/r=e^ 2020-05-15 …
A、B、E为矩阵,A=1/2(B+E),当且仅当B^2为何值时,A^2=A?填空题,E应该为单位矩 2020-06-30 …
电阻R1、R2并联接入某电路,e们的电阻之比是3:2,则通过e们的电流之比和加在e们两端的电压之比 2020-07-13 …
MH代表储氢合金反应NiO(OH)+MH=Ni(OH)2+M他的放电反应式是-:MH-e+OH=H 2020-07-21 …
(2014•达州)有A、B、C、D、E五种物质,分别是Mg、MgSO4、Mg(OH)2、MgO、M 2020-07-22 …
(1)计算对数函数y=lnx对应于x取1/e^2,1/e,1,e,e^2时的函数值(2)计算对数函 2020-08-02 …
1e后面有4格2空一个e后面有3格3空2格e空2格4空3个e空1格5空4格e空1格6前面空5哥e后面 2020-10-30 …
已知函数f(x)=2㏑X-x图像上一点P(2,f(2))处的切线方程为y=-3x+2㏑2+2大神们帮 2020-12-08 …
两道数学题1.为什么e^1/4–2<0?为什么e^1/2–1>0?在只知道e^1/4-2和e^1/2 2021-01-04 …
A+、B+、C-、D、E五种粒子(分子或离子),它们分别含10个电子,已知它们有如下转化关系:①A+ 2021-01-04 …