早教吧作业答案频道 -->化学-->
溴乙烷是一种重要的有机化工原料,制备溴乙烷的原料有95%乙醇、80%硫酸(用蒸馏水稀释浓硫酸)、研细的溴化钠粉末和几粒碎瓷片,该反应的原理如下:NaBr+H2SO4→NaHSO4+HBrCH3CH2OH+HBr
题目详情
溴乙烷是一种重要的有机化工原料,制备溴乙烷的原料有95%乙醇、80%硫酸(用蒸馏水稀释浓硫酸)、研细的溴化钠粉末和几粒碎瓷片,该反应的原理如下:
NaBr+H2SO4→NaHSO4+HBr
CH3CH2OH+HBr
CH3CH2Br+H2O
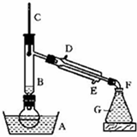
某课外小组欲在实验室制备溴乙烷的装置如图.数据如下表.
请回答下列问题.
(1)加入药品之前须做的操作是:___,实验进行的途中若发现未加入碎瓷片,其处理的方法是___.
(2)装置B的作用是除了使溴乙烷馏出,还有一个目的是___.温度计的温度应控制在___之间.
(3)反应时有可能生成SO2和一种红棕色气体,可选择氢氧化钠溶液除去该气体,有关的离子方程式是___,___,此操作可在___(填写玻璃仪器名称)中进行,同时进行分离.
(4)实验中采用80%硫酸,而不能用98%浓硫酸,一方面是为了减少副反应,另一方面是为了___.
(5)粗产品中含有的主要有机液体杂质是___,为进一步制得纯净的溴乙烷,对粗产品进行水洗涤、分液,再加入无水CaCl2,进行___操作.
NaBr+H2SO4→NaHSO4+HBr
CH3CH2OH+HBr
| 硫酸 |
| |
某课外小组欲在实验室制备溴乙烷的装置如图.数据如下表.
| 物质 数据 | 乙醇 | 溴乙烷 | 1,2-二溴乙烷 | 乙醚 | 浓硫酸 |
| 密度/g•cm-3 | 0.79 | 1.46 | 2.2 | 0.71 | 1.84 |
| 熔点(℃) | -130 | -119 | 9 | -116 | 10 |
| 沸点(℃) | 78.5 | 38.4 | 132 | 34.6 | 338 |
| 在水中的溶解度(g/100g水) | 互溶 | 0.914 | 1 | 7.5 | 互溶 |

(1)加入药品之前须做的操作是:___,实验进行的途中若发现未加入碎瓷片,其处理的方法是___.
(2)装置B的作用是除了使溴乙烷馏出,还有一个目的是___.温度计的温度应控制在___之间.
(3)反应时有可能生成SO2和一种红棕色气体,可选择氢氧化钠溶液除去该气体,有关的离子方程式是___,___,此操作可在___(填写玻璃仪器名称)中进行,同时进行分离.
(4)实验中采用80%硫酸,而不能用98%浓硫酸,一方面是为了减少副反应,另一方面是为了___.
(5)粗产品中含有的主要有机液体杂质是___,为进一步制得纯净的溴乙烷,对粗产品进行水洗涤、分液,再加入无水CaCl2,进行___操作.
▼优质解答
答案和解析
(1)实验室制备溴乙烷,用95%乙醇、80%硫酸(用蒸馏水稀释浓硫酸)、研细的溴化钠粉末为原料,反应中有气体生成,且乙醇易挥发,所以在加入药品之前应进行的操作是:检查装置的气密性;碎瓷片能防止液体爆沸,实验...
看了溴乙烷是一种重要的有机化工原料...的网友还看了以下:
一定量的稀硝酸溶液恰好与一定量的铁粉完全反应,若有四分之一的硝酸全部被还原成一氧化氮,则硝酸与铁粉 2020-05-16 …
一台粉碎机原来每天可加工饲料0.75吨,现在每天比原来多加工0.2吨.现在用这样的2台粉碎机加工1 2020-06-19 …
67、一台粉碎机原来每天可加工饲料0.75吨,现在每天比原来多加工0.2吨.现在用这样的2台粉碎机 2020-06-19 …
1.2.3.4···共十多个自然数.因为擦掉了1个,所以剩下的数的平均数是8.2.原来一共写了几个 2020-06-21 …
英语翻译线材在押出时过粉不充分,不均匀造成脱皮不良,而过粉不充分,不均匀可能为如下原因:1.过粉机 2020-06-22 …
根据意思写词语1.形容费尽心机.2.原指一部合乎道德规范的经典,后用以形容态度端庄严肃,郑重其事. 2020-06-27 …
工业上制漂粉精的化学方程式是什么?1.漂粉精的有效成分是什么?2.漂粉精在空气中久置失效的原理是( 2020-07-06 …
粮店原有一批面粉,第一次卖出1/3少4袋,第二次又卖出余的1/2少2袋,还剩下156袋.粮店原有面 2020-07-18 …
晓明的卧室有一扇门和一扇窗户,房间长8米,宽6米,高4米,门长2米、宽1米,窗户长4米,宽2米.( 2020-07-27 …
把5个完全一样的正方体拼成一个大长方体,表面积是440厘米2.原来一个正方体的表面积是多少平方厘米 2020-08-01 …