早教吧作业答案频道 -->化学-->
A、B、C、D、E、X是中学常见的无机物,存在如图转化关系(部分生成物和反应条件略去).(1)若A为常见的金属单质,焰色反应呈黄色,X能使品红溶液褪色,写出C和E反应的离子方程式:
题目详情
A、B、C、D、E、X是中学常见的无机物,存在如图转化关系(部分生成物和反应条件略去).
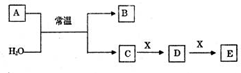
(1)若A为常见的金属单质,焰色反应呈黄色,X能使品红溶液褪色,写出C和E反应的离子方程式:___.
(2)若A为短周期元素组成的单质,该元素的最高价氧化物的水化物酸性最强,则:
①组成单质A的元素在周期表中的位置为___.
②X可能为___(填代号).
a.NaHCO3b.Na2CO3c.Na2SO3d.Al(OH)3
(3)若A为淡黄色粉末,回答下列问题:
①A与H2O反应的氧化产物为___.
②若X为非金属单质,通常为黑色粉末,写出E的化学式___.
③若X为一种造成温室效应的气体.则鉴别等浓度的D、E两种溶液,可选择的试剂为___(填代号).
a.盐酸b.BaCl2溶液c.NaOH溶液d.Ca(OH)2溶液
(4)若A为氧化物,X是Fe,溶液D中加入KSCN溶液变红.
①A与H2O反应的化学反应方程式为___.
②检验溶液D中还可能存在Fe2+的方法是___(注明试剂、现象).

(1)若A为常见的金属单质,焰色反应呈黄色,X能使品红溶液褪色,写出C和E反应的离子方程式:___.
(2)若A为短周期元素组成的单质,该元素的最高价氧化物的水化物酸性最强,则:
①组成单质A的元素在周期表中的位置为___.
②X可能为___(填代号).
a.NaHCO3b.Na2CO3c.Na2SO3d.Al(OH)3
(3)若A为淡黄色粉末,回答下列问题:
①A与H2O反应的氧化产物为___.
②若X为非金属单质,通常为黑色粉末,写出E的化学式___.
③若X为一种造成温室效应的气体.则鉴别等浓度的D、E两种溶液,可选择的试剂为___(填代号).
a.盐酸b.BaCl2溶液c.NaOH溶液d.Ca(OH)2溶液
(4)若A为氧化物,X是Fe,溶液D中加入KSCN溶液变红.
①A与H2O反应的化学反应方程式为___.
②检验溶液D中还可能存在Fe2+的方法是___(注明试剂、现象).
▼优质解答
答案和解析
(1)若A为常见的金属单质,焰色反应呈黄色,应为Na,X能使品红溶液褪色,应为SO2,则B为H2,C为NaOH,D为Na2SO3,E为NaHSO3,
C和E反应的离子方程式为OH-+HSO3-=SO32-+H2O,
故答案为:OH-+HSO3-=SO32-+H2O;
(2)若A为短周期元素组成的单质,该元素的最高价氧化物的水化物酸性最强,应为Cl2,则B为HClO,C为HCl,
①Cl原子核外有3个电子层,最外层电子数为7,位于周期表第三周期ⅦA族,
故答案为:第三周期ⅦA族;
②C为盐酸,可与NaHCO3反应生成CO2,但CO2与NaHCO3不反应,故a错误;与Na2CO3反应生成CO2,CO2与Na2CO3反应可生成NaHCO3,故b正确;与Na2SO3反应生成SO2,SO2与Na2SO3反应可生成NaHSO3,故c正确;盐酸与氢氧化铝反应生成氯化铝,氯化铝与氢氧化铝不反应,故d错误,
故答案为:bc;
(3)若A为淡黄色粉末,应为Na2O2;
①A与足量的H2O充分反应时过氧化钠自身发生氧化还原反应,氧化产物为O2,
故答案为:O2;
②若X为非金属单质,通常为黑色粉末,应为C,则D为CO2,E为CO,
故答案为:CO;
③若X为一种造成温室效应的气体,应为CO2,则C为NaOH,D为Na2CO3,E为NaHCO3,鉴别等浓度的D、E两种溶液,可用盐酸或氯化钡溶液,
故答案为:ab;
(4)若A为氧化物,X是Fe,由转化关系可知C具有强氧化性,则A为NO2,B为NO,C为HNO3,
①NO2与水反应的方程式为3NO2+H2O=2HNO3+NO,
故答案为:3NO2+H2O=2HNO3+NO;
②Fe2+具有还原性,可与酸性高锰酸钾发生氧化还原反应而使高锰酸钾褪色,则可用高锰酸钾溶液检验,操作为取D中适量溶液置于洁净试管中,滴加几滴酸性高锰酸钾溶液,充分反应后褪色,证明溶液中含有亚铁离子,否则无,
故答案为:取D中适量溶液置于洁净试管中,滴加几滴酸性高锰酸钾溶液,充分反应后褪色,证明溶液中含有亚铁离子,否则无.
C和E反应的离子方程式为OH-+HSO3-=SO32-+H2O,
故答案为:OH-+HSO3-=SO32-+H2O;
(2)若A为短周期元素组成的单质,该元素的最高价氧化物的水化物酸性最强,应为Cl2,则B为HClO,C为HCl,
①Cl原子核外有3个电子层,最外层电子数为7,位于周期表第三周期ⅦA族,
故答案为:第三周期ⅦA族;
②C为盐酸,可与NaHCO3反应生成CO2,但CO2与NaHCO3不反应,故a错误;与Na2CO3反应生成CO2,CO2与Na2CO3反应可生成NaHCO3,故b正确;与Na2SO3反应生成SO2,SO2与Na2SO3反应可生成NaHSO3,故c正确;盐酸与氢氧化铝反应生成氯化铝,氯化铝与氢氧化铝不反应,故d错误,
故答案为:bc;
(3)若A为淡黄色粉末,应为Na2O2;
①A与足量的H2O充分反应时过氧化钠自身发生氧化还原反应,氧化产物为O2,
故答案为:O2;
②若X为非金属单质,通常为黑色粉末,应为C,则D为CO2,E为CO,
故答案为:CO;
③若X为一种造成温室效应的气体,应为CO2,则C为NaOH,D为Na2CO3,E为NaHCO3,鉴别等浓度的D、E两种溶液,可用盐酸或氯化钡溶液,
故答案为:ab;
(4)若A为氧化物,X是Fe,由转化关系可知C具有强氧化性,则A为NO2,B为NO,C为HNO3,
①NO2与水反应的方程式为3NO2+H2O=2HNO3+NO,
故答案为:3NO2+H2O=2HNO3+NO;
②Fe2+具有还原性,可与酸性高锰酸钾发生氧化还原反应而使高锰酸钾褪色,则可用高锰酸钾溶液检验,操作为取D中适量溶液置于洁净试管中,滴加几滴酸性高锰酸钾溶液,充分反应后褪色,证明溶液中含有亚铁离子,否则无,
故答案为:取D中适量溶液置于洁净试管中,滴加几滴酸性高锰酸钾溶液,充分反应后褪色,证明溶液中含有亚铁离子,否则无.
看了 A、B、C、D、E、X是中学...的网友还看了以下:
已知:图甲是由某温度下Fe(OH)3(s)、Cu(OH)2(s)分别在溶液中达到沉淀溶解平衡后,改 2020-05-13 …
将同一植物的细胞,依次浸在蒸馏水、0.3moL的蔗糖溶液和0.5mol的尿素溶液中,测得细胞的体积 2020-05-15 …
由氢气和氯气按物质的量为3:7组成的混合气体在一定条件下反应,将反应后的气体通入amol的氢氧化钠 2020-05-17 …
图书>少儿>科普/百科图书>科普读物>儿童科普在中图法中属于哪一类顺便把英文字母标上,书名:灵泉. 2020-06-18 …
已知在常温下Cu2+和Fe3+在溶液中随pH变化时水解的曲线如图所示,对图中a点的说法正确的是() 2020-07-15 …
往氯水中滴入Na2SO3溶液的pH变化如图所示,下列说法正确的是()A.a点表示的溶液中存在3种分 2020-07-20 …
如图为某固体溶解度随温度变化的曲线.该固体从溶液中析出时不带结晶水.M、N两点分别表示该固体形成的 2020-07-29 …
补一问:如果ABC三个细胞处于同一浓度的溶液中,图中各细胞细胞液浓度大小?我填的是A>C>B,可答案 2020-11-03 …
7.下列图象是在一定温度下,向不同电解质溶液中加入新物质时,溶液的导电性能(I)随7.下列图象是在一 2021-01-13 …
如图所示是某化学兴趣小组探究溶液中离子浓度与溶液导电能力的关系装置图.首先在水槽中加入200mL2m 2021-01-13 …