早教吧作业答案频道 -->化学-->
某化学兴趣小组为探究元素性质的递变规律,设计了如下系列实验.Ⅰ、(1)将钠、钾、镁、铝各1mol分别投入到足量的0.1mol•L-1的盐酸中,试预测实验结果:与盐酸反应最剧烈,与盐
题目详情
某化学兴趣小组为探究元素性质的递变规律,设计了如下系列实验.
Ⅰ、(1)将钠、钾、镁、铝各1mol分别投入到足量的0.1mol•L-1的盐酸中,试预测实验结果:___与盐酸反应最剧烈,___与盐酸反应最慢.
(2)将NaOH溶液与NH4Cl溶液混合生成NH3•H2O,从而验证NaOH的碱性大于NH3•H2O,继而可以验证Na的金属性大于N,你认为此设计是否合理?___;说明理由:___.
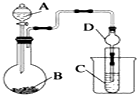
Ⅱ.、利用如图装置可以验证非金属性的变化规律.
(3)仪器A的名称为___,干燥管D的作用是___.
(4)实验室中现有药品Na2S、KMnO4、浓盐酸、MnO2,请在其中选择合适药品设计实验验证氯的非金属性大于硫:装置A、B、C中所装药品分别为___、___、___,装置C中的实验现象为有淡黄色沉淀生成,离子方程式为___.
(5)若要证明非金属性:C>Si,请根据所学过的知识选择相应的试剂,则A中加___、B中加Na2CO3、C中加___,观察到C中溶液的现象为___.
Ⅰ、(1)将钠、钾、镁、铝各1mol分别投入到足量的0.1mol•L-1的盐酸中,试预测实验结果:___与盐酸反应最剧烈,___与盐酸反应最慢.
(2)将NaOH溶液与NH4Cl溶液混合生成NH3•H2O,从而验证NaOH的碱性大于NH3•H2O,继而可以验证Na的金属性大于N,你认为此设计是否合理?___;说明理由:___.
Ⅱ.、利用如图装置可以验证非金属性的变化规律.
(3)仪器A的名称为___,干燥管D的作用是___.
(4)实验室中现有药品Na2S、KMnO4、浓盐酸、MnO2,请在其中选择合适药品设计实验验证氯的非金属性大于硫:装置A、B、C中所装药品分别为___、___、___,装置C中的实验现象为有淡黄色沉淀生成,离子方程式为___.
(5)若要证明非金属性:C>Si,请根据所学过的知识选择相应的试剂,则A中加___、B中加Na2CO3、C中加___,观察到C中溶液的现象为___.

▼优质解答
答案和解析
I、(1)同一周期元素,金属性随着原子序数增大而减弱,元素的金属性越强,同一主族,原子序数越大,金属性越强,其单质与酸或水反应越剧烈,所以金属性K>Na>Mg>Al,则K与盐酸反应最剧烈、Al与盐酸反应...
看了某化学兴趣小组为探究元素性质的...的网友还看了以下:
关于氢氧化铝的有些问题制备氢氧化铝时,如果用铝盐溶液,应该加入足量___,因为氢氧化铝不与___反 2020-05-17 …
将某镁铝合金3.9克投入足量的盐酸中,可得气体0.02MOL,求合金中铝的质量分数.溶将某镁铝合金 2020-05-23 …
下列关于铁和铝的性质叙述错误的是()A.补血剂中含有+2价铁元素B.铝比铁耐腐蚀,说明铝比铁稳定C 2020-06-19 …
工业上用铝土矿(主要成分为Al2O3、Fe2O3、SiO2)提取氧化铝做冶炼铝的原料,提取的操作过 2020-07-10 …
在一个钢质零件上面挖一个洞再用铝填平替换后零件总重减少51牛则填入...在一个钢质零件上面挖一个洞 2020-07-21 …
铝热反应是铝的一个重要性质.某校化学兴趣小组同学,取磁性氧化铁在如图1验装置进行铝热反应,冷却后得到 2020-11-02 …
在金属中,铝已经够轻了,后来科研人员受泡沫塑料的启发,又研制出了更轻的铝--泡沫铝.在纯铝或铝合金中 2020-12-14 …
下列关于铁和铝的性质叙述错误的是()A.补血剂中含有+2价铁元素B.铝比铁耐腐蚀,说明铝比铁稳定C. 2020-12-20 …
把5.1g镁铝合金放入足量盐酸把5.1g镁铝合金的粉末放入过量的盐酸中,得到5.6LH2(标准状况下 2021-01-13 …
把含有10.2g氧化铝的铝条放入1L1.5mol/L热的NaOH溶液中,过一段时间取出铝条,溶液增重 2021-01-13 …