早教吧作业答案频道 -->化学-->
废旧铅蓄电池的回收利用是发展循环经济的必经之路.其阴、阳极填充物(铅膏,主要含PbO、PbO2、PbSO4)是废旧铅蓄电池的主要部分,回收时所得黄丹(PbO)、碳酸铅可用于合成三盐基硫酸
题目详情
废旧铅蓄电池的回收利用是发展循环经济的必经之路.其阴、阳极填充物(铅膏,主要含PbO、PbO2、PbSO4)是废旧铅蓄电池的主要部分,回收时所得黄丹(PbO)、碳酸铅可用于合成三盐基硫酸铅(组成可表示为3PbO•PbSO4•H2O),其工艺流程如下:
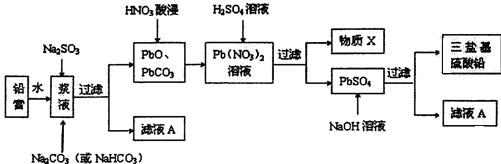
(1)用碳酸盐作转化剂,将铅膏中的硫酸铅转化为碳酸铅,转化反应式如下:
PbSO4(s)+CO32-(aq)⇌PbCO3(s)+SO42-(aq)
①下列说法错误的是:___.
A.PbSO4的Ksp比PbCO3的Ksp大
B.该反应平衡时,c(CO32-)=c(SO42-)
C.该反应的平衡常数K=
②室温时,向两份相同的PbSO4样品中分别加入同体积、同浓度的Na2CO3和NaHCO3溶液均可实现上述转化,在___溶液中PbSO4转化率较大,理由是___.
(2)滤液A能用来回收Na2SO4•10H2O,提取该晶体的主要步骤有___、___、过滤、洗涤、干燥;检验该晶体中阴离子的实验方法是___.
(3)物质X是一种可循环使用的物质,其溶质主要是___(填化学式),若X中残留的SO42-过多,循环利用时可能出现的问题是___.
(4)生成三盐基硫酸铅的离子方程式为___.
(5)向铅膏浆液中加入Na2SO3溶液的目的是将其中的PbO2还原为PbO.若实验中所取铅膏的质量为47.8g,其中PbO2的质量分数为15%,则要将PbO2全部还原,至少需要加入___mL的0.5mol•L-1 Na2SO3溶液.

(1)用碳酸盐作转化剂,将铅膏中的硫酸铅转化为碳酸铅,转化反应式如下:
PbSO4(s)+CO32-(aq)⇌PbCO3(s)+SO42-(aq)
①下列说法错误的是:___.
A.PbSO4的Ksp比PbCO3的Ksp大
B.该反应平衡时,c(CO32-)=c(SO42-)
C.该反应的平衡常数K=
| KSP(PbSO4) |
| KSP(PbCO3) |
②室温时,向两份相同的PbSO4样品中分别加入同体积、同浓度的Na2CO3和NaHCO3溶液均可实现上述转化,在___溶液中PbSO4转化率较大,理由是___.
(2)滤液A能用来回收Na2SO4•10H2O,提取该晶体的主要步骤有___、___、过滤、洗涤、干燥;检验该晶体中阴离子的实验方法是___.
(3)物质X是一种可循环使用的物质,其溶质主要是___(填化学式),若X中残留的SO42-过多,循环利用时可能出现的问题是___.
(4)生成三盐基硫酸铅的离子方程式为___.
(5)向铅膏浆液中加入Na2SO3溶液的目的是将其中的PbO2还原为PbO.若实验中所取铅膏的质量为47.8g,其中PbO2的质量分数为15%,则要将PbO2全部还原,至少需要加入___mL的0.5mol•L-1 Na2SO3溶液.
▼优质解答
答案和解析
(1)①A.用碳酸盐作转化剂,将铅膏中的硫酸铅转化为碳酸铅,说明碳酸铅的溶解度小于硫酸铅,所以PbSO4的Ksp比PbCO3的Ksp大,故正确;
B.浓度不变不一定相等,故错误;
C.根据反应的平衡常数的表达式书写,K=
的分子和分母同乘以铅离子的浓度,即K=
,故正确;
故选:B;
②碳酸根离子浓度越大硫酸铅的转化率越高,而碳酸钠直接电离产生碳酸根离子,而碳酸氢钠是多元弱酸的酸式盐,盐电离产生的酸根离子碳酸氢根离子微弱的电离产生碳酸根离子,所以同浓度的两种盐,碳酸钠溶液中的碳酸根离子浓度大于碳酸氢钠溶液中碳酸根离子的浓度,
故答案为:Na2CO3;相同浓度的Na2CO3和NaHCO3溶液中,前者c(CO32-)较大;
(2)回收Na2SO4•10H2O,温度不宜过高,否则容易失去结晶水,所以溶液中得到溶质晶体的方法为:蒸发浓缩,冷却结晶,过滤洗涤,干燥等;Na2SO4•10H2O中阴离子为SO42-,检验硫酸根离子的方法为:取少量晶体溶于蒸馏水,然后用盐酸酸化,再滴BaCl2溶液,若出现白色沉淀,即证明该晶体中含有SO42-,
故答案为:蒸发浓缩;冷却结晶;取少量晶体溶于蒸馏水,然后用盐酸酸化,再滴BaCl2溶液,若出现白色沉淀,即证明该晶体中含有SO42-;
(3)由流程可知,PbO和PbCO3在硝酸的作用下转化成Pb(NO3)2 ,Pb(NO3)2中加稀H2SO4转化成PbSO4和硝酸,因此X为HNO3,HNO3在反应流程中可循环利用;
若母液中残留的SO42-过多,浸出时部分铅离子会与SO42-反应生成PbSO4随浸出渣排出,降低了PbSO4的产率,
故答案为:HNO3 ;浸出时部分铅离子生成PbSO4随浸出渣排出,降低PbSO4的产率;
(4)硫酸铅在碱溶液中与氢氧根离子反应生成三盐基硫酸铅,反应的离子方程式为:4PbSO4+6OH-=3PbO•PbSO4•H2O+3SO42-+2H2O,
故答案为:4PbSO4+6OH-=3PbO•PbSO4•H2O+3SO42-+2H2O;
(5)向铅膏浆液中加入Na2SO3溶液的目的是将PbO2还原为PbO,若实验中所取铅膏浆液质量为47.8g,其中PbO2的质量分数为15.0%,要将PbO2还原,加入的亚硫酸钠依据化学方程式定量关系和电子守恒计算得到:Na2SO3~2e-~PbO2,
则:n(Na2SO3)=n( PbO2)=
=0.03mol,
所以需要亚硫酸钠溶液的体积为:
=0.06L=60mL,
故答案为:60.
B.浓度不变不一定相等,故错误;
C.根据反应的平衡常数的表达式书写,K=
c(S
| ||
c(C
|
| KSP(PbSO4) |
| KSP(PbCO3) |
故选:B;
②碳酸根离子浓度越大硫酸铅的转化率越高,而碳酸钠直接电离产生碳酸根离子,而碳酸氢钠是多元弱酸的酸式盐,盐电离产生的酸根离子碳酸氢根离子微弱的电离产生碳酸根离子,所以同浓度的两种盐,碳酸钠溶液中的碳酸根离子浓度大于碳酸氢钠溶液中碳酸根离子的浓度,
故答案为:Na2CO3;相同浓度的Na2CO3和NaHCO3溶液中,前者c(CO32-)较大;
(2)回收Na2SO4•10H2O,温度不宜过高,否则容易失去结晶水,所以溶液中得到溶质晶体的方法为:蒸发浓缩,冷却结晶,过滤洗涤,干燥等;Na2SO4•10H2O中阴离子为SO42-,检验硫酸根离子的方法为:取少量晶体溶于蒸馏水,然后用盐酸酸化,再滴BaCl2溶液,若出现白色沉淀,即证明该晶体中含有SO42-,
故答案为:蒸发浓缩;冷却结晶;取少量晶体溶于蒸馏水,然后用盐酸酸化,再滴BaCl2溶液,若出现白色沉淀,即证明该晶体中含有SO42-;
(3)由流程可知,PbO和PbCO3在硝酸的作用下转化成Pb(NO3)2 ,Pb(NO3)2中加稀H2SO4转化成PbSO4和硝酸,因此X为HNO3,HNO3在反应流程中可循环利用;
若母液中残留的SO42-过多,浸出时部分铅离子会与SO42-反应生成PbSO4随浸出渣排出,降低了PbSO4的产率,
故答案为:HNO3 ;浸出时部分铅离子生成PbSO4随浸出渣排出,降低PbSO4的产率;
(4)硫酸铅在碱溶液中与氢氧根离子反应生成三盐基硫酸铅,反应的离子方程式为:4PbSO4+6OH-=3PbO•PbSO4•H2O+3SO42-+2H2O,
故答案为:4PbSO4+6OH-=3PbO•PbSO4•H2O+3SO42-+2H2O;
(5)向铅膏浆液中加入Na2SO3溶液的目的是将PbO2还原为PbO,若实验中所取铅膏浆液质量为47.8g,其中PbO2的质量分数为15.0%,要将PbO2还原,加入的亚硫酸钠依据化学方程式定量关系和电子守恒计算得到:Na2SO3~2e-~PbO2,
则:n(Na2SO3)=n( PbO2)=
| 47.8g×15% |
| 239g/mol |
所以需要亚硫酸钠溶液的体积为:
| 0.03mol |
| 0.5mol/L |
故答案为:60.
看了废旧铅蓄电池的回收利用是发展循...的网友还看了以下:
抽水蓄能电站在缓解用电高峰电力紧张方面,取得了良好的社会效益和经济效益.抽蓄水能电站的工作原理是: 2020-05-17 …
一道计算蓄能电站发电量的物理题,急!赏50分抽水蓄能电站不同于一般的水力发电站.一般的水力发电站是 2020-06-26 …
铅蓄电池的两极分别为Pb和PbO2,电解质溶液为H2SO4,工作时发生的反应为:Pb+PbO2+2 2020-06-30 …
关于原电池电极式1.铅蓄电池:(负极—Pb正极—PbO2电解液—稀硫酸)总化学方程式Pb+PbO2+ 2020-11-01 …
南阳市南召县回龙抽水蓄能电站,是我省第一座抽水蓄能电站。在深夜用电低谷,它用电网过剩的电能把山下水库 2020-11-12 …
南阳市南召县回龙抽水蓄水能电站,是我省第一座抽水蓄能电站.在深夜用电低估,它用电网过剩的电能把山下水 2020-11-12 …
到2015年,江苏省最大的抽水蓄能电站将在溧阳建成。抽水蓄能电站的工作原理是:用电低谷时,电站利用电 2020-12-27 …
到2015年,江苏省最大的抽水蓄能电站将在溧阳建成.抽水蓄能电站的工作原理是:用电低谷时,电站利用电 2020-12-27 …
南阳市南召县回龙抽水蓄水能电站,是我省第一座抽水蓄能电站.在深夜用电低谷,它用电网过剩的电能把山下水 2020-12-27 …
十三陵抽水蓄能电站的工作原理是,在用电低谷时,电站利用电网多余电能把水抽到高出蓄水池中,到用电高峰时 2020-12-27 …