早教吧作业答案频道 -->化学-->
(1)铁元素能形成多种配合物,如:Fe(CO)x①基态Fe3+的M层电子排布式为.②配合物Fe(CO)x的中心原子价电子数与配体提供电子数之和为18,则x=.常温下呈液态,熔点为-20.5℃,沸点
题目详情
(1)铁元素能形成多种配合物,如:Fe(CO)x
①基态Fe3+的M层电子排布式为___.
②配合物Fe(CO)x的中心原子价电子数与配体提供电子数之和为18,则x=___.常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)x晶体属于___(填晶体类型).
(2)氨分子中氮原子的杂化类型是___,如图1氨水中四种氢键哪一种是最主要的___.
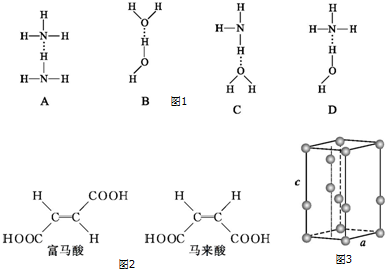
(3)试分析如图2富马酸的K2大于其顺式异构体马来酸的K2,原因是___.
(4)常压下,水冷却至0℃以下,即可结晶成六方晶系的冰.日常生活中见到的冰、霜和雪等都是属于这种结构,其晶胞如图3所示(只显示氧原子,略去氢原子),晶胞参数侧棱c=737pm,菱形底边a=452pm,底面菱形的锐角是60°.(sin60°=0.865)
回答下列问题:
①计算每个晶胞中含有___个水分子.
②计算冰的密度ρ=___ g•cm-3.
①基态Fe3+的M层电子排布式为___.
②配合物Fe(CO)x的中心原子价电子数与配体提供电子数之和为18,则x=___.常温下呈液态,熔点为-20.5℃,沸点为103℃,易溶于非极性溶剂,据此可判断Fe(CO)x晶体属于___(填晶体类型).
(2)氨分子中氮原子的杂化类型是___,如图1氨水中四种氢键哪一种是最主要的___.

(3)试分析如图2富马酸的K2大于其顺式异构体马来酸的K2,原因是___.
(4)常压下,水冷却至0℃以下,即可结晶成六方晶系的冰.日常生活中见到的冰、霜和雪等都是属于这种结构,其晶胞如图3所示(只显示氧原子,略去氢原子),晶胞参数侧棱c=737pm,菱形底边a=452pm,底面菱形的锐角是60°.(sin60°=0.865)
回答下列问题:
①计算每个晶胞中含有___个水分子.
②计算冰的密度ρ=___ g•cm-3.
▼优质解答
答案和解析
(1)①Fe原子核外有26个电子,核外电子排布为1s22s22p63s23p63d64s2,Fe原子失去4s能级2个电子、3d能级1个电子形成Fe3+,Fe3+电子排布式为1s22s22p63s23p63d5,则M层电子排布式为:3s23p63d5,
故答案为:3s23p63d5;
②配合物Fe(CO)x的中心原子是铁原子,其价电子数是8,每个配体提供的电子数是2,8+2x=18,x=5,分子晶体的熔沸点较低,根据题给信息知,该物质的熔沸点较低,所以为分子晶体,
故答案为:5;分子晶体;
(2)NH3中只含有单键为σ键,分子中N原子含有3个σ键电子对和1个孤电子对,杂化类型为sp3,氨水中的氢键主要是氨气分子中氮原子和水分子中氢原子间的氢键,即D选项表示的氢键,
故答案为:sp3;D;
(3)马来酸属于顺式结构,羧基上与氧原子相连的氢原子和氧原子间形成氢键,导致氢原子不易电离,酸性减弱;
故答案为:马来酸分子中酸性氢原子参与形成分子内氢键,其酸性减弱;
(4):①冰晶胞中顶点有8个分子,棱上有4个分子,体内有2个分子,晶胞中含有水分子的个数为:8×
+4×
+2=4,晶胞中含有4个水分子,
故答案为:4;
②ρ=
=
=
=0.917 g•cm-3
故答案为:0.917.
故答案为:3s23p63d5;
②配合物Fe(CO)x的中心原子是铁原子,其价电子数是8,每个配体提供的电子数是2,8+2x=18,x=5,分子晶体的熔沸点较低,根据题给信息知,该物质的熔沸点较低,所以为分子晶体,
故答案为:5;分子晶体;
(2)NH3中只含有单键为σ键,分子中N原子含有3个σ键电子对和1个孤电子对,杂化类型为sp3,氨水中的氢键主要是氨气分子中氮原子和水分子中氢原子间的氢键,即D选项表示的氢键,
故答案为:sp3;D;
(3)马来酸属于顺式结构,羧基上与氧原子相连的氢原子和氧原子间形成氢键,导致氢原子不易电离,酸性减弱;
故答案为:马来酸分子中酸性氢原子参与形成分子内氢键,其酸性减弱;
(4):①冰晶胞中顶点有8个分子,棱上有4个分子,体内有2个分子,晶胞中含有水分子的个数为:8×
| 1 |
| 8 |
| 1 |
| 4 |
故答案为:4;
②ρ=
| m |
| v |
| ||
| a2•c•sin60° |
| ||
| 4522×737×0.866×(10-10)3 |
故答案为:0.917.
看了(1)铁元素能形成多种配合物,...的网友还看了以下:
球的体积公式是V=4/3πr的三次方,将两个半径为5.2cm的小铁球熔炼成一个大铁球,已知每立方米 2020-05-13 …
实验室用铁粉和稀硫酸反应制取氧气,现在用10g的铁和100g9.8%的稀硫酸反应,能制的多少L氢气 2020-05-14 …
把棱长分别为2.15cm和3.24cm的两个正方体铁块熔化,制成一个大的正方体铁块,求这个大正方体 2020-05-14 …
两到中学陪优物理题目.1.把7.9千克的铁和10.8千克的铝混合在一起作成铝合金,求铝合金的密度? 2020-05-20 …
把一个棱长为六分米的正方体铁块和一个底面积是31.4平方分米,高是3分米的圆锥形铁块熔铸成一个底面 2020-05-23 …
纯铁的熔点是1535.c,但在高炉中,铁在1200.c左右就熔化了,这是因为——A.脉石降低了铁的 2020-06-19 …
有谁知道10g的铁被熔化需要的热量是多少J?熔化10g铁的功率又是多少W?有谁知道10g的铁被熔化 2020-07-20 …
(2000•烟台)用铁锅可以熔化铝,而用铝锅却不能熔化铁,这主要是因为()A.铁的传热性能比铝差B. 2020-11-13 …
铜钱在历史上曾经是一种广泛流通的货币,已知铜的熔点是1083.4℃,铁的熔点是1534.8℃.(1) 2020-12-05 …
回答下列有关金属的问题:(1)铜钱在历史上曾经是一种广泛流通的货币.已知铜的熔点是1083.4℃,铁 2021-01-22 …