早教吧作业答案频道 -->化学-->
雾霾天气肆虐给人类健康带来了严重影响.燃煤和汽车尾气是造成空气污染的原因之一.(1)汽车尾气净化的主要原理为:2NO(g)+2CO催化剂加热
题目详情
雾霾天气肆虐给人类健康带来了严重影响.燃煤和汽车尾气是造成空气污染的原因之一.
(1)汽车尾气净化的主要原理为:2NO(g)+2CO
2CO2(g)+N2(g)△H<O
①反应的速率时间罔像如图1所示.若其他条件不变,仅在反应前加入合适的催化剂,其速率时间图象如图2所示.以下说法正确的是___(填对应字母).
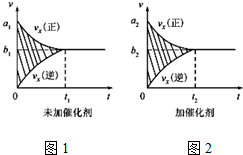
A.a1>a2,B.b1<b2 C.t1>t2
D.图2中阴影部分面积更大
E.图1中阴影部分面积更大
②若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是___(填代号)
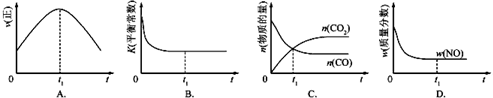
(2)直接排放煤燃烧产生的烟气会引起严重的环境问题.煤燃烧产生的烟气含氮的氧化物,用CH4催化还原NOx可以消除氮氧化物的污染.
已知:CH4(g)+2NO2(g)⇌N2(g)+CO2(g)+2H2O(g)△H=-867kJ/mol
2NO2(g)⇌N2O4(g)△H=-56.9kJ/mol H2O(g)=H2O(l)△H=-44.0kJ/mol
写出CH4催化还原N2O4(g)生成N2和H2O(l)的热化学方程式:___.
(3)CH4和H2O(g) 在催化剂表面发生反应CH4+H2O⇌CO+3H2,该反应在不同温度下的化学平衡常数如表:
①该反应是___反应(填“吸热”或“放热”).
②T℃时,向1L密闭容器中投人l mol CH4和l mol H2O(g),平衡时c(CH4)=0.5mol/L,该温度下反应CH4+H2O⇌CO+3H2的平衡常数K=___.
(4)甲烷燃料电池可以提升能量利用率.如图是利用甲烷燃料电池电解100ml1mol/L食盐水,电解一段时间后,收集到标准状况下的氢气2.24L(设电解后溶液体积不变).
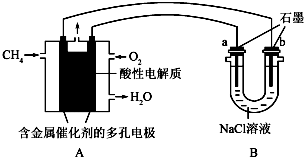
①甲烷燃料电池的负极反应式:___
②电解后溶液的pH=___(忽略氯气与氢氧化钠溶液反应)
③阳极产生气体的体积在标准状况下是___L.
(1)汽车尾气净化的主要原理为:2NO(g)+2CO
| 催化剂 |
| |
| 加热 |
①反应的速率时间罔像如图1所示.若其他条件不变,仅在反应前加入合适的催化剂,其速率时间图象如图2所示.以下说法正确的是___(填对应字母).

A.a1>a2,B.b1<b2 C.t1>t2
D.图2中阴影部分面积更大
E.图1中阴影部分面积更大
②若该反应在绝热、恒容的密闭体系中进行,下列示意图正确且能说明反应在进行到t1时刻达到平衡状态的是___(填代号)

(2)直接排放煤燃烧产生的烟气会引起严重的环境问题.煤燃烧产生的烟气含氮的氧化物,用CH4催化还原NOx可以消除氮氧化物的污染.
已知:CH4(g)+2NO2(g)⇌N2(g)+CO2(g)+2H2O(g)△H=-867kJ/mol
2NO2(g)⇌N2O4(g)△H=-56.9kJ/mol H2O(g)=H2O(l)△H=-44.0kJ/mol
写出CH4催化还原N2O4(g)生成N2和H2O(l)的热化学方程式:___.
(3)CH4和H2O(g) 在催化剂表面发生反应CH4+H2O⇌CO+3H2,该反应在不同温度下的化学平衡常数如表:
| 温度/℃ | 800 | 1000 | 1200 | 1400 |
| 平衡常数 | 0.45 | 1.92 | 276.5 | 1771.5 |
②T℃时,向1L密闭容器中投人l mol CH4和l mol H2O(g),平衡时c(CH4)=0.5mol/L,该温度下反应CH4+H2O⇌CO+3H2的平衡常数K=___.
(4)甲烷燃料电池可以提升能量利用率.如图是利用甲烷燃料电池电解100ml1mol/L食盐水,电解一段时间后,收集到标准状况下的氢气2.24L(设电解后溶液体积不变).

①甲烷燃料电池的负极反应式:___
②电解后溶液的pH=___(忽略氯气与氢氧化钠溶液反应)
③阳极产生气体的体积在标准状况下是___L.
▼优质解答
答案和解析
(1)①加入催化剂,正逆反应速率都增大,达到平衡所用时间较少,但平衡不移动,则图象阴影部分面积不变,故答案为:BC;
②A.到达平衡后正、逆速率相等,不再变化,t1时刻V正最大,之后随反应进行速率发生变化,未到达平衡,故A错误;
B.该反应正反应为放热反应,随反应进行温度升高,化学平衡常数减小,到达平衡后,温度为定值,达最高,平衡常数不变,为最小,图象与实际符合,故B正确;
C.t1时刻后二氧化碳、CO的物质的量发生变化,t1时刻未到达平衡状态,故C错误;
D.NO的质量分数为定值,t1时刻处于平衡状态,故D正确,
故答案为:BD;
(2)已知:CH4(g)+2NO2(g)═N2(g)+CO2(g)+2H2O(g)△H1=-867kJ/mol①
2NO2(g)⇌N2O4(g)△H2=-56.9kJ/mol②
H2O(g)=H2O(l)△H=-44.0kJ/mol③
根据盖斯定律,①-②+④×2可得CH4(g)+N2O4(g)=N2(g)+CO2(g)+2H2O(l),故△H=-867kJ/mol-(-56.9kJ/mol)+2(-44.0)kJ/mol=-898.1kJ/mol 即CH4(g)+N2O4(g)═N2(g)+2H2O(l)+CO2(g)△H=-898.1kJ/mol,
故答案为:CH4(g)+N2O4(g)═N2(g)+2H2O(l)+CO2(g)△H=-898.1kJ/mol;
(3)①温度升高,平衡常数增大即平衡向正反应方向移动,故该反应为吸热反应,
故答案为:吸热;
②T℃时,向1L密闭容器中投入1molCH4和1mol H2O(g),平衡时c(CH4)=0.5mol•L-1,该温度K=
=
=6.75,
故答案为:6.75;
(4)①、原电池负极发生氧化反应,甲烷在负极通入,酸性条件下,发生氧化反应生成CO2、H+,负极电极反应式为:CH4-8e-+2H2O=CO2+8H+,
故答案为:CH4-8e-+2H2O=CO2+8H+;
②100mL 1mol/L食盐水中含有氯化钠0.1mol,根据反应方程式2NaCl+2H2O
2NaOH+H2↑+Cl2↑可知,电解0.1molNaCl生成0.1mol氢氧化钠和0.05mol氢气,同时生成0.05mol氯气;继续电解实质为电解水,标况下2.24L氢气的物质的量为0.1mol,电解水生成0.05mol氢气会生成0.025mol氧气,及电解过程中阳极总共生成0.075mol气体,
电解生成标况下2.24L氢气时,NaCl完全电解,生成0.1molNaOH,溶液体积为0.1L,则c(OH-)=1mol/L,c(H+)=10-14,所以PH=14,
故答案为:14;
③根据②的分析可知,电解过程中阳极生成了0.05mol氯气和0.025mol氧气,总共生成0.075mol气体,标准状况下阳极生成气体的体积为:22.4L/mol×0.075mol=1.68L,
故答案为:1.68.
②A.到达平衡后正、逆速率相等,不再变化,t1时刻V正最大,之后随反应进行速率发生变化,未到达平衡,故A错误;
B.该反应正反应为放热反应,随反应进行温度升高,化学平衡常数减小,到达平衡后,温度为定值,达最高,平衡常数不变,为最小,图象与实际符合,故B正确;
C.t1时刻后二氧化碳、CO的物质的量发生变化,t1时刻未到达平衡状态,故C错误;
D.NO的质量分数为定值,t1时刻处于平衡状态,故D正确,
故答案为:BD;
(2)已知:CH4(g)+2NO2(g)═N2(g)+CO2(g)+2H2O(g)△H1=-867kJ/mol①
2NO2(g)⇌N2O4(g)△H2=-56.9kJ/mol②
H2O(g)=H2O(l)△H=-44.0kJ/mol③
根据盖斯定律,①-②+④×2可得CH4(g)+N2O4(g)=N2(g)+CO2(g)+2H2O(l),故△H=-867kJ/mol-(-56.9kJ/mol)+2(-44.0)kJ/mol=-898.1kJ/mol 即CH4(g)+N2O4(g)═N2(g)+2H2O(l)+CO2(g)△H=-898.1kJ/mol,
故答案为:CH4(g)+N2O4(g)═N2(g)+2H2O(l)+CO2(g)△H=-898.1kJ/mol;
(3)①温度升高,平衡常数增大即平衡向正反应方向移动,故该反应为吸热反应,
故答案为:吸热;
②T℃时,向1L密闭容器中投入1molCH4和1mol H2O(g),平衡时c(CH4)=0.5mol•L-1,该温度K=
| c(CO)c3(H2) |
| c(CH4)c(H2O) |
| 0.5×1.53 |
| 0.5×0.5 |
故答案为:6.75;
(4)①、原电池负极发生氧化反应,甲烷在负极通入,酸性条件下,发生氧化反应生成CO2、H+,负极电极反应式为:CH4-8e-+2H2O=CO2+8H+,
故答案为:CH4-8e-+2H2O=CO2+8H+;
②100mL 1mol/L食盐水中含有氯化钠0.1mol,根据反应方程式2NaCl+2H2O
| ||
电解生成标况下2.24L氢气时,NaCl完全电解,生成0.1molNaOH,溶液体积为0.1L,则c(OH-)=1mol/L,c(H+)=10-14,所以PH=14,
故答案为:14;
③根据②的分析可知,电解过程中阳极生成了0.05mol氯气和0.025mol氧气,总共生成0.075mol气体,标准状况下阳极生成气体的体积为:22.4L/mol×0.075mol=1.68L,
故答案为:1.68.
看了雾霾天气肆虐给人类健康带来了严...的网友还看了以下:
甲、乙两列火车均长180米,如果两列火车相对行驶,后面的是:那么从车头相遇到车尾相离共需12s;如 2020-05-17 …
小敏同学以2米\秒的速度在货车车厢内行走,车厢长20米,当火车向前匀速运动时,下列说法正确的是:A 2020-05-21 …
客车和货车分别在两条平行的铁轨上行驶,客车长450米,货车长600米.如果两车相向而行,那么从两车 2020-05-21 …
一列快车长280米,一列慢车长200米,在平行轨道上行驶.若相向而行,从两车头相遇到两车尾相离,经 2020-06-22 …
数学思考题,高手来解答,悬赏多又多,乐趣享不尽!一列长150米的客车和一列180米长的货车错车而过 2020-06-30 …
一列快车长188米,一列慢车长212米,两车相向而行,从车头相遇到车尾离开需12秒.若同向而行,从 2020-07-26 …
甲乙两列火车均长180米,如果两列车相对行驶,从车头相遇的车尾相离共需12秒.如果两车同向行驶,则 2020-07-26 …
一列快车长280米,--列慢车长200米,在平行轨道上行驶,相向而行,从两车头相遇到两车尾相离,经 2020-07-26 …
当汽车尾气排放速度大于汽车行驶速度时,尾气对车的加速度是多少?当汽车以100km/h的速度匀速直线行 2020-11-01 …
客车和货车分别在两条平行的铁轨上行驶,客车厂150米,货车长250米.如果两车相向而行,那么从两车车 2020-11-30 …