早教吧作业答案频道 -->化学-->
A、B、C、D、E、F、G七种元素,它们的原子序数依次增大,除G外均为前20号元素.A原子基态时p能级原子轨道上电子数等于次外能层电子数,C元素的原子基态时s能级与p能级上的电子数相等,C
题目详情
A、B、C、D、E、F、G七种元素,它们的原子序数依次增大,除G外均为前20号元素.A原子基态时p能级原子轨道上电子数等于次外能层电子数,C元素的原子基态时s能级与p能级上的电子数相等,C、D处于相同的能级,且D是同期中电负性最大的元素,E原子的第一至第四电离能(kJ•mol-1)分别为:578、1817、2745、11575,F元素原子中4s能级有2个电子.G元素的离子形成的硫酸盐结晶水合物呈蓝色.
(1)B形成的单质中σ键和Π键的个数比为___,上述元素形成的化合物中和B的单质是等电子体的是___(填化学式)
(2)G元素的基态原子的电子排布式为___.
(3)常温下,E单质投入到B的最高价氧化物对应的水化物的浓溶液中的现象是___.
(4)D、F组成的晶体FD2结构如图Ⅰ所示,G形成晶体的结构如Ⅲ所示,Ⅱ为H3BO3(硼酸)晶体结构图(层状结构,层内的H3BO3分子通过氢键结合).
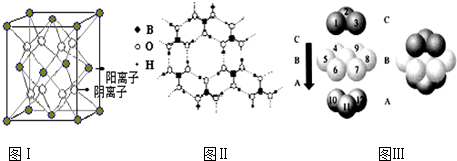
①图Ⅰ所示的FD2晶体中与F离子最近且等距离的F离子数为___,图Ⅲ中未标号的G原子形成晶体后周围最紧邻的G原子数为___;
②图Ⅱ所示的物质结构中最外能层已达8电子结构的原子是___(写元素符号),H3BO3晶体中B原子个数与极性键个数比为___;
③三种晶体中熔点高低的顺序为___(填化学式),H3BO3晶体受热熔化时,克服的微粒之间的相互作用为___.
(1)B形成的单质中σ键和Π键的个数比为___,上述元素形成的化合物中和B的单质是等电子体的是___(填化学式)
(2)G元素的基态原子的电子排布式为___.
(3)常温下,E单质投入到B的最高价氧化物对应的水化物的浓溶液中的现象是___.
(4)D、F组成的晶体FD2结构如图Ⅰ所示,G形成晶体的结构如Ⅲ所示,Ⅱ为H3BO3(硼酸)晶体结构图(层状结构,层内的H3BO3分子通过氢键结合).

①图Ⅰ所示的FD2晶体中与F离子最近且等距离的F离子数为___,图Ⅲ中未标号的G原子形成晶体后周围最紧邻的G原子数为___;
②图Ⅱ所示的物质结构中最外能层已达8电子结构的原子是___(写元素符号),H3BO3晶体中B原子个数与极性键个数比为___;
③三种晶体中熔点高低的顺序为___(填化学式),H3BO3晶体受热熔化时,克服的微粒之间的相互作用为___.
▼优质解答
答案和解析
由除G外均为前20号元素A原子基态时p能级原子轨道上电子数等于次外层电子数,则A的电子排布为1s22s22p2,即A为碳元素;C元素的原子基态时s能级与p能级上的电子数相等,则C的电子排布为1s22s22p4,则C为氧元素;
A、B、C原子序数依次增大,则B为氮元素;C、D有相同的能级,且D是同期中电负性最大的元素,则D为氟元素;
E原子的第一至第四电离能(kJ•mol-1)分别为:578、1817、2745、11575,即容易失去3个电子,则E为铝元素;
F元素原子中4s能级有2个电子,F的电子排布为1s22s22p63s22p64s2,则F为钙元素;G元素的离子形成的硫酸盐结晶水合物呈蓝色,则G为铜元素;
(1)B形成的单质为N2,N≡N中有2个π键、1个σ键,σ键和Π键的个数比为1:2;
氮气分子中的原子数为2,价电子数为10,而CO中的原子数为2,价电子数为4+6=10,则二者互为等电子体,
故答案为:1:2;CO;
(2)G为铜元素,原子序数为29,其基态电子排布为:1s22s22p63s22p63d104s1,
故答案为:1s22s22p63s23p63d104s1;
(3)因E为铝,B为氮元素,则常温下铝遇浓硝酸发生钝化,无明显现象,
故答案为:无明显现象(或钝化);
(4)①由图I可以看出晶体中与F离子最近且等距离的F离子数为:
=12;由图III中未标号的G原子形成晶体后周围最紧邻的G原子数为:3+6+3=12,
故答案为:12;12;
②图Ⅱ所示的物质结构中最外能层已达8电子结构的原子是O原子;硼酸分子中含有3个氧氢键极性键和3个B-O极性键,所以B原子与极性键的个数比为1:6,
故答案为:O;
③CaF2为离子晶体,Cu为金属晶体,H3BO3为分子晶体,离子晶体的熔点高,金属晶体熔点大于分子晶体、小于离子晶体,即熔点由高到低的排列顺序为:CaF2>Cu>H3BO3;H3BO3晶体中存在的作用力除共价键以外,分子和分子之间存在分子间作用力,有因氧的电负性大,分子之间存在氢键,
故答案为:CaF2>Cu>H3BO3;分子间作用力、氢键.
A、B、C原子序数依次增大,则B为氮元素;C、D有相同的能级,且D是同期中电负性最大的元素,则D为氟元素;
E原子的第一至第四电离能(kJ•mol-1)分别为:578、1817、2745、11575,即容易失去3个电子,则E为铝元素;
F元素原子中4s能级有2个电子,F的电子排布为1s22s22p63s22p64s2,则F为钙元素;G元素的离子形成的硫酸盐结晶水合物呈蓝色,则G为铜元素;
(1)B形成的单质为N2,N≡N中有2个π键、1个σ键,σ键和Π键的个数比为1:2;
氮气分子中的原子数为2,价电子数为10,而CO中的原子数为2,价电子数为4+6=10,则二者互为等电子体,
故答案为:1:2;CO;
(2)G为铜元素,原子序数为29,其基态电子排布为:1s22s22p63s22p63d104s1,
故答案为:1s22s22p63s23p63d104s1;
(3)因E为铝,B为氮元素,则常温下铝遇浓硝酸发生钝化,无明显现象,
故答案为:无明显现象(或钝化);
(4)①由图I可以看出晶体中与F离子最近且等距离的F离子数为:
| 3×8 |
| 2 |
故答案为:12;12;
②图Ⅱ所示的物质结构中最外能层已达8电子结构的原子是O原子;硼酸分子中含有3个氧氢键极性键和3个B-O极性键,所以B原子与极性键的个数比为1:6,
故答案为:O;
③CaF2为离子晶体,Cu为金属晶体,H3BO3为分子晶体,离子晶体的熔点高,金属晶体熔点大于分子晶体、小于离子晶体,即熔点由高到低的排列顺序为:CaF2>Cu>H3BO3;H3BO3晶体中存在的作用力除共价键以外,分子和分子之间存在分子间作用力,有因氧的电负性大,分子之间存在氢键,
故答案为:CaF2>Cu>H3BO3;分子间作用力、氢键.
看了A、B、C、D、E、F、G七种...的网友还看了以下:
概率论:随机事件A,C,满足P(A|A+C)+P(C|A+C)=1下列说法正确的是a,A、C不相容 2020-06-12 …
条件概率问题,已知P(A),P(B|A),P(C|A),能否求得P(C|A,B)?写错了,是已知P 2020-06-13 …
设C={A与B恰好发生一个},证明:P(C)=P(A)+P(B)—2P(AB) 2020-07-21 …
设事件ABC两两独P(A)=P(B)=P(C)=a,且ABC=空集,证明:a小于等于2/1 2020-07-22 …
P(C(A-B))=P(AC-BC)怎么推?P是概率符号就是事件A,B的差集与事件C的交集的概率, 2020-07-30 …
P(C(A-B))=P(AC-BC)怎么推?P是概率符号就是事件A,B的差集与事件C的交集的概率, 2020-07-30 …
p是q的什么条件(1)p:未位数是2的正整数,q:可以被2整除的整数(2)p:角A与角B是对顶角, 2020-07-30 …
请教三角形的几个己和恒等式的证明设I,O分别是三角形ABC的内心与外心,p为半周长,a、b、c为边 2020-08-03 …
P(A)=0,B为任一事件,则A.A是空集B.A是B的子集C.A与B相互独立D.A与B互不相容给的答 2020-11-03 …
条件概率公式中P(B∪C|A)=P(B|A)+P(C|A)中A、B、C分别表示什么?哪两个是互斥条件 2020-12-01 …