早教吧作业答案频道 -->化学-->
根据有关能量变化关系图,回答下列问题.(1)①根据图1A,写出反应的热化学方程式:.②根据如图1B所示情况,判断下列说法中正确的是.A.其热化学方程式为CO(g)+H2O(g)═CO2
题目详情
根据有关能量变化关系图,回答下列问题.
(1)①根据图1A,写出反应的热化学方程式:___.
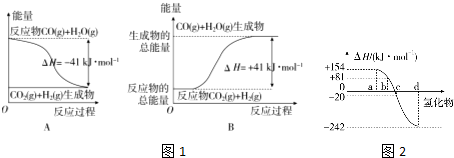
②根据如图1B所示情况,判断下列说法中正确的是___.
A.其热化学方程式为CO(g)+H2O(g)═CO2(g)+H2(g)△H=+41kJ•mol-1
B.该反应为吸热反应
C.该反应为放热反应
D.当H2O为液态时,其△H>+41kJ•mol-1
(2)已知16g固体硫完全燃烧时放出148.4kJ的热量,该反应的热化学方程式是___.
(3)如图2表示氧族元素中氧、硫、硒、碲生成氢化物时的焓变数据,根据焓变数据可确定a、b、c、d分别代表哪种元素.
①非金属元素氢化物的稳定性与氢化物生成热△H的关系为___.
②写出硒化氢发生分解反应的热化学方程式___.
(1)①根据图1A,写出反应的热化学方程式:___.

②根据如图1B所示情况,判断下列说法中正确的是___.
A.其热化学方程式为CO(g)+H2O(g)═CO2(g)+H2(g)△H=+41kJ•mol-1
B.该反应为吸热反应
C.该反应为放热反应
D.当H2O为液态时,其△H>+41kJ•mol-1
(2)已知16g固体硫完全燃烧时放出148.4kJ的热量,该反应的热化学方程式是___.
(3)如图2表示氧族元素中氧、硫、硒、碲生成氢化物时的焓变数据,根据焓变数据可确定a、b、c、d分别代表哪种元素.
①非金属元素氢化物的稳定性与氢化物生成热△H的关系为___.
②写出硒化氢发生分解反应的热化学方程式___.
▼优质解答
答案和解析
(1)图象分析可知为放热反应,反应的热化学方程式为:CO(g)+H2O(g)=CO2(g)+H2(g)△H=-41 kJ/mol,
故答案为:CO(g)+H2O(g)=CO2(g)+H2(g)△H=-41 kJ/mol;
②图象分析生成物能量高于反应物可知为吸热反应,则根据图象该反应的热化学方程式为:CO2(g)+H2(g)═CO(g)+H2O(g)△H=+41kJ/mol,
A.将反应的反应物与生成物弄反了,该反应的热化学方程式为:CO2(g)+H2(g)═CO(g)+H2O(g)△H=+41kJ/mol,故A错误;
B.生成物的能量比反应物的能量高,故该反应为吸热反应,故B正确;
C.生成物的能量比反应物的能量高,故该反应为吸热反应,故C错误;
D.因为气态水变成液态水还要放热,当H2O为液态时,其反应热值大于41kJ/mol,则△H<+41kJ•mol-1,故D错误;
故答案为:B;
(2)16g固体硫完全燃烧时放出148.4kJ的热量,则1molS完全燃烧时放出放出296.8kJ热量,则热化学方程式为:S(s)+O2(g)=SO2(g)△H=-296.8 kJ/mol,
故答案为:S(s)+O2(g)=SO2(g)△H=-296.8 kJ/mol;
(3)①非金属元素氢化物的稳定性与生成1mol氢化物时的△H的关系为:根据元素周期律,同一主族元素非金属性越强,生成气态氢化物越容易,气态氢化物越稳定,而能量越低越稳定,所以a、b、c、d依次为:H2Te、H2Se、H2S、H2O,
故答案为:非金属元素氢化物越稳定,△H越小,反之亦然;
②由①可知,b为硒化氢的生成热数据,则硒化氢分解吸热,△H=-81kJ/mol,所以H2Se发生分解反应的热化学反应方程式为:H2Se(g)=Se(s)+H2(g)△H=-81kJ/mol,
故答案为:H2Se(g)=Se(s)+H2(g)△H=-81kJ/mol.
故答案为:CO(g)+H2O(g)=CO2(g)+H2(g)△H=-41 kJ/mol;
②图象分析生成物能量高于反应物可知为吸热反应,则根据图象该反应的热化学方程式为:CO2(g)+H2(g)═CO(g)+H2O(g)△H=+41kJ/mol,
A.将反应的反应物与生成物弄反了,该反应的热化学方程式为:CO2(g)+H2(g)═CO(g)+H2O(g)△H=+41kJ/mol,故A错误;
B.生成物的能量比反应物的能量高,故该反应为吸热反应,故B正确;
C.生成物的能量比反应物的能量高,故该反应为吸热反应,故C错误;
D.因为气态水变成液态水还要放热,当H2O为液态时,其反应热值大于41kJ/mol,则△H<+41kJ•mol-1,故D错误;
故答案为:B;
(2)16g固体硫完全燃烧时放出148.4kJ的热量,则1molS完全燃烧时放出放出296.8kJ热量,则热化学方程式为:S(s)+O2(g)=SO2(g)△H=-296.8 kJ/mol,
故答案为:S(s)+O2(g)=SO2(g)△H=-296.8 kJ/mol;
(3)①非金属元素氢化物的稳定性与生成1mol氢化物时的△H的关系为:根据元素周期律,同一主族元素非金属性越强,生成气态氢化物越容易,气态氢化物越稳定,而能量越低越稳定,所以a、b、c、d依次为:H2Te、H2Se、H2S、H2O,
故答案为:非金属元素氢化物越稳定,△H越小,反之亦然;
②由①可知,b为硒化氢的生成热数据,则硒化氢分解吸热,△H=-81kJ/mol,所以H2Se发生分解反应的热化学反应方程式为:H2Se(g)=Se(s)+H2(g)△H=-81kJ/mol,
故答案为:H2Se(g)=Se(s)+H2(g)△H=-81kJ/mol.
看了根据有关能量变化关系图,回答下...的网友还看了以下:
解释在光谱化学序列中为什么OH-的八面体配合物分离能小于相应水合物的分裂能?(光谱化学序列中为什么是 2020-03-30 …
.有A、B两种配合物,化学式为CoCl3.5NH3.H2O,试根据以下实验结果,确定它们的配离子, 2020-07-03 …
实验室可以用乙醇和浓硫酸在170℃制乙烯,化学反应原理:CH3CH2OH浓硫酸170℃CH2=CH 2020-07-18 …
某校化学研究性学习小组通过实验研究高炉炼铁的化学原理,设计了如图1实验装置:(1)已知HCOOH浓 2020-07-24 …
(2014•扬州)某校化学研究性学习小组通过实验研究高炉炼铁的化学原理,设计了如图1实验装置:(1 2020-07-24 …
水煤气是由煤(C)和水蒸气(H2O)在高温下制取.某同学根据质量守恒定律猜测水煤气的成分,并对其所含 2020-11-02 …
实验室可以用乙醇和浓硫酸在170℃制乙烯,化学反应原理:CH3CH2OHCH2=CH2↑+H2O,由 2020-11-23 …
水是地球上最普通、最常见的物质之一,不仅江河湖海中含有水,各种生物体内也都含有水.生命的孕育和维系需 2020-12-02 …
某反应体系的物质有:NaOH、Au2O3、Na2S4O6、Na2S2O3、Au2O、H2O.下列选项 2020-12-25 …
在常温下,下列五种溶液:①0.1mol/LNH4Cl②0.1mol/LCH3COONH4③0.1mo 2021-02-01 …