早教吧作业答案频道 -->化学-->
参考如图和有关要求回答问题:(1)甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的一种原理是CH3OH(g)和H2O(g)反应生成CO2和H2.图1是该过程中能量变化示意图,若在反应体系中加
题目详情
参考如图和有关要求回答问题:
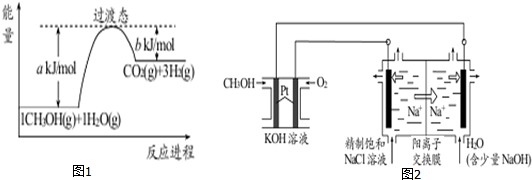
(1)甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的一种原理是CH3OH(g)和H2O(g)反应生成CO2和H2.图1是该过程中能量变化示意图,若在反应体系中加入催化剂,反应速率增大,正反应活化能 a的变化是___ (填“增大”、“减小”、“不变”),反应热△H的变化是___(填“增大”、“减小”、“不变”).
(2)以CH3OH燃料电池为电源电解法制取ClO2.二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂.
①CH3OH燃料电池放电过程中,通入O2的电极附近溶液的pH___(填“增大”、“减小”、“不变”).负极反应式为___.
②图2中电解池用石墨作电极,在一定条件下电解饱和食盐水制取 ClO2.阳极产生 ClO2的反应式为___.
③电解一段时间,从阴极处收集到的气体比阳极处收集到气体多 6.72L时(标准状况,忽略生成的气体溶解),停止电解,通过阳离子交换膜的阳离子为___mol.
(3)图2中电解池改为用石墨作电极,在一定条件下电解0.05mol•L-1的硫酸铜溶液200ml,当两极产生的气体体积相同时,
①发生电解的总反应方程式为___
②若电解后溶液的体积还是200ml,溶液的pH=___
③电解后加入下列___固体物质可使溶液恢复到电解前
A CuO B Cu (OH)2C CuCO3D CuSO4.

(1)甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的一种原理是CH3OH(g)和H2O(g)反应生成CO2和H2.图1是该过程中能量变化示意图,若在反应体系中加入催化剂,反应速率增大,正反应活化能 a的变化是___ (填“增大”、“减小”、“不变”),反应热△H的变化是___(填“增大”、“减小”、“不变”).
(2)以CH3OH燃料电池为电源电解法制取ClO2.二氧化氯(ClO2)为一种黄绿色气体,是国际上公认的高效、广谱、快速、安全的杀菌消毒剂.
①CH3OH燃料电池放电过程中,通入O2的电极附近溶液的pH___(填“增大”、“减小”、“不变”).负极反应式为___.
②图2中电解池用石墨作电极,在一定条件下电解饱和食盐水制取 ClO2.阳极产生 ClO2的反应式为___.
③电解一段时间,从阴极处收集到的气体比阳极处收集到气体多 6.72L时(标准状况,忽略生成的气体溶解),停止电解,通过阳离子交换膜的阳离子为___mol.
(3)图2中电解池改为用石墨作电极,在一定条件下电解0.05mol•L-1的硫酸铜溶液200ml,当两极产生的气体体积相同时,
①发生电解的总反应方程式为___
②若电解后溶液的体积还是200ml,溶液的pH=___
③电解后加入下列___固体物质可使溶液恢复到电解前
A CuO B Cu (OH)2C CuCO3D CuSO4.
▼优质解答
答案和解析
(1)催化剂降低反应的活化能,加快反应速率,即a减小,但催化剂不能改变活化能,即反应热△H不变,反应能量图中生成物的总能量大于反应物的总能量,则为吸热反应,由图可知,1mol 甲醇和1mol 水蒸气反应生成CO2和氢气吸收的热量为(a-b)kJ,反应热化学方程式为:CH3OH(g)+H2O(g)=CO2(g)+3H2(g)△H=+(a-b)kJ/mol,
故答案为:减小;不变;CH3OH(g)+H2O(g)=CO2(g)+3H2(g)△H=+(a-b)kJ/mol;
(2)①CH3OH燃料电池放电过程中,通入O2的电极是正极,氧气得到电子转化为氢氧根,则附近溶液的pH增大,
故答案为:增大;
②电解池中阳极失去电子,则阳极氯离子放电,产生ClO2的反应式为:Cl--5e-+2H2O=4H++ClO2↑,
故答案为:Cl--5e-+2H2O=4H++ClO2↑;
③电解一段时间,从阴极处收集到的气体比阳极处收集到气体多 6.72L时(标准状况,忽略生成的气体溶解),多出的气体是氢气,物质的量=
=0.3mol,设阳极产生的气体是xmol,则根据电子得失守恒可知5x=(0.3+x)×2,解得x=0.2,即转移1mol电子,钠离子通过阳离子交换膜,所以通过阳离子交换膜的阳离子为1mol,
故答案为:1;
(3)①电解总反应式为2CuSO4+2H20
2Cu+2H2SO4+O2↑,故答案为:2CuSO4+2H20
2Cu+2H2SO4+O2↑;
②电解硫酸铜溶液0.01mol,阴极上发生反应:Cu2++2e-═Cu,2H++2e-═H2↑,0.01mol铜离子得电子转移0.02mol电子,若产生224mL即0.01mol气体,转移电子是0.022mol,共0.04mol电子转移,阳极上发生反应4OH--4e-═2H2O+O2↑,产生相同气体,若为224mL即0.01mol气体,转移电子的物质的量是0.04mol,根据反应式:2CuSO4+2H20
2Cu+2H2SO4+O2↑,当生成0.01mol铜,生成硫酸是0.01mol,所以氢离子浓度是
=0.1mol/L,所以pH=1;故答案为:1;
③电解过程中少什么加什么,少多少加多少,根反应式:阴极上发生反应:Cu2++2e-═Cu,2H++2e-═H2↑,阳极上发生反应4OH--4e-═2H2O+O2↑,析出了铜,跑掉了氧气和氢气,故选B.
故答案为:减小;不变;CH3OH(g)+H2O(g)=CO2(g)+3H2(g)△H=+(a-b)kJ/mol;
(2)①CH3OH燃料电池放电过程中,通入O2的电极是正极,氧气得到电子转化为氢氧根,则附近溶液的pH增大,
故答案为:增大;
②电解池中阳极失去电子,则阳极氯离子放电,产生ClO2的反应式为:Cl--5e-+2H2O=4H++ClO2↑,
故答案为:Cl--5e-+2H2O=4H++ClO2↑;
③电解一段时间,从阴极处收集到的气体比阳极处收集到气体多 6.72L时(标准状况,忽略生成的气体溶解),多出的气体是氢气,物质的量=
| 6.72L |
| 22.4L/mol |
故答案为:1;
(3)①电解总反应式为2CuSO4+2H20
| ||
| ||
②电解硫酸铜溶液0.01mol,阴极上发生反应:Cu2++2e-═Cu,2H++2e-═H2↑,0.01mol铜离子得电子转移0.02mol电子,若产生224mL即0.01mol气体,转移电子是0.022mol,共0.04mol电子转移,阳极上发生反应4OH--4e-═2H2O+O2↑,产生相同气体,若为224mL即0.01mol气体,转移电子的物质的量是0.04mol,根据反应式:2CuSO4+2H20
| ||
| 0.01mol×2 |
| 0.2L |
③电解过程中少什么加什么,少多少加多少,根反应式:阴极上发生反应:Cu2++2e-═Cu,2H++2e-═H2↑,阳极上发生反应4OH--4e-═2H2O+O2↑,析出了铜,跑掉了氧气和氢气,故选B.
看了参考如图和有关要求回答问题:(...的网友还看了以下:
英语翻译鞍钢年产80万吨焦炭焦炉的设计摘 要随着钢铁行业等重工业的发展,炼焦行业也迅速发展,焦炭产 2020-05-15 …
汽车烧甲醇 天然气甲醇和煤制甲醇那个好一点 2020-05-16 …
在标准状况下,由甲烷、甲醛和乙烷组成的11.2升混合气体完全燃烧后,生成0.7mol二氧化碳气体. 2020-05-16 …
有一混合气体,经测定其中只有甲烷和一氧化碳,现将3.0克该混合气体氧气中燃烧,测得生成6.6克二氧 2020-05-16 …
月球是地球上唯一的天然()星.月球上(),造成月球上昼夜温差大.()传声,无天气变化和四季变化,月 2020-06-04 …
从全球来讲,大气环流把热量和水汽从一个地区输送到另一个地区,使高低纬度之间、海陆之间的热量和水分得 2020-07-01 …
有一种气体,可能由氢气,甲烷,和二氧化碳三种气体中的一种或几种组成,为证明该物体的组成 2020-07-22 …
甲烷自热重整是先进的制氢方法,包含甲烷氧化和蒸气重整.向反应系统同时通入甲烷、氧气和水蒸气,发生的 2020-07-22 …
(1)工业上可利用“甲烷蒸气转化法”生产氢气,反应为甲烷和水蒸气在高温和催化剂存在的条件下生成一氧化 2020-11-04 …
有关煤的综合利用下列说法正确的是()A.煤和水煤气均是二次能源B.煤的干馏为化学变化,煤的液化和气化 2020-11-16 …