早教吧作业答案频道 -->化学-->
硝酸钱可用作化肥、军用炸药、杀虫剂、冷冻剂等,工业制取硝酸钱的工艺流程如图1:(l)合成氨气的工业设备名称是,设备中设置热交换器的目的是,合成氨的原料气必须先脱硫,
题目详情
硝酸钱可用作化肥、军用炸药、杀虫剂、冷冻剂等,工业制取硝酸钱的工艺流程如图1:
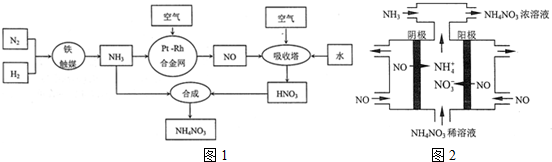
(l)合成氨气的工业设备名称是___,设备中设置热交换器的目的是___,合成氨的原料气必须先脱硫,目的是___
(2)吸收塔中反应的化学方程式为___从生产流程看,吸收塔中需要补充空气,其原因是___
(3)生产硝酸的过程中常会产生氮的氧化物,可用如下三种方法处理:
方法一:碱性溶液吸收法
NO+NO2+2NaOH=2NaNO2+H2O;
2NO2+N2CO3=NaNO2+NaNO3+CO2
方法二:NH3还原法
8NH3(g)+6NO2(g)═7N2(g)+12H2O(g)△H=-2635kJ.mol-1(NO也有类似的反应)
方法三:甲烷吸收法
CH4(g)+2NO2(g)═CO2(g)+N2(g)+2H2O(g)△H=+867kJ.mol-1(NO也有类似的反应)
上述三种方法中,方法一的主要缺点是___
方法三和方法二相比,方法三的缺点是___
(4)工业上也可以通过电解NO制备NH4N03,其工作原理如图2所示.
①图中通入NH3的目的是___
②若维持电流强度为3A,电解2小时,理论上可制得NH4NO3的最大质量为___g.(已知F=96500C•mol一l)
(5)某化肥厂用NH3制备NH4NO3.己知:NH3制NO的产率是94%,NO制HNO3的产率是89%,则制HNO3所用NH3的质量占总耗NH3质量(不考虑其他损耗)的百分比为___.

(l)合成氨气的工业设备名称是___,设备中设置热交换器的目的是___,合成氨的原料气必须先脱硫,目的是___
(2)吸收塔中反应的化学方程式为___从生产流程看,吸收塔中需要补充空气,其原因是___
(3)生产硝酸的过程中常会产生氮的氧化物,可用如下三种方法处理:
方法一:碱性溶液吸收法
NO+NO2+2NaOH=2NaNO2+H2O;
2NO2+N2CO3=NaNO2+NaNO3+CO2
方法二:NH3还原法
8NH3(g)+6NO2(g)═7N2(g)+12H2O(g)△H=-2635kJ.mol-1(NO也有类似的反应)
方法三:甲烷吸收法
CH4(g)+2NO2(g)═CO2(g)+N2(g)+2H2O(g)△H=+867kJ.mol-1(NO也有类似的反应)
上述三种方法中,方法一的主要缺点是___
方法三和方法二相比,方法三的缺点是___
(4)工业上也可以通过电解NO制备NH4N03,其工作原理如图2所示.
①图中通入NH3的目的是___
②若维持电流强度为3A,电解2小时,理论上可制得NH4NO3的最大质量为___g.(已知F=96500C•mol一l)
(5)某化肥厂用NH3制备NH4NO3.己知:NH3制NO的产率是94%,NO制HNO3的产率是89%,则制HNO3所用NH3的质量占总耗NH3质量(不考虑其他损耗)的百分比为___.
▼优质解答
答案和解析
(1)合成氨的工业设备是合成塔;合成氨的反应属于放热反应,反应过程中会放出大量的热,用热交换器可以充分利用余热,节约能源;N2与H2合成NH3,生产中原料气必须进行脱硫可以防止催化剂中毒;
故答案为:合成塔;充分利用热能,节约能源;防止催化剂中毒;
(2)在吸收塔中二氧化氮与水反应生成硝酸和NO,通入空气,NO能被空气中的氧气氧化为二氧化氮,二氧化氮再与水反应生成硝酸,这样使NO循环利用,全部转化为硝酸,反应的化学方程式为4NO+3O2+2H2O=4HNO3;
故答案为:4NO+3O2+2H2O=4HNO3;可使NO循环利用,提高原料利用率;
(3)方法一最大的缺点是单独的NO不能被吸收,只能与NO2一起被碱液吸收;方法三和方法二相比,优点是甲烷比氨价格便宜,节约成本;缺点是方法三的反应热为+867kJ•mol-1,耗能较高;
故答案为:单独的NO不能被吸收;耗能高;
(4)①电解NO制备NH4NO3,阳极反应为NO-3e-+2H2O=NO3-+4H+,阴极反应为:NO+5e-+6H+=NH4++H2O,从两极反应可看出,要使得失电子守恒,阳极产生的NO3-的物质的量大于阴极产生的NH4+的物质的量,总反应方程式为:8NO+7H2O
3NH4NO3+2HNO3,因此补充NH3,使电解产物全部转化为NH4NO3,
故答案为:使电解产物全部转化为NH4NO3;
②维持电流强度为3A,电解2小时,时间为7200S,F=96500C•mol-1,Q=It=3.0C/s×7200S,则理论上可制得NH4NO3的最大质量为
×80g/mol=6.0g
故答案为:6.0;
(5)由NH3制NO的产率是94%、NO制HNO3的产率是89%,根据氮原子守恒可知,NH3~NO~HNO3,则1mol氨气可得到硝酸1mol×94%×89%=0.8366mol,由HNO3+NH3═NH4NO3,则该反应消耗的氨气的物质的量为0.8366mol,氨气的质量之比等于物质的量之比,则制HNO3所用去的NH3的质量占总耗NH3质量的百分数为
×100%=54.4%;即制HNO3所用去的NH3的质量占总耗NH3质量的54.4%,
故答案为:54.4%.
故答案为:合成塔;充分利用热能,节约能源;防止催化剂中毒;
(2)在吸收塔中二氧化氮与水反应生成硝酸和NO,通入空气,NO能被空气中的氧气氧化为二氧化氮,二氧化氮再与水反应生成硝酸,这样使NO循环利用,全部转化为硝酸,反应的化学方程式为4NO+3O2+2H2O=4HNO3;
故答案为:4NO+3O2+2H2O=4HNO3;可使NO循环利用,提高原料利用率;
(3)方法一最大的缺点是单独的NO不能被吸收,只能与NO2一起被碱液吸收;方法三和方法二相比,优点是甲烷比氨价格便宜,节约成本;缺点是方法三的反应热为+867kJ•mol-1,耗能较高;
故答案为:单独的NO不能被吸收;耗能高;
(4)①电解NO制备NH4NO3,阳极反应为NO-3e-+2H2O=NO3-+4H+,阴极反应为:NO+5e-+6H+=NH4++H2O,从两极反应可看出,要使得失电子守恒,阳极产生的NO3-的物质的量大于阴极产生的NH4+的物质的量,总反应方程式为:8NO+7H2O
| ||
故答案为:使电解产物全部转化为NH4NO3;
②维持电流强度为3A,电解2小时,时间为7200S,F=96500C•mol-1,Q=It=3.0C/s×7200S,则理论上可制得NH4NO3的最大质量为
| 3.0C/S×7200S | ||
|
故答案为:6.0;
(5)由NH3制NO的产率是94%、NO制HNO3的产率是89%,根据氮原子守恒可知,NH3~NO~HNO3,则1mol氨气可得到硝酸1mol×94%×89%=0.8366mol,由HNO3+NH3═NH4NO3,则该反应消耗的氨气的物质的量为0.8366mol,氨气的质量之比等于物质的量之比,则制HNO3所用去的NH3的质量占总耗NH3质量的百分数为
| 1mol |
| 1mol+0.8366mol |
故答案为:54.4%.
看了硝酸钱可用作化肥、军用炸药、杀...的网友还看了以下:
哪些金属氟化物可溶?难溶?工业合成氨中1.注入过量氮气2.加催化剂这两种方法哪个可以提高氨的产量, 2020-04-25 …
工业上用氨催化氧化法可生产硝酸,其生产过程可表示为:4NH3+5O2催化剂.△4NO2+6H2O① 2020-06-30 …
氨对人类的生产生活具有重要影响.(1)氨的制备与利用.①工业合成氨的化学方程式是.②氨催化氧化生成 2020-07-03 …
合成氨是化学科学对人类社会发展与进步作出巨大贡献的典例之一,合成氨工业包括原料气的制备、净化、氨的合 2020-11-04 …
氨是生产硝酸、尿素等物质的重要原料,工业合成氨是最重要的化工生产之一.(1)氨催化氧化法是工业制硝酸 2020-11-04 …
氨对人类的生产生活具有重要影响.(1)氨的制备与利用.①工业合成氨的化学方程式是.②氨催化氧化生成一 2020-11-05 …
(2009•宿迁模拟)工业合成氨与制备硝酸一般可连续生产,流程如图1:在800℃、铂催化剂存在条件下 2020-11-12 …
(2010•南通模拟)合成氨是人类科学技术发展史上的一项重大突破,目前工业上用氢气和氮气直接合成氨, 2020-11-12 …
以化学平衡移动原理为依据,解释以下事实:(1)在氨水中加入氢氧化钠固体,有氨气逸出。(2)合成氨工业 2020-12-01 …
工业合成氨可以实现大规模固氮,氨可用于生产氯化铵、硫酸铵等化学肥料.(1)等物质的量浓度的两溶液,p 2020-12-14 …