早教吧作业答案频道 -->化学-->
氨气是一种重要的化工产品,在生产和科研中应用广泛,氨气是工业合成氨的原料之一,工业上制取氨气有下列两种途径:途径一、用水和天然气作原料一步反应制得途径二,用煤和水作原
题目详情
氨气是一种重要的化工产品,在生产和科研中应用广泛,氨气是工业合成氨的原料之一,工业上制取氨气有下列两种途径:
途径一、用水和天然气作原料一步反应制得
途径二,用煤和水作原料经多步反应制得.
请回答下列问题:
(1)途径一反应的还原产物是___
(2)途径二中的一步反应为:CO(g)+H2O(g)⇌CO2(g)+H2(g)△H<0
①上述反应达到平衡后,为提高CO的转化率,下列措施中正确的是___(填写序号)
A.增大压强B.降低温度C.增大H2O(g)的浓度D.使用催化剂
②已知1000K时,上述反应的平衡常数K=0.627,若要使CO的转化率超过90%,则起始无中c(H2O):c(CO)不低于___.
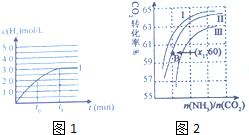
③在容积为2L的容器中发生上述反应,测得c(H)2与反应时间t的变化曲线Ⅰ如图1所示,若在t0时刻将容器的体积扩大至4L,请在答题卡图中绘出c(H2)与反应时间变化的曲线Ⅱ
(3)目前常用氨气处理硝酸生产的工业尾气,在400℃左右且有催化剂存在的情况下,氨气能把NO(g)还原成无色无毒气体,直接排入空气中,已知氢气的燃烧热为286kJ•mol-1
N2(g)+3H2(g)⇌2NH3(g)△H=-92.4kJ•mol-1
N2(g)+O2(g)⇌2NO(g)△H=+180kJ•mol-1
试写出氨气与NO(g)反应生成五毒气体和液态水的热化学方程式___
(4)工业上用氨和二氧化碳反应合成尿素,其反应为:2NH3(g)+CO2(g)⇌CO(NH2)2(l)+H2O(g)生成过程中,原料原料气常混有水蒸气,CO2的转化率与氨碳比
、水碳比
的变化关系如图所示
①曲线Ⅰ、Ⅱ、Ⅲ对应的水碳比最小的是___.
②若B点氨的转化率为60%,则x1=___.
(5)某同学将NH3和CO2按物质的量之比2:1通入水中,充分反应所得溶液中NH
、CO
、HCO
三种离子浓度由大到小的顺序是___(已知:氨水、碳酸的电离平衡常数如表)
途径一、用水和天然气作原料一步反应制得
途径二,用煤和水作原料经多步反应制得.
请回答下列问题:

(1)途径一反应的还原产物是___
(2)途径二中的一步反应为:CO(g)+H2O(g)⇌CO2(g)+H2(g)△H<0
①上述反应达到平衡后,为提高CO的转化率,下列措施中正确的是___(填写序号)
A.增大压强B.降低温度C.增大H2O(g)的浓度D.使用催化剂
②已知1000K时,上述反应的平衡常数K=0.627,若要使CO的转化率超过90%,则起始无中c(H2O):c(CO)不低于___.
③在容积为2L的容器中发生上述反应,测得c(H)2与反应时间t的变化曲线Ⅰ如图1所示,若在t0时刻将容器的体积扩大至4L,请在答题卡图中绘出c(H2)与反应时间变化的曲线Ⅱ
(3)目前常用氨气处理硝酸生产的工业尾气,在400℃左右且有催化剂存在的情况下,氨气能把NO(g)还原成无色无毒气体,直接排入空气中,已知氢气的燃烧热为286kJ•mol-1
N2(g)+3H2(g)⇌2NH3(g)△H=-92.4kJ•mol-1
N2(g)+O2(g)⇌2NO(g)△H=+180kJ•mol-1
试写出氨气与NO(g)反应生成五毒气体和液态水的热化学方程式___
(4)工业上用氨和二氧化碳反应合成尿素,其反应为:2NH3(g)+CO2(g)⇌CO(NH2)2(l)+H2O(g)生成过程中,原料原料气常混有水蒸气,CO2的转化率与氨碳比
| n(NH3) |
| n(CO2) |
| n(H2O) |
| n(CO2) |
①曲线Ⅰ、Ⅱ、Ⅲ对应的水碳比最小的是___.
②若B点氨的转化率为60%,则x1=___.
(5)某同学将NH3和CO2按物质的量之比2:1通入水中,充分反应所得溶液中NH
| + 4 |
| 2- 3 |
| - 3 |
| 弱电解质 | 化学式 | 电离常数(K) |
| 氨水 | NH3•H2O | 1.79×10-5 |
| 碳酸 | H2CO3 | K1=4.30×10-7 |
| K2=5.61×10-11 |
▼优质解答
答案和解析
(1)途径一是用水和天然气作原料一步反应制得氢气,氢的化合价降低,氢气作还原产物,故答案为:氢气;
(2)①提高CO的转化率可以让平衡正向进行即可:
A.增加压强,该平衡不会发生移动,故A错误;
B.降低温度,化学平衡向着放热方向即正向进行,故B正确;
C.增大水蒸气的浓度,化学平衡向着正方向进行,故C正确;
D.催化剂不会引起化学平衡的移动,故D错误;
故答案为:BC;
②设CO的起始浓度为xmol,H2O的起始浓度为ymol,则转化的CO的最小值为0.9x,
CO(g)+H2O(g)⇌CO2(g)+H2(g)
起始 x y 0 0
变化 0.9x 0.9x 0.9x 0.9x
平衡 0.1x y-0.9x 0.9x 0.9x
根据平衡常数列式:
=0.627,
解得:
=13.8,故此只要此值大于13.8,转化率就会超过90%,
故答案为:13.8;
③体积增大2倍,浓度缩小2倍,压强变小,但压强对CO(g)+H2O(g)⇌CO2(g)+H2(g)的平衡无影响,所以达平衡时,氢气的浓度是原平衡的一半,则c(H2)与反应时间变化的曲线Ⅱ: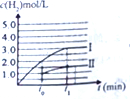 ;故答案为:
;故答案为: ;
;
(3)氢气的燃烧热为286kJ•mol-1,则氢气的燃烧的热化学方程式为:
H2(g)+
O2(g)=H2O(l)△H=-286kJ•mol-1①
N2(g)+3H2(g)⇌2NH3(g)△H=-92.4kJ•mol-1②
N2(g)+O2(g)⇌2NO(g)△H=+180kJ•mol-1③
根据盖斯定律①×6-②×2-③×3得4NH3(g)+6NO(g)═5N2(g)+6H2O(l)△H=-2071.2kJ•mol-1,
故答案为:4NH3(g)+6NO(g)═5N2(g)+6H2O(l)△H=-2071.2kJ•mol-1;
(4)①根据图2可知,氨碳比一定时,水碳比越大,说明原料气中含二氧化碳越少,二氧化碳的转化率越低,所以二氧化碳转化率最低的即为水碳比最大的,则曲线Ⅰ、Ⅱ、Ⅲ对应的水碳比最小的是Ⅰ曲线,故答案为:Ⅰ;
②B点二氧化碳的转化率为60%,氨气的转化率是60%,
设NH3、CO2的起始物质的量分别为x、y,
则:x×60%×
=y×60%,
解得:
=x1=2,
故答案为:2;
(5)将NH3和CO2按物质的量之比2:1通入水中,生成碳酸铵溶液,铵根和碳酸根都水解,铵根的水解平衡常数Kh=
=
,碳酸根的水解平衡常数Kh=
=
,则碳酸根的水解程度大,铵根的水解程度小,溶液中的铵根浓度大于碳酸根,水解是弱水解,碳酸根的浓度大于碳酸氢根,则离子浓度大小关系为:c(NH4+)>c(CO32-)>c(HCO3-),故答案为:c(NH4+)>c(CO32-)>c(HCO3-).
(2)①提高CO的转化率可以让平衡正向进行即可:
A.增加压强,该平衡不会发生移动,故A错误;
B.降低温度,化学平衡向着放热方向即正向进行,故B正确;
C.增大水蒸气的浓度,化学平衡向着正方向进行,故C正确;
D.催化剂不会引起化学平衡的移动,故D错误;
故答案为:BC;
②设CO的起始浓度为xmol,H2O的起始浓度为ymol,则转化的CO的最小值为0.9x,
CO(g)+H2O(g)⇌CO2(g)+H2(g)
起始 x y 0 0
变化 0.9x 0.9x 0.9x 0.9x
平衡 0.1x y-0.9x 0.9x 0.9x
根据平衡常数列式:
| (0.9x)2 |
| 0.1x×(y-0.9x) |
解得:
| y |
| x |
故答案为:13.8;
③体积增大2倍,浓度缩小2倍,压强变小,但压强对CO(g)+H2O(g)⇌CO2(g)+H2(g)的平衡无影响,所以达平衡时,氢气的浓度是原平衡的一半,则c(H2)与反应时间变化的曲线Ⅱ:
 ;故答案为:
;故答案为: ;
;(3)氢气的燃烧热为286kJ•mol-1,则氢气的燃烧的热化学方程式为:
H2(g)+
| 1 |
| 2 |
N2(g)+3H2(g)⇌2NH3(g)△H=-92.4kJ•mol-1②
N2(g)+O2(g)⇌2NO(g)△H=+180kJ•mol-1③
根据盖斯定律①×6-②×2-③×3得4NH3(g)+6NO(g)═5N2(g)+6H2O(l)△H=-2071.2kJ•mol-1,
故答案为:4NH3(g)+6NO(g)═5N2(g)+6H2O(l)△H=-2071.2kJ•mol-1;
(4)①根据图2可知,氨碳比一定时,水碳比越大,说明原料气中含二氧化碳越少,二氧化碳的转化率越低,所以二氧化碳转化率最低的即为水碳比最大的,则曲线Ⅰ、Ⅱ、Ⅲ对应的水碳比最小的是Ⅰ曲线,故答案为:Ⅰ;
②B点二氧化碳的转化率为60%,氨气的转化率是60%,
设NH3、CO2的起始物质的量分别为x、y,
则:x×60%×
| 1 |
| 2 |
解得:
| x |
| y |
故答案为:2;
(5)将NH3和CO2按物质的量之比2:1通入水中,生成碳酸铵溶液,铵根和碳酸根都水解,铵根的水解平衡常数Kh=
| KW |
| Ka |
| 10-14 |
| 1.79×10-5 |
| KW |
| Ka2 |
| 10-14 |
| 5.61×10-11 |
看了氨气是一种重要的化工产品,在生...的网友还看了以下:
我们学过有六种途径可以制得氧气,如图所示:(1)写出途径B制得氧气的反应化学方程式:2KMnO4△ 2020-05-02 …
我们学过有六种途径可制得氧气,如图所示:(1)写出途径B的文字表达式并注明基本反应类型.B:;.( 2020-05-14 …
制取气体发生装置智取气体的发生装置两种,一种是固体和液体接触及反应的制气装置,一种是------- 2020-05-24 …
通过学习化学,我们知道了多种途径可以制取氧气.如:A.电解水B.分离空气C.加热高猛酸钾D.分解过 2020-06-27 …
(1)我们知道有多种途径可以获得氧气.如:A.电解水B.分离液态空气C.加热高锰酸钾D.分解过氧化 2020-07-22 …
以铜、硫酸、水、空气等为原料,可用多种方法制取CuSO4.(1)试设计两种制取CuSO4的途径(用 2020-08-01 …
利用下列四种途径都可以获得氧气.(1)途径甲和乙均要用到同一种辅助试剂A.A是(填化学式),但实验室 2020-11-29 …
通过化学学习,应该知道有多种途径可以制取氧气.如:A.电解水B.分离空气C.加热高锰酸钾D.分解过氧 2020-12-20 …
一种充气式的圆柱形柱子,充气后底面,直径是0.5m,高3m。它的底是用黄色布,侧面是用红色布做成一种 2021-01-13 …
实验室用氯化铵和消石灰制氨气的装置和下列哪种制气装置相同()A.加热高锰酸钾制O2B.石灰石和稀盐酸 2021-02-08 …