早教吧作业答案频道 -->化学-->
钼酸钠晶体(Na2MoO4•2H2O)是一种无公害型冷却水系统的金属缓蚀剂.工业上利用钼精矿(主要成分是不溶于水的MoS2)制备钼酸钠的两种途径如图1所示:(1)NaClO的电子式是.(2)为了
题目详情
钼酸钠晶体( Na2MoO4•2H2O)是一种无公害型冷却水系统的金属缓蚀剂.工业上利用钼精矿(主要成分是不溶于水的MoS2)制备钼酸钠的两种途径如图1所示:
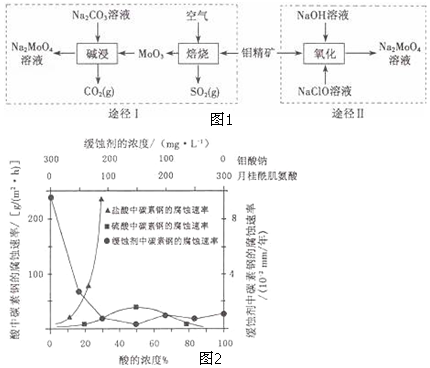
(1)NaClO的电子式是___.
(2)为了提高焙烧效率,除增大空气量外还可以采用的措施是___.
(3)途径I碱浸时发生反应的离子方程式为___.
(4)途径Ⅱ氧化时发生反应的离子方程式为___.
(5)钼酸钠和月桂酰肌氨酸的混合液常作为碳素钢的缓蚀剂.常温下,碳素钢在三种不同介质中的腐蚀速率实验结果如图2:
①要使碳素钢的缓蚀效果最优,钼酸钠和月桂酰肌氨酸的浓度比应为___.
②当硫酸的浓度大于90%时,腐蚀速率几乎为零,原因是___.
③试分析随着盐酸和硫酸浓度的增大,碳素钢在两者中腐蚀速率产生明显差异的主要原因是___.

(1)NaClO的电子式是___.
(2)为了提高焙烧效率,除增大空气量外还可以采用的措施是___.
(3)途径I碱浸时发生反应的离子方程式为___.
(4)途径Ⅱ氧化时发生反应的离子方程式为___.
(5)钼酸钠和月桂酰肌氨酸的混合液常作为碳素钢的缓蚀剂.常温下,碳素钢在三种不同介质中的腐蚀速率实验结果如图2:
①要使碳素钢的缓蚀效果最优,钼酸钠和月桂酰肌氨酸的浓度比应为___.
②当硫酸的浓度大于90%时,腐蚀速率几乎为零,原因是___.
③试分析随着盐酸和硫酸浓度的增大,碳素钢在两者中腐蚀速率产生明显差异的主要原因是___.
▼优质解答
答案和解析
(1)离子化合物NaClO的电子式为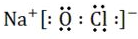 ,故答案为:
,故答案为: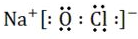 ;
;
(2)提高焙烧效率,除增大空气量外还可以采用的措施是充分粉碎或逆流焙烧,故答案为:充分粉碎或逆流焙烧;
(3)途径I碱浸时发生反应的离子方程式为MoO3+CO32-=MnO42-+CO2↑,故答案为:MoO3+CO32-=MoO42-+CO2↑;
(4)途径Ⅱ用NaClO在碱性条件下氧化MoO3,发生反应的离子方程式为MnS2+9ClO-+6OH-=MoO42-+9Cl-+2SO42-+3H2O,故答案为:MoS2+9ClO-+6OH-=MoO42-+9Cl-+2SO42-+3H2O;
(5)①根据图示可知,当钼酸钠、月桂酸肌氨酸浓度相等时,腐蚀速率最小,腐蚀效果最好,即浓度比为1:1,答案为:1:1;
②当硫酸的浓度大于90%时,腐蚀速率几乎为零,原因是常温下浓硫酸具有强氧化性,会使铁钝化,起到防腐蚀作用,故答案为:常温下浓硫酸具有强氧化性,会使铁钝化;
③由图示数据可知,碳钢在盐酸中的腐蚀速率明显快于硫酸的腐蚀速度;硫酸浓度增大变成浓硫酸后,发生了钝化现象,腐蚀速度很慢,故答案为:Cl-有利于碳钢的腐蚀,SO42-不利于碳钢的腐蚀.
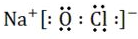 ,故答案为:
,故答案为: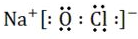 ;
;(2)提高焙烧效率,除增大空气量外还可以采用的措施是充分粉碎或逆流焙烧,故答案为:充分粉碎或逆流焙烧;
(3)途径I碱浸时发生反应的离子方程式为MoO3+CO32-=MnO42-+CO2↑,故答案为:MoO3+CO32-=MoO42-+CO2↑;
(4)途径Ⅱ用NaClO在碱性条件下氧化MoO3,发生反应的离子方程式为MnS2+9ClO-+6OH-=MoO42-+9Cl-+2SO42-+3H2O,故答案为:MoS2+9ClO-+6OH-=MoO42-+9Cl-+2SO42-+3H2O;
(5)①根据图示可知,当钼酸钠、月桂酸肌氨酸浓度相等时,腐蚀速率最小,腐蚀效果最好,即浓度比为1:1,答案为:1:1;
②当硫酸的浓度大于90%时,腐蚀速率几乎为零,原因是常温下浓硫酸具有强氧化性,会使铁钝化,起到防腐蚀作用,故答案为:常温下浓硫酸具有强氧化性,会使铁钝化;
③由图示数据可知,碳钢在盐酸中的腐蚀速率明显快于硫酸的腐蚀速度;硫酸浓度增大变成浓硫酸后,发生了钝化现象,腐蚀速度很慢,故答案为:Cl-有利于碳钢的腐蚀,SO42-不利于碳钢的腐蚀.
看了钼酸钠晶体(Na2MoO4•2...的网友还看了以下:
取某气态烷烃的一种二卤代产物21.6g与足量的NaOH溶液共热充分反应后,冷却,再用适量的硝酸酸化 2020-04-12 …
这道题是不是有错6、取甲种硫酸300克和乙种硫酸250克,再加水200克,可混合成浓度为50%的硫 2020-04-26 …
你知道烟草的核酸种类是什么吗? 2020-05-13 …
豌豆叶肉细胞中的核酸种类是5种,但是大豆根细胞所含的核酸中,含有碱基AGCT的核苷酸为什么是7种? 2020-06-12 …
不同生物含有的核酸种类不同.原核生物和真核生物同时含有DNA和RNA,病毒体内含有DNA或RNA, 2020-06-12 …
已知菠菜的干叶病是干叶病毒导致的,但不清楚干叶病毒的核酸种类,试设计实验探究.实验原理:(略).( 2020-06-27 …
已知菠菜的干叶病是干叶病毒导致的,但不清楚干叶病毒的核酸种类,试设计实验探究之。(1)实验原理:( 2020-06-27 …
不同生物含有的核酸种类不同.真核生物同时含有DNA和RNA,病毒体内含有DNA或RNA,下列关于各 2020-06-30 …
不同生物含有的核酸种类不同,下列各种生物中关于碱基、核苷酸种类的描述不正确的是()A口腔上皮细胞B 2020-06-30 …
裂谷热是由裂谷热病毒(含有单链RNA)引起的,经蚊类媒介或接触传播的急性病毒性传染病.下列关于裂谷 2020-07-04 …