早教吧作业答案频道 -->化学-->
钼(Mo)是一种重要的过渡金属元素,常见化合价为+6、+5、+4.由钼精矿(主要成分是MoS2)可制备单质钼和钼酸钠晶体(Na2MoO4.2H2O),部分流程如图1:(1)MoS2焙烧时反应的化学方程式为
题目详情
钼(Mo)是一种重要的过渡金属元素,常见化合价为+6、+5、+4.由钼精矿(主要成分是MoS2)可制备单质钼和钼酸钠晶体(Na2MoO4.2H2O),部分流程如图1:
(1)MoS2焙烧时反应的化学方程式为___;钼冶炼厂对大气产生污染的主要物质是___(填化学式),其对环境的主要危害是___.
(2)操作l中,加入碳酸钠溶液充分反应后,碱浸液中c(MoO42-)=0.80mol•L-1,c(SO42-)=0.04mol•L-1,在结晶前需加入Ba(OH)2固体以除去溶液中的SO42-.当BaMoO4开始沉淀时,SO42-的去除率是___.[KSP(BaSO4)=1.1×10-10、酶(BaMoO4)=4.0×10-8,溶液体积变化可忽略.
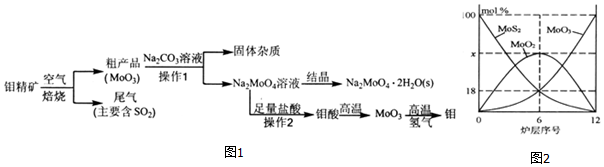
(3)焙烧钼精矿所用的装置是多层焙烧炉,图2为各炉层固体物料的物质的量的百分组成.
①图象中纵坐标x=___.
②焙烧炉中也会发生MoS2与MoO3反应生成MoO2和SO2的反应,该反应的化学方程式为___.若该反应转移6mol电子,则消耗的氧化剂的化学式及物质的量为___、___mol.
(4)钼电池未来有可能代替锂电池,成为动力电池的霸主.镁钼蓄电池的总反应为:xMg+Mo3S4
MgxMo3S4,则该电池充电时的阳极反应是___.

(1)MoS2焙烧时反应的化学方程式为___;钼冶炼厂对大气产生污染的主要物质是___(填化学式),其对环境的主要危害是___.
(2)操作l中,加入碳酸钠溶液充分反应后,碱浸液中c(MoO42-)=0.80mol•L-1,c(SO42-)=0.04mol•L-1,在结晶前需加入Ba(OH)2固体以除去溶液中的SO42-.当BaMoO4开始沉淀时,SO42-的去除率是___.[KSP(BaSO4)=1.1×10-10、酶(BaMoO4)=4.0×10-8,溶液体积变化可忽略.
(3)焙烧钼精矿所用的装置是多层焙烧炉,图2为各炉层固体物料的物质的量的百分组成.
①图象中纵坐标x=___.
②焙烧炉中也会发生MoS2与MoO3反应生成MoO2和SO2的反应,该反应的化学方程式为___.若该反应转移6mol电子,则消耗的氧化剂的化学式及物质的量为___、___mol.
(4)钼电池未来有可能代替锂电池,成为动力电池的霸主.镁钼蓄电池的总反应为:xMg+Mo3S4
| 充电 |
| |
| 放电 |
▼优质解答
答案和解析
(1)焙烧时MoS2发生氧化反应生成MoO3同时生成二氧化硫:2MoS2+7O2
2MoO3+4SO2;其中SO2形成酸雨危害环境;
故答案为:2MoS2+7O2
2MoO3+4SO2;SO2;形成酸雨;
(2)c(MoO42-)=0.80mol•L-1,c(SO42-)=0.04mol•L-1,当BaMoO4开始沉淀时,c(Ba2+)=
=
mol/L=5.0×10-8mol•L-1,
此时c(SO42-)=
mol/L=2.2×10-3mol•L-1,
SO42-的去除率=
×100%=94.5%;
故答案为:94.5%;
(3)①由图2可知,6层中存在的固体物质分别为MoS2、MoO3、MoO2,图象分析MoS2、MoO3的物质的量百分比均为18%,根据Mo元素守恒,则MoO2 的物质的量百分比为64%,则x为64;
故答案为:64;
②MoS2与MoO3反应生成MoO2和SO2,反应为:MoS2+6MoO3
7MoO2+2SO2,其中MoS2中Mo元素化合价不变,S元素由-4升高到+4价,被氧化,MoO3中Mo元素化合价由+6价降低到+4价,作氧化剂,6mol氧化剂MoO3反应转移电子12mol,故若该反应转移6mol电子,消耗的MoO33mol;
故答案为:MoS2+6MoO3
7MoO2+2SO2;MoO3;3;
(4)充电时,阳极失去电子发生氧化反应,故反应式为:MgxMo3S4-2xe-=Mo3S4+xMg2+或MoS42x--2xe-=Mo3S4;
故答案为:MgxMo3S4-2xe-=Mo3S4+xMg2+或MoS42x--2xe-=Mo3S4.
| ||
故答案为:2MoS2+7O2
| ||
(2)c(MoO42-)=0.80mol•L-1,c(SO42-)=0.04mol•L-1,当BaMoO4开始沉淀时,c(Ba2+)=
| Ksp(BaMoO4) |
| c(MoO42-) |
| 4.0×10-8 |
| 0.80 |
此时c(SO42-)=
| 1.1×10-10 |
| 5.0×10-8 |
SO42-的去除率=
| 0.040-2.2×10-3 |
| 0.040 |
故答案为:94.5%;
(3)①由图2可知,6层中存在的固体物质分别为MoS2、MoO3、MoO2,图象分析MoS2、MoO3的物质的量百分比均为18%,根据Mo元素守恒,则MoO2 的物质的量百分比为64%,则x为64;
故答案为:64;
②MoS2与MoO3反应生成MoO2和SO2,反应为:MoS2+6MoO3
| ||
故答案为:MoS2+6MoO3
| ||
(4)充电时,阳极失去电子发生氧化反应,故反应式为:MgxMo3S4-2xe-=Mo3S4+xMg2+或MoS42x--2xe-=Mo3S4;
故答案为:MgxMo3S4-2xe-=Mo3S4+xMg2+或MoS42x--2xe-=Mo3S4.
看了钼(Mo)是一种重要的过渡金属...的网友还看了以下:
选择下列元素S、O、C、H、Na、Cu、Fe写出符合题意的化学式:(1)配制溶液最常见的溶剂是;( 2020-04-11 …
由下列各组的三种元素构成的化合物中既有离子晶体,又有分子晶体的是( )A. H、O、CB. Na 2020-05-17 …
主谓宾宾补形式的name.paint.force.keep.find.find造句~1.s+vt+ 2020-05-20 …
有Na、S、O、H4种元素中的两种或3种元素组成的4种常见的化合物.其中,甲能跟氯化钡反应生成一种 2020-05-23 …
关于Ca.C.S.H.O.N元素的问题写出Ca.C.S.H.O.N六种元素能组成的所有化学式.所有 2020-06-11 …
19、下列属于同位素的是:A S和O B H2和O2 C 1735Cl 和 1736Cl D O2 2020-06-27 …
据报道,在小00℃、70uP你下由八氧化碳和氢气合成乙醇已成为现实.其反应如下:得了O得(g)+6s 2020-11-10 …
甲基橙(指示剂)是种酸的钠盐,含C、H、N、S、O、Na等元素,定量分析得到下列元素的质量分数:C为 2020-11-23 …
选下列5种元素:Na,O,S,Zn,H写出(1)金属氧化物(2)非金属氧化物(3)氢氧化物(4)5种 2020-12-24 …
由Na、S、O、H四种元素中的两种或三种元素组成的四种化合物,其中甲能跟氯化钡溶液反应生成两种盐;乙 2021-02-01 …