在含3molNaHSO3的溶液中加入含amolNaIO3的溶液充分反应(不考虑I2+I-⇌I3-),所得溶液中的I-与加入NaIO3的物质的量的关系曲线如图所示,下列说法不正确的是()A.还原性HSO3->I-,氧化
在含3molNaHSO3的溶液中加入含a mol NaIO3的溶液充分反应(不考虑I2+I-⇌I3-),所得溶液中的I-与加入NaIO3的物质的量的关系曲线如图所示,下列说法不正确的是( )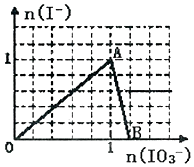
A. 还原性HSO3->I-,氧化性:IO3->SO42->I2
B. 当a=1时,溶液中n(I2):n(I-)=3:5
C. AB段,反应的离子方程式为:IO3-+5I-+6H+═3I2+3H2O
D. l<a<1.2时,溶液中SO42-与I-的物质的量之比为3:(6-5a)
B、当a=1时,溶液中n(I2):n(I-)=3:5,由反应IO3-+3HSO3-═I-+3SO42-+3H+可知,反应生成1mol的碘离子,则生成
| 3 |
| 5 |
C、AB段,生成的碘离子被碘酸根离子氧化,反应的离子方程式为:IO3-+5I-+6H+═3I2+3H2O,故C正确;
D、l<a<1.2时,溶液中SO42-的物质的量为3mol,而生成I-的物质的量为:1mol,余IO3-的物质的量为:(a-1)mol,则0<a-1<0.2时,由反应IO3-+6H++5I-═3H2O+3I2,碘离子过量,所以反应的碘离子的物质的量为:5(a-1)mol,此时溶液中碘离子的物质的量为:(6-5a)mol,则SO42-与I-的物质的量之比为3:(6-5a),故D正确;
故选A.
( 24 )通道是一种A ) I/O 设备 B ) I/O 控制器 C ) I/O 处理机 D )设 2020-05-23 …
通道是一种________。A.I/O设备B.I/O控制器C.I/O处理机D.设备控制器 2020-05-23 …
CPU与通道可以并行执行,并通过______实现彼此之间的通信和同步。A.I/O指令B.I/O中断C 2020-05-23 …
I/O缓冲区位于( )。A.主存储器内B.磁盘存储器内C.I/O接口内D.I/O设备内 2020-05-24 …
通道是一种A.I/O设备B.I/O控制器C.I/O处理机D.设备控制器 2020-05-24 …
能够利用DMA方式建立直接数据通路的两个部件是______。A.I/O设备和主存B.I/O设备和I/ 2020-05-26 …
O,I分别是锐角三角形ABC的外心,内心.O',I'分别是O,I关于BC的对称点.已知A、B、O' 2020-07-30 …
有括号的部分读音相同用S不相同的D1.m(i)lkth(i)s2.(th)at(th)is3.ph( 2020-10-31 …
单词拼写。①brcc1A.o;o;iB.o;i;oC.o;o;y②cartA.roB.orC.re③ 2020-10-31 …
英语向高人求教!写几句话.每句开头的第一个字母分别是“L,i,U,F,E,i,F,E,i,w,o,a 2020-12-15 …