早教吧作业答案频道 -->化学-->
金属硫化物和硫酸盐在工农业生产中有广泛应用.(1)二硫化钼(MoS2)是重要的固体润滑剂.向体积为2L的恒容密闭容器中加入0.1molMoS2、0.2molNa2CO3,并充入0.4molH2,发生反应:MoS2(s)+2Na2CO
题目详情
金属硫化物和硫酸盐在工农业生产中有广泛应用.
(1)二硫化钼(MoS2)是重要的固体润滑剂.
向体积为2L的恒容密闭容器中加入0.1molMoS2、0.2molNa2CO3,并充入0.4molH2,
发生反应:MoS2(s)+2Na2CO3(s)+4H2(g)⇌Mo(s)+2CO(g)+4H2O(g)+2Na2S(s)△H=akJ•mol-1,测得在不同温度下达到平衡时各气体的物质的量分数如图1所示.
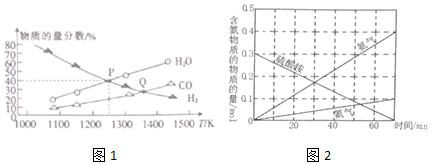
①a___0(填“<”“>”“=”,下同).
②容器内的总压:P点___Q点.
③P点对应温度下,H2的平衡转化率为___,平衡常数K=___.
(2)辉铜矿(主要成分是Cu2S)在冶炼过程中会产生大量的SO2.已知冶炼过程中部分反应为:
①2Cu2S(s)+3O2(g)═2Cu2O(s)+2SO2(g)△H=-768.2kJ/mol
②2Cu2O+Cu2S(s)═Cu(s)+SO2(g)△H=+116kJ/mol,则Cu2S与O2反应生成Cu与SO2的热化学方程式为___.
(3)回收处理SO2的方法之一是用氨水将其转化为NH4HSO3.已知常温下 Kb(NH3•H2O)=1.5×l0-5 Ka1(H2SO3)=1.6×l0-2 Ka2(H2SO3)=1×10-7,若吸收过程中氨水与SO2恰好完全反应,则所得溶液在常温下的pH___7(填“>”“<”或“=”,下同),溶液中c(SO32-)___c(H2SO3).
(4)在500℃下硫酸铵分解会得到4种产物,其含氮物质的物质的量随时间的变化如图2所示.则该条件下硫酸铵分解的化学方程式为___.
(1)二硫化钼(MoS2)是重要的固体润滑剂.
向体积为2L的恒容密闭容器中加入0.1molMoS2、0.2molNa2CO3,并充入0.4molH2,
发生反应:MoS2(s)+2Na2CO3(s)+4H2(g)⇌Mo(s)+2CO(g)+4H2O(g)+2Na2S(s)△H=akJ•mol-1,测得在不同温度下达到平衡时各气体的物质的量分数如图1所示.

①a___0(填“<”“>”“=”,下同).
②容器内的总压:P点___Q点.
③P点对应温度下,H2的平衡转化率为___,平衡常数K=___.
(2)辉铜矿(主要成分是Cu2S)在冶炼过程中会产生大量的SO2.已知冶炼过程中部分反应为:
①2Cu2S(s)+3O2(g)═2Cu2O(s)+2SO2(g)△H=-768.2kJ/mol
②2Cu2O+Cu2S(s)═Cu(s)+SO2(g)△H=+116kJ/mol,则Cu2S与O2反应生成Cu与SO2的热化学方程式为___.
(3)回收处理SO2的方法之一是用氨水将其转化为NH4HSO3.已知常温下 Kb(NH3•H2O)=1.5×l0-5 Ka1(H2SO3)=1.6×l0-2 Ka2(H2SO3)=1×10-7,若吸收过程中氨水与SO2恰好完全反应,则所得溶液在常温下的pH___7(填“>”“<”或“=”,下同),溶液中c(SO32-)___c(H2SO3).
(4)在500℃下硫酸铵分解会得到4种产物,其含氮物质的物质的量随时间的变化如图2所示.则该条件下硫酸铵分解的化学方程式为___.
▼优质解答
答案和解析
(1)①图1中曲线随温度升高,氢气含量减小,说明升温平衡正向进行,正反应为吸热反应,a>0,
故答案为:>;
②Q点温度高于P点,温度越高平衡正向进行,气体物质的量增大,容器中压强增大,则容器内的总压:P点故答案为:<;
③向体积为2L的恒容密闭容器中加入0.1molMoS2、0.2molNa2CO3,并充入0.4molH2,P点对应温度下,氢气和水蒸气的物质的量含量相同为40%,设 生成CO物质的量浓度为x,
发生反应:MoS2(s)+2Na2CO3(s)+4H2(g)⇌Mo(s)+2CO(g)+4H2O(g)+2Na2S(s)
起始量(mol/L) 0.2 0 0
变化量(mol/L) 2x x 2x
平衡量(mol/L) 0.2-2x x 2x
×100%=40%
x=0.05,
H2的平衡转化率=
×100%=50%,
平衡常数K=
=0.0025,
故答案为:50%;0.0025;
(2)①2Cu2S(s)+3O2(g)═2Cu2O(s)+2SO2(g)△H=-768.2kJ/mol
②2Cu2O+Cu2S(s)═Cu(s)+SO2(g)△H=+116kJ/mol,
结合盖斯定律计算(①+②)×
,得到Cu2S与O2反应生成Cu与SO2的热化学方程式:Cu2S(s)+O2(g)=2Cu(s)+SO2(g)△H=-217.4kJ/mol,
故答案为:Cu2S(s)+O2(g)=2Cu(s)+SO2(g)△H=-217.4kJ/mol;
(3)(3)已知常温下 Kb(NH3•H2O)=1.5×l0-5 Ka1(H2SO3)=1.6×l0-2 Ka2(H2SO3)=1×10-7,电离程度H2SO3>NH3•H2O>HSO3-,用氨水将其转化为NH4HSO3溶液中HSO3-电离程度大溶液显酸性,溶液PH<7,溶液中c(SO32-)>c(H2SO3),
故答案为:<;>;
(4)在500℃下硫酸铵分解过程中得到4种产物,其含氮物质随时间变化关系如图甲所示,硫酸铵分解生成氮气、氨气、二氧化硫和水,结合电子守恒和原子守恒配平书写得到化学方程式为3(NH4)2SO4
N2↑+4NH3↑+3SO2↑+6H2O↑,
故答案为:3(NH4)2SO4⇌N2↑+4NH3↑+3SO2↑+6H2O↑.
故答案为:>;
②Q点温度高于P点,温度越高平衡正向进行,气体物质的量增大,容器中压强增大,则容器内的总压:P点
③向体积为2L的恒容密闭容器中加入0.1molMoS2、0.2molNa2CO3,并充入0.4molH2,P点对应温度下,氢气和水蒸气的物质的量含量相同为40%,设 生成CO物质的量浓度为x,
发生反应:MoS2(s)+2Na2CO3(s)+4H2(g)⇌Mo(s)+2CO(g)+4H2O(g)+2Na2S(s)
起始量(mol/L) 0.2 0 0
变化量(mol/L) 2x x 2x
平衡量(mol/L) 0.2-2x x 2x
| 2x |
| 0.2-2x+x+2x |
x=0.05,
H2的平衡转化率=
| 2×0.05 |
| 0.2 |
平衡常数K=
| (2×0.05)4×0.052 |
| (0.2-0.05×2)4 |
故答案为:50%;0.0025;
(2)①2Cu2S(s)+3O2(g)═2Cu2O(s)+2SO2(g)△H=-768.2kJ/mol
②2Cu2O+Cu2S(s)═Cu(s)+SO2(g)△H=+116kJ/mol,
结合盖斯定律计算(①+②)×
| 1 |
| 3 |
故答案为:Cu2S(s)+O2(g)=2Cu(s)+SO2(g)△H=-217.4kJ/mol;
(3)(3)已知常温下 Kb(NH3•H2O)=1.5×l0-5 Ka1(H2SO3)=1.6×l0-2 Ka2(H2SO3)=1×10-7,电离程度H2SO3>NH3•H2O>HSO3-,用氨水将其转化为NH4HSO3溶液中HSO3-电离程度大溶液显酸性,溶液PH<7,溶液中c(SO32-)>c(H2SO3),
故答案为:<;>;
(4)在500℃下硫酸铵分解过程中得到4种产物,其含氮物质随时间变化关系如图甲所示,硫酸铵分解生成氮气、氨气、二氧化硫和水,结合电子守恒和原子守恒配平书写得到化学方程式为3(NH4)2SO4
| ||
故答案为:3(NH4)2SO4⇌N2↑+4NH3↑+3SO2↑+6H2O↑.
看了金属硫化物和硫酸盐在工农业生产...的网友还看了以下:
各种加速度的区分什么是变加速运动,变速运动,变减速运动,匀速匀速,匀变速运动,匀速圆周运动加速度怎 2020-04-13 …
运动员对杠铃施加恒力作用使杠铃竖直向上加速运动,杠铃升到B处时运动员要停止发力,杠铃继续向上运动, 2020-04-26 …
以Na2CO3、NaHCO3为例:电荷守恒:c(Na+)+c(H+)=c(HCO3-)+2c(CO 2020-05-13 …
穿过一个电阻为2Ω的闭合线圈的磁通量每秒均匀减小0.4Wb,则线圈中()A.感应电动势每秒减小0. 2020-06-02 …
高数题目设f(x)在[a,b]上可导,又f'(x)+[f(x)]^2-∫(a到x)f(t)dt=0 2020-06-12 …
钼锑抗分光光度法测定总磷时,配制钼酸盐的注意事项,为什么有时灵敏度低呢?我在配制时并没有加热钼酸氨 2020-06-24 …
请问这是什么型号不锈钢:碳0.12硅0.26锰7.8磷0.74铬14.58镍1.61钼0.16铜1. 2020-11-01 …
测定湖水中总磷,结果值为负,怎么回事?方法如下测定湖水中总磷,结果值为负,怎么回事?方法:50ml比 2020-11-01 …
卵磷脂的分子式,水解产物,鸡蛋黄加入95%的酒精有什么现象?卵磷脂在氢氧化钠中加热水解,产生的气体能 2020-11-01 …
某鸭梨产区建立恒温库储存鸭梨,为反季销售提供了条件,也为梨农增收提供了保障,据测算,没储存1千克鸭梨 2020-12-22 …