早教吧作业答案频道 -->化学-->
锰是冶炼工业中常用的添加剂.以碳酸锰矿(主要成分为MnCO3,还含有铁、镍、钴等碳酸盐杂质)为原料生产金属锰的工艺流程如下:已知25℃,部分物质的溶度积常数如下:物质Mn(O
题目详情
锰是冶炼工业中常用的添加剂.以碳酸锰矿(主要成分为MnCO3,还含有铁、镍、钴等碳酸盐杂质)为原料生产金属锰的工艺流程如下:
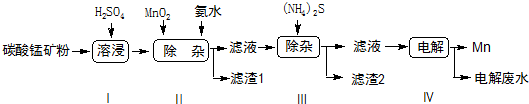
已知25℃,部分物质的溶度积常数如下:
(1)步骤Ⅰ中,MnCO3与硫酸反应的化学方程式是___.
(2)步骤Ⅱ中,MnO2在酸性条件下可将Fe2+离子氧化为Fe3+,则该反应过程中的离子方程式是___,加氨水调节溶液的pH为5.0-6.0,以除去Fe3+.
(3)步骤Ⅲ中,滤渣2的主要成分是___.
(4)步骤Ⅳ中,在___(填“阴”或“阳”)极析出Mn,电极反应方程式为___.
(5)已知:S(s)+O2(g)=SO2(g)△H=a kJ•mol-1
Mn(s)+S(s)+2O2(g)=MnSO4(s)△H=b kJ•mol-1
MnO2(s)+SO2(g)=MnSO4(s)△H=c kJ•mol-1,则Mn的燃烧热△H=___.
(6)按照图示流程,含MnCO3质量分数为57.5%的碳酸锰矿a kg,最终得到Mn的质量为110b kg,忽略中间过程的损耗,则除杂质时,所引入的锰元素相当于MnO2___kg.[MnCO3摩尔质量115g/mol,MnO2摩尔质量87g/mol].

已知25℃,部分物质的溶度积常数如下:
| 物质 | Mn(OH)2 | Co(OH)2 | Ni(OH)2 | MnS | CoS | NiS |
| Ksp | 2.1×10-13 | 3.0×10-16 | 5.0×10-16 | 1.0×10-11 | 5.0×10-22 | 1.0×10-22 |
(2)步骤Ⅱ中,MnO2在酸性条件下可将Fe2+离子氧化为Fe3+,则该反应过程中的离子方程式是___,加氨水调节溶液的pH为5.0-6.0,以除去Fe3+.
(3)步骤Ⅲ中,滤渣2的主要成分是___.
(4)步骤Ⅳ中,在___(填“阴”或“阳”)极析出Mn,电极反应方程式为___.
(5)已知:S(s)+O2(g)=SO2(g)△H=a kJ•mol-1
Mn(s)+S(s)+2O2(g)=MnSO4(s)△H=b kJ•mol-1
MnO2(s)+SO2(g)=MnSO4(s)△H=c kJ•mol-1,则Mn的燃烧热△H=___.
(6)按照图示流程,含MnCO3质量分数为57.5%的碳酸锰矿a kg,最终得到Mn的质量为110b kg,忽略中间过程的损耗,则除杂质时,所引入的锰元素相当于MnO2___kg.[MnCO3摩尔质量115g/mol,MnO2摩尔质量87g/mol].
▼优质解答
答案和解析
(1)加稀硫酸时样品中的MnCO3和硫酸反应生成可溶性的MnSO4,并产生二氧化碳和水,步骤Ⅰ中,MnCO3与硫酸反应的化学方程式为:MnCO3+H2SO4=MnSO4+CO2↑+H2O;
故答案为:MnCO3+H2SO4=MnSO4+CO2↑+H2O;
(2)步骤Ⅱ中,MnO2在酸性条件下可将Fe2+离子氧化为Fe3+,反应的离子方程式是据得失电子守恒有MnO2+2Fe2+-Mn2++2Fe3+,再据电荷守恒有MnO2+2Fe2++4H+-Mn2++2Fe3+,最后据原子守恒得,MnO2+2Fe2++4H+=Mn2++2Fe3++2H2O;
故答案为:MnO2+2Fe2++4H+=Mn2++2Fe3++2H2O;
(3)由于在第一次过滤之后的滤液中含有Mn2+、Ni2+、Co2+,向其中加入(NH4)2S,根据各物质的溶度积常数可确定有CoS和NiS沉淀(滤渣2)生成;
故答案为:CoS和NiS;
(4)由于第二次过滤后的滤液中主要含有NiSO4,电解该溶液时Ni2+在阴极上被还原:Mn2++2e-=Mn;
故答案为:阴,Mn2++2e-=Mn;
(5)①S(s)+O2(g)=SO2(g)△H=a kJ•mol-1
②Mn(s)+S(s)+2O2(g)=MnSO4(s)△H=b kJ•mol-1
③MnO2(s)+SO2(g)=MnSO4(s)△H=c kJ•mol-1,则Mn的燃烧热
盖斯定律计算得到②-①-③得到Mn(s)+O2(g)=MnO2(s)△H=-( a+c-b)kJ•mol-1
故答案为:-(a+c-b) kJ•mol-1;
(6)按照图示流程,含MnCO3质量分数为57.5%的碳酸锰矿a kg,最终得到Mn的质量为110b kg,忽略中间过程的损耗,除杂质时,所引入的锰元素和原来碳酸锰中锰元素总和为110b kg,设引入的锰元素相当于MnO2物质的量为x,
+x=
x=
-
相当于MnO2质量=(
-
)×87=(174b-0.435a )kg
故答案为:174b-0.435a;
故答案为:MnCO3+H2SO4=MnSO4+CO2↑+H2O;
(2)步骤Ⅱ中,MnO2在酸性条件下可将Fe2+离子氧化为Fe3+,反应的离子方程式是据得失电子守恒有MnO2+2Fe2+-Mn2++2Fe3+,再据电荷守恒有MnO2+2Fe2++4H+-Mn2++2Fe3+,最后据原子守恒得,MnO2+2Fe2++4H+=Mn2++2Fe3++2H2O;
故答案为:MnO2+2Fe2++4H+=Mn2++2Fe3++2H2O;
(3)由于在第一次过滤之后的滤液中含有Mn2+、Ni2+、Co2+,向其中加入(NH4)2S,根据各物质的溶度积常数可确定有CoS和NiS沉淀(滤渣2)生成;
故答案为:CoS和NiS;
(4)由于第二次过滤后的滤液中主要含有NiSO4,电解该溶液时Ni2+在阴极上被还原:Mn2++2e-=Mn;
故答案为:阴,Mn2++2e-=Mn;
(5)①S(s)+O2(g)=SO2(g)△H=a kJ•mol-1
②Mn(s)+S(s)+2O2(g)=MnSO4(s)△H=b kJ•mol-1
③MnO2(s)+SO2(g)=MnSO4(s)△H=c kJ•mol-1,则Mn的燃烧热
盖斯定律计算得到②-①-③得到Mn(s)+O2(g)=MnO2(s)△H=-( a+c-b)kJ•mol-1
故答案为:-(a+c-b) kJ•mol-1;
(6)按照图示流程,含MnCO3质量分数为57.5%的碳酸锰矿a kg,最终得到Mn的质量为110b kg,忽略中间过程的损耗,除杂质时,所引入的锰元素和原来碳酸锰中锰元素总和为110b kg,设引入的锰元素相当于MnO2物质的量为x,
| a×57.5% |
| 115 |
| 110b |
| 55 |
x=
| 110b |
| 55 |
| a×57.5% |
| 115 |
相当于MnO2质量=(
| 110b |
| 55 |
| a×57.5% |
| 115 |
故答案为:174b-0.435a;
看了锰是冶炼工业中常用的添加剂.以...的网友还看了以下:
根尖的分生区也称生长锥,或细胞分裂区,是细胞分裂最旺盛的顶端分生组织.分生区会产生不再分裂的新细胞 2020-05-04 …
心脏的结构部分:三静脉:⑦(4条)、⑧、⑨(1)如何分清心脏的左右?方法1:手捏法捏下部的,厚而硬 2020-05-13 …
(8分)鼠尾藻是一种着生在礁石上的大型海洋褐藻,可作为海参的优质饲料。鼠尾藻枝条中上部的叶片较窄, 2020-05-16 …
鼠尾藻是一种着生在礁石上的大型海洋褐藻,可作为海参的优质饲料。鼠尾藻枝条中上部的叶片较窄,称之狭叶 2020-05-16 …
如图所示,半径为R,内径很小的光滑半圆管竖直放置.两个质量均为m的小球a、b以不同的速度进入管内, 2020-05-22 …
物体受到的浮力等于下部的压力减上部的压力什么意思? 2020-05-23 …
由于药隔延长,花药的花粉囊分成两部分,且()。A.花药上部的裂片可育,下部的裂片不育B.花药上部的裂 2020-05-25 …
鼠尾草花由于药隔延长,花药的花粉囊分成两部分,且()。A.花药上部的裂片可育,下部的裂片不育B.花药 2020-05-25 …
二元一次方程:我校为丰富校园文化氛围,要设计一座2米高的人体雕像,使雕像的上部(腰以上)与全部高度 2020-06-14 …
体检时,医生常用小槌敲打膝盖下部的韧带,会使小腿前伸,被检查的这种行为受哪部分控制()A.脑干B. 2020-06-21 …