早教吧作业答案频道 -->化学-->
现向含6molKI的硫酸溶液中逐滴加入KBrO3溶液,整个过程中含碘物质的物质的量与所加入KBrO3的物质的量的关系如图所示.已知①BrO3-+6I一+6H+=3I2+Br-+3H2O;②2BrO3-+I2=2IO3-+Br2;请回答下列问题:
题目详情
现向含6mol KI的硫酸溶液中逐滴加入KBrO3溶液,整个过程中含碘物质的物质的量与所加入KBrO3的物质的量的关系如图所示.
已知①BrO3-+6I一+6H+=3I2+Br-+3H2O;
②2BrO3-+I2=2IO3-+Br2;
请回答下列问题:
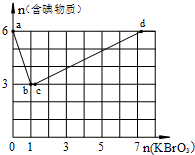
(1)由反应②有同学由此得出氧化性:I2>Br2的结论,你认为是否正确___(填是或否),并说明理由___
(2)b点时,KI反应完全,则消耗的氧化剂与还原剂物质的量之比为___,还原产物是___.
(3)b→c过程中只有一种元素的化合价发生变化,写出该过程的离子反应方程式___.
(4)含6mol KI的硫酸溶液所能消耗n(KBrO3)的最大值为___mol.
(5)n(KBrO3)=4mol时,对应含碘物质的化学式为___.
(6)若实验室需要6mol•L-1的KI溶液480mL,根据配制情况回答下列问题:
①实验室中除了托盘天平、烧杯、药匙、量筒外还需要的其它仪器有___.
②下列操作使所配溶液浓度偏低的有___(填字母);
A.容量瓶未干燥就用来配制溶液B.定容时,加蒸馏水超过刻度线,又用胶头滴管吸出
C.往容量瓶转移时有少量液体溅出 D.定容时仰视刻度线.
已知①BrO3-+6I一+6H+=3I2+Br-+3H2O;
②2BrO3-+I2=2IO3-+Br2;
请回答下列问题:

(1)由反应②有同学由此得出氧化性:I2>Br2的结论,你认为是否正确___(填是或否),并说明理由___
(2)b点时,KI反应完全,则消耗的氧化剂与还原剂物质的量之比为___,还原产物是___.
(3)b→c过程中只有一种元素的化合价发生变化,写出该过程的离子反应方程式___.
(4)含6mol KI的硫酸溶液所能消耗n(KBrO3)的最大值为___mol.
(5)n(KBrO3)=4mol时,对应含碘物质的化学式为___.
(6)若实验室需要6mol•L-1的KI溶液480mL,根据配制情况回答下列问题:
①实验室中除了托盘天平、烧杯、药匙、量筒外还需要的其它仪器有___.
②下列操作使所配溶液浓度偏低的有___(填字母);
A.容量瓶未干燥就用来配制溶液B.定容时,加蒸馏水超过刻度线,又用胶头滴管吸出
C.往容量瓶转移时有少量液体溅出 D.定容时仰视刻度线.
▼优质解答
答案和解析
(1)根据反应:2BrO3-+I2═2IO3-+Br2,还原剂的还原性强于还原产物的氧化性,所以得出还原性I2>Br2,
故答案为:否;该反应中I2作还原剂,Br2为还原产物,应得出还原性I2>Br2结论;
(2)b点时,KI反应完全,有图象可知参加反应的KI为6mol,KBrO3为1mol,则消耗的氧化剂与还原剂物质的量之比为1:6,
发生反应为6I-+BrO3-=Br-+3I2,还原产物是KBr,
故答案为:1:6;KBr;
(3)b→c过程中,仅有一种元素发生化合价变化,应是BrO3-与Br-之间的氧化还原反应,反应的离子方程式为BrO3-+5Br-+6H+=3Br2+3H2O,
故答案为:BrO3-+5Br-+6H+=3Br2+3H2O;
(4)发生的反应依次有6I-+6H++BrO3-=Br-+3I2+3H2O,BrO3-+5Br-+6H+=3Br2+3H2O,2BrO3-+I2=2IO3-+Br2,
总反应为5I-+6H++6BrO3-=5IO3-+3Br2+3H2O,则含6molKI的硫酸溶液所能消耗n(KBrO3)的最大值为1.2×6mol=7.2mol,
故答案为:7.2;
(5)n(KBrO3)=4时,发生的反应依次有6I-+BrO3-=Br-+3I2,BrO3-+5Br-+6H+=3Br2+3H2O,2BrO3-+I2=2IO3-+Br2,6molKI生成I2,需要1molKBrO3,同时生成1molKBr,发生BrO3-+5Br-+6H+=3Br2+3H2O,需要0.2molKBrO3,如I2完全被氧化生成KIO3,还应需要6molKBrO3,
则n(KBrO3)=4时,对应含碘物质的化学式为I2,KIO3,
故答案为:I2,KIO3;
(6)①6mol•L-1的KI溶液480mL,托盘天平、烧杯、药匙、量筒外还需要的其它仪器有:玻璃棒、胶头滴管、500ml 容量瓶,故答案为:玻璃棒、胶头滴管、500ml 容量瓶;
②A.容量瓶未干燥就用来配制溶液,无影响,故不选;
B.定容时,加蒸馏水超过刻度线,又用胶头滴管吸出,溶质的量减少,浓度偏低,故选;
C.往容量瓶转移时有少量液体溅出,溶质的量减少,浓度偏低,故选;
D.定容时仰视刻度线,体积变大,浓度偏低,故选,
故选:BCD.
故答案为:否;该反应中I2作还原剂,Br2为还原产物,应得出还原性I2>Br2结论;
(2)b点时,KI反应完全,有图象可知参加反应的KI为6mol,KBrO3为1mol,则消耗的氧化剂与还原剂物质的量之比为1:6,
发生反应为6I-+BrO3-=Br-+3I2,还原产物是KBr,
故答案为:1:6;KBr;
(3)b→c过程中,仅有一种元素发生化合价变化,应是BrO3-与Br-之间的氧化还原反应,反应的离子方程式为BrO3-+5Br-+6H+=3Br2+3H2O,
故答案为:BrO3-+5Br-+6H+=3Br2+3H2O;
(4)发生的反应依次有6I-+6H++BrO3-=Br-+3I2+3H2O,BrO3-+5Br-+6H+=3Br2+3H2O,2BrO3-+I2=2IO3-+Br2,
总反应为5I-+6H++6BrO3-=5IO3-+3Br2+3H2O,则含6molKI的硫酸溶液所能消耗n(KBrO3)的最大值为1.2×6mol=7.2mol,
故答案为:7.2;
(5)n(KBrO3)=4时,发生的反应依次有6I-+BrO3-=Br-+3I2,BrO3-+5Br-+6H+=3Br2+3H2O,2BrO3-+I2=2IO3-+Br2,6molKI生成I2,需要1molKBrO3,同时生成1molKBr,发生BrO3-+5Br-+6H+=3Br2+3H2O,需要0.2molKBrO3,如I2完全被氧化生成KIO3,还应需要6molKBrO3,
则n(KBrO3)=4时,对应含碘物质的化学式为I2,KIO3,
故答案为:I2,KIO3;
(6)①6mol•L-1的KI溶液480mL,托盘天平、烧杯、药匙、量筒外还需要的其它仪器有:玻璃棒、胶头滴管、500ml 容量瓶,故答案为:玻璃棒、胶头滴管、500ml 容量瓶;
②A.容量瓶未干燥就用来配制溶液,无影响,故不选;
B.定容时,加蒸馏水超过刻度线,又用胶头滴管吸出,溶质的量减少,浓度偏低,故选;
C.往容量瓶转移时有少量液体溅出,溶质的量减少,浓度偏低,故选;
D.定容时仰视刻度线,体积变大,浓度偏低,故选,
故选:BCD.
看了现向含6molKI的硫酸溶液中...的网友还看了以下:
已知:2AlO2-+CO2+3H2O=2Al(OH)3↓+CO32-.向含1molNaOH、0.5 2020-04-07 …
A、B两种物质都是H、N、O、Na中的任意三种元素组成的强电解质,A的水溶液呈碱性,B的水溶液呈酸 2020-04-11 …
设一人群中有37.5%的人血液为A型,20.9%的人血液为B型,33.7%的人血液为O型,7.9% 2020-04-26 …
在100ml,0.1mol•L-1HA的溶液中,c(H+)=0.05mol•L-1,往该溶液中加入 2020-05-13 …
有机物A的分子式为C57H104O6,在硫酸存在的条件下发生水解反应:A+3H2O=3B+C,其中 2020-05-13 …
镁镍蓄电池放电时的总反应为Mg+Ni2O3+3H2O═Mg(OH)2+2Ni(OH)2.下列有关该 2020-05-14 …
(2010•江苏)设NA为阿伏加德罗常数的值,下列叙述正确的是()A.常温下,1L0.1mol•L 2020-05-14 …
下列表示对应化学反应的离子方程式正确的是A. 用KIO3 氧化酸性溶液中的KI: 5I-+IO3- 2020-05-16 …
2013浦东新区高考化学一模最后一道计算题怎么做?工业常利用Cl2+6KOH(热)→KClO3+5 2020-05-22 …
设NA为阿伏加德罗常数的值,下列叙述正确的是()A.常温下,1L0.1mol•L-1的NH4NO3 2020-05-23 …