早教吧作业答案频道 -->化学-->
(1)过氧化氢(H2O2)有广泛的用途.过氧化氢的制备方法很多,下列方法中原子利用率最高的是(填序号).A.BaO2+H2SO4=BaSO4↓+H2O2B.2NH4HSO4电解
题目详情
(1)过氧化氢(H2O2)有广泛的用途.过氧化氢的制备方法很多,下列方法中原子利用率最高的是___(填序号).
A.BaO2+H2SO4=BaSO4↓+H2O2
B.2NH4HSO4
(NH4)2S2O8+H2↑;(NH4)2S2O8+2H2O=2NH4HSO4+H2O2
C.CH3CHOHCH3+O2→CH3COCH3+H2O2
D.乙基蒽醌法见图1
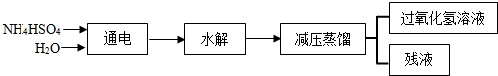
Ⅰ.B选项的方法流程图如下:
回答下列问题:
(2)若要制得1mol H2O2,电解时转移电子数为___,电解硫酸氢铵溶液时,阳极的电极反应方程是:___.
(3)在上流程图中,采用减压蒸馏的原因是:___.可循环利用的物质是(写化学式)___.
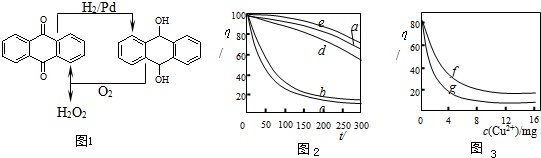
Ⅱ.某文献报导了不同金属离子及其浓度对双氧水氧化降解海藻酸钠溶液反应速率的影响,实验结果如图2、图3所示.注:以上实验均在温度为20℃、w(H2O2)=0.25%、pH=7.12、海藻酸钠溶液浓度为8mg•L-1的条件下进行.图2中曲线a:H2O2;b:H2O2+Cu2+;c:H2O2+Fe2+;d:H2O2+Zn2+;e:H2O2+Mn2+;图3中曲线f:反应时间为1h;g:反应时间为2h;两图中的纵坐标代表海藻酸钠溶液的粘度(海藻酸钠浓度与溶液粘度正相关).
(4)由上述信息可知,下列叙述错误的是___(填序号).
A.锰离子能使该降解反应速率减缓
B.亚铁离子对该降解反应的催化效率比铜离子低
C.海藻酸钠溶液粘度的变化快慢可反映出其降解反应速率的快慢
D.一定条件下,铜离子浓度一定时,反应时间越长,海藻酸钠溶液浓度越小.
A.BaO2+H2SO4=BaSO4↓+H2O2
B.2NH4HSO4
| ||
C.CH3CHOHCH3+O2→CH3COCH3+H2O2
D.乙基蒽醌法见图1

Ⅰ.B选项的方法流程图如下:

回答下列问题:
(2)若要制得1mol H2O2,电解时转移电子数为___,电解硫酸氢铵溶液时,阳极的电极反应方程是:___.
(3)在上流程图中,采用减压蒸馏的原因是:___.可循环利用的物质是(写化学式)___.
Ⅱ.某文献报导了不同金属离子及其浓度对双氧水氧化降解海藻酸钠溶液反应速率的影响,实验结果如图2、图3所示.注:以上实验均在温度为20℃、w(H2O2)=0.25%、pH=7.12、海藻酸钠溶液浓度为8mg•L-1的条件下进行.图2中曲线a:H2O2;b:H2O2+Cu2+;c:H2O2+Fe2+;d:H2O2+Zn2+;e:H2O2+Mn2+;图3中曲线f:反应时间为1h;g:反应时间为2h;两图中的纵坐标代表海藻酸钠溶液的粘度(海藻酸钠浓度与溶液粘度正相关).
(4)由上述信息可知,下列叙述错误的是___(填序号).
A.锰离子能使该降解反应速率减缓
B.亚铁离子对该降解反应的催化效率比铜离子低
C.海藻酸钠溶液粘度的变化快慢可反映出其降解反应速率的快慢
D.一定条件下,铜离子浓度一定时,反应时间越长,海藻酸钠溶液浓度越小.
▼优质解答
答案和解析
(1)ABC中除了生成双氧水为还有其它物质生成,D中只有双氧水生成,所以D中原子利用率最高,故答案为:D;
(2)该反应中氧元素的化合价变化为:-2价→-1价,所以生成1mol双氧水转移电子2NA;SO42-失去e-生成S2O82-,阳极的电极反应方程是:2SO42--2e-=S2O82-,故答案为:2NA;2SO42--2e-=S2O82-;
(3)过氧化氢受热容易分解,减小气压,使液体沸点降低;残液为NH4HSO4,可循环利用,故答案为:过氧化氢不稳定,受热容易分解,减小气压,使液体沸点降低;NH4HSO4;
(4)根据图2知,纵坐标越大其粘度越大,相同时间内纵坐标变化越大,其反应速率越快,根据图3知,相同浓度的铜离子溶液中,纵坐标变化越大,其反应速率越大,
A.e曲线变化不明显,所以锰离子能使该降解反应速率减缓,故正确;
B.相同时间内,含有亚铁离子的曲线纵坐标变化比含有铜离子的大,所以亚铁离子对该降解反应的催化效率比铜离子高,故错误;
C.海藻酸钠浓度与溶液粘度正相关,粘度变化越大海藻酸钠浓度变化越大,其反应速率越大,所以海藻酸钠溶液粘度的变化快慢可反映出其降解反应速率的快慢,故正确;
D.根据图3知,一定条件下,铜离子浓度一定时,反应时间越长,溶液粘度越小,则海藻酸钠溶液浓度越小,故正确;
故答案为:B.
(2)该反应中氧元素的化合价变化为:-2价→-1价,所以生成1mol双氧水转移电子2NA;SO42-失去e-生成S2O82-,阳极的电极反应方程是:2SO42--2e-=S2O82-,故答案为:2NA;2SO42--2e-=S2O82-;
(3)过氧化氢受热容易分解,减小气压,使液体沸点降低;残液为NH4HSO4,可循环利用,故答案为:过氧化氢不稳定,受热容易分解,减小气压,使液体沸点降低;NH4HSO4;
(4)根据图2知,纵坐标越大其粘度越大,相同时间内纵坐标变化越大,其反应速率越快,根据图3知,相同浓度的铜离子溶液中,纵坐标变化越大,其反应速率越大,
A.e曲线变化不明显,所以锰离子能使该降解反应速率减缓,故正确;
B.相同时间内,含有亚铁离子的曲线纵坐标变化比含有铜离子的大,所以亚铁离子对该降解反应的催化效率比铜离子高,故错误;
C.海藻酸钠浓度与溶液粘度正相关,粘度变化越大海藻酸钠浓度变化越大,其反应速率越大,所以海藻酸钠溶液粘度的变化快慢可反映出其降解反应速率的快慢,故正确;
D.根据图3知,一定条件下,铜离子浓度一定时,反应时间越长,溶液粘度越小,则海藻酸钠溶液浓度越小,故正确;
故答案为:B.
看了 (1)过氧化氢(H2O2)有...的网友还看了以下:
铁氧体是一类磁性材料,通式为MO•xFe2O3(M为二价金属离子).根据题意完成:(1)为了制备铁 2020-05-13 …
钴及其化合物可应用与催化剂、电池、颜料与染料等.(1)CoO是一种油漆添加剂,可通过反应①②制备. 2020-05-13 …
利用LiOH和钴氧化物可制备锂离子电池正极材料。LiOH可由电解法制备,利用如图装置电解制备LiO 2020-06-14 …
由二氧化锰制备金属锰是否能自发进行快!由二氧化锰制备金属锰可采取下列两种方法:(1)MnO2(s) 2020-06-14 …
制备BaCl2和SO3的流程图如下:已知;①BaSO4(s)+4C(s)高温4CO(g)+BaS( 2020-07-19 …
磷单质及其化合物的、有广泛应用(1)同磷灰石[主要成分]在高温下制备黄磷(P4)的热化学方程式为:4 2020-11-24 …
某化学兴趣小组的同学利用图所示实验装置进行NH3、Cl2的制备、性质等实验(图中夹持装置有省略).请 2020-12-19 …
我国钾长石(KAlSi3O8)的资源比较丰富.工业上可用食盐和钾长石在一定条件下制备氯化钾:NaCl 2021-01-04 …
(2013•江苏三模)金属镁可用于制造合计、储氢材料、镁电池等.已知:C(s)+12O2(g)=CO 2021-01-13 …
某化学小组利用以下装置制备氨气、氯气以及LiH固体.(1)为制备干燥的氨气,可将装置C与(填装置编号 2021-02-08 …