早教吧作业答案频道 -->化学-->
碱性锌锰干电池是生活中应用最普遍的电池之一,其结构如图所示,已知电池放电后的产物是Zn(OH)2和MnOOH.(1)该电池的负极材料是,正极反应式为;(2)锌能和KOH发生反应,类似
题目详情
碱性锌锰干电池是生活中应用最普遍的电池之一,其结构如图所示,已知电池放电后的产物是Zn(OH)2和MnOOH.
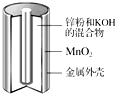
(1)该电池的负极材料是___,正极反应式为___;
(2)锌能和KOH发生反应,类似于铝与KOH的反应,其化学方程式为___;
(3)用该电池作电源,以硫酸铜溶液为电解液,模拟电解精炼铜.
①精炼铜时,粗铜连接电源的___(填“正”或“负”)极;电解一段时间后,CuSO4溶液的浓度___(填“增大”、“减小”或“不变”);
②若阴极质量增重32g,则电池消耗MnO2的质量为___g.

(1)该电池的负极材料是___,正极反应式为___;
(2)锌能和KOH发生反应,类似于铝与KOH的反应,其化学方程式为___;
(3)用该电池作电源,以硫酸铜溶液为电解液,模拟电解精炼铜.
①精炼铜时,粗铜连接电源的___(填“正”或“负”)极;电解一段时间后,CuSO4溶液的浓度___(填“增大”、“减小”或“不变”);
②若阴极质量增重32g,则电池消耗MnO2的质量为___g.
▼优质解答
答案和解析
(1)原电池中Zn转化为Zn(OH)2,Zn化合价升高,失电子,做负极,正极上发生得电子的还原反应,电极反应式为:MnO2+H2O+e-═MnOOH+OH-,故答案为:Zn;MnO2+H2O+e-=MnOOH+OH-;
(2)金属锌和氢氧化钾之间反应生成偏锌酸钾和氢气,即Zn+2KOH=K2ZnO2+H2↑,故答案为:Zn+2KOH=K2ZnO2+H2↑;
(3)①利用电解法进行粗铜提纯时,粗铜应作阳极,精铜作阴极,粗铜连接电源的正极,阳极与电池的正极相连发生氧化反应,依次是Zn、Fe、Cu放电,阴极与电池的负极相连发生还原反应:Cu2++2e-═Cu,电解一段时间后,CuSO4溶液的浓度减小,故答案为:正;减小;
②若阴极质量增重32g即0.5mol,根据电极反应:Cu2++2e-═Cu,转移电子是1mol,电池的正极反应:MnO2+H2O+e-═MnOOH+OH-,此时消耗MnO2的物质的量是:1mol,质量是87g,故答案为:87.
(2)金属锌和氢氧化钾之间反应生成偏锌酸钾和氢气,即Zn+2KOH=K2ZnO2+H2↑,故答案为:Zn+2KOH=K2ZnO2+H2↑;
(3)①利用电解法进行粗铜提纯时,粗铜应作阳极,精铜作阴极,粗铜连接电源的正极,阳极与电池的正极相连发生氧化反应,依次是Zn、Fe、Cu放电,阴极与电池的负极相连发生还原反应:Cu2++2e-═Cu,电解一段时间后,CuSO4溶液的浓度减小,故答案为:正;减小;
②若阴极质量增重32g即0.5mol,根据电极反应:Cu2++2e-═Cu,转移电子是1mol,电池的正极反应:MnO2+H2O+e-═MnOOH+OH-,此时消耗MnO2的物质的量是:1mol,质量是87g,故答案为:87.
看了 碱性锌锰干电池是生活中应用最...的网友还看了以下:
(1)完成下列反应的化学方程式,并注明反应的基本类型.①高锰酸钾制氧气2KMnO4△.K2MnO4 2020-05-02 …
铜锌原电池 硫酸锌 硫酸铜 一些基本的问题锌为什么会溶解? 不是不和硫酸锌反应吗?是锌片和铜 2020-05-15 …
实验室常用锌和稀硫酸反应制取氢气,同时生成硫酸锌.现在要制取氢气0.3g,需要锌的质量多少克?同时 2020-05-17 …
烯烃通过臭氧化并经锌和水处理得到醛或酮.例如:CH3CH2CH═,CH3CH2CH═O+O═上述反 2020-07-04 …
下列变化过程中,原物质分子内共价键被破坏,同时有离子键形成的是()A.盐酸和NaOH溶液混合B.氯 2020-07-21 …
烯烃通过臭氧氧化并经锌和水处理得到醛或酮.例如CH3O3CH3CH3CH2CH=C〈-------> 2020-11-03 …
将金属锌投入足量的稀硝酸中锌完全反应若参加反应的锌和HNO3的物质的量之比为2:5,则HNO3被还原 2020-11-27 …
已知锰盐中锰元素显+2价,写出一个有金属锰参加的置换反应:锌和稀硫酸反应所得溶液的颜色:镁与水蒸汽的 2021-01-07 …
写化学方程式写出下列反应方程式:1.二氧化碳通入紫色石蕊试液2.生石灰溶于水3.无水硫酸铜做干燥剂4 2021-02-01 …
高一化学急在线等乙醇是只能和纳这一个金属反应吗锌和钡呢?哪类金属可以和乙醇反应? 2021-02-05 …