早教吧作业答案频道 -->化学-->
中药药剂砒霜(主要成分为As2O3,微溶于水),可用于治疗急性白血病.工业上用含硫化砷(As2S3)的废渣生产砒霜的工艺流程如图1所示:(1)硫化砷中砷元素化合价为,其难溶于水,“
题目详情
中药药剂砒霜(主要成分为As2O3,微溶于水),可用于治疗急性白血病.工业上用含硫化砷(As2S3)的废渣生产砒霜的工艺流程如图1所示:
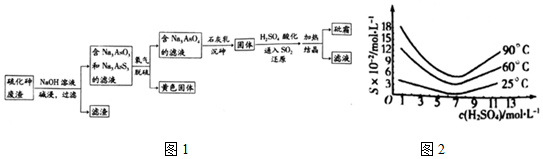
(1)硫化砷中砷元素化合价为___,其难溶于水,“碱浸”过程中硫元素价态不变,发生的主要反应的离子方程式为___.
(2)氧化脱硫过程中被氧化的元素是___.
(3)还原过程中H3AsO4转化为H3AsO3,反应的化学方程式是___.
(4)“沉砷”是在一定温度下将砷元素转化为Ca5(AsO4)3OH沉淀的过程,主要反应有:
a.Ca(OH)2(S)⇌Ca2+(aq)+2OH-(aq)Ksp=10-7
b.Ca5(AsO4)3OH (s)⇌5Ca2+(aq)+OH-(aq)+3AsO43-(aq) Ksp=10-40
加入石灰乳调溶液中c(OH-)=0.01mol•L-1,此时溶液中c(AsO43-)=___.
(已知:
=2.15)
(5)还原后加热溶液,H3AsO3分解为As2O3,结晶得到粗As2O3.As2O3在不同温度和不同浓度硫酸中的溶解度度(S)曲线如图2所示.
为了提高粗的沉淀率,“结晶”过程进行的操作是蒸发浓缩,冷却结晶,过滤,洗涤,在此过程中应控制的条件为___.
(6)在工业生产中,最后一步所得滤液可循环使用,其目的是___.

(1)硫化砷中砷元素化合价为___,其难溶于水,“碱浸”过程中硫元素价态不变,发生的主要反应的离子方程式为___.
(2)氧化脱硫过程中被氧化的元素是___.
(3)还原过程中H3AsO4转化为H3AsO3,反应的化学方程式是___.
(4)“沉砷”是在一定温度下将砷元素转化为Ca5(AsO4)3OH沉淀的过程,主要反应有:
a.Ca(OH)2(S)⇌Ca2+(aq)+2OH-(aq)Ksp=10-7
b.Ca5(AsO4)3OH (s)⇌5Ca2+(aq)+OH-(aq)+3AsO43-(aq) Ksp=10-40
加入石灰乳调溶液中c(OH-)=0.01mol•L-1,此时溶液中c(AsO43-)=___.
(已知:
| 3 | 10 |
(5)还原后加热溶液,H3AsO3分解为As2O3,结晶得到粗As2O3.As2O3在不同温度和不同浓度硫酸中的溶解度度(S)曲线如图2所示.
为了提高粗的沉淀率,“结晶”过程进行的操作是蒸发浓缩,冷却结晶,过滤,洗涤,在此过程中应控制的条件为___.
(6)在工业生产中,最后一步所得滤液可循环使用,其目的是___.
▼优质解答
答案和解析
(1)硫化砷(As2S3)中硫元素-2价,则砷元素+3价;“碱浸”过程中硫元素价态不变,由流程可知生成Na3AsS3、Na3AsO3溶液,离子方程式为:As2S3+6OH-=AsO33-+AsS33-+3H2O;
故答案为:+3;As2S3+6OH-=AsO33-+AsS33-+3H2O;
(2)根据流程可知氧化脱硫过程中,Na3AsS3、Na3AsO3生成Na3AsO4溶液和S单质,其中硫元素、砷元素化合价升高,发生氧化反应,故被氧化的元素为As、S;
故答案为:As、S;
(3)还原过程中二氧化硫将H3AsO4转化为H3AsO3,反应为:SO2+H3AsO4+H2O=H3AsO3+H2SO4;
故答案为:SO2+H3AsO4+H2O=H3AsO3+H2SO4;
(4)c(OH-)=0.01mol•L-1,已知:Ca(OH)2(S)⇌Ca2+(aq)+2OH-(aq)Ksp=10-7,则c(Ca2+)=
=10-3mol•L-1,Ca5(AsO4)3OH (s)⇌5Ca2+(aq)+OH-(aq)+3AsO43-(aq) Ksp=10-40,溶液中c(AsO43-)=
=2.15×10-8mol•L-1;
故答案为:2.15×10-8mol•L-1;
(5)由图2可知:As2O3在25℃、硫酸浓度约为7 mol•L-1时的溶解度度(S)最小,故“结晶”过程应调硫酸浓度约为7 mol•L-1,冷却至温度为25℃;
故答案为:调硫酸浓度约为7 mol•L-1,冷却至温度为25℃;
(6)提高砷的回收率,在工业生产中,最后一步所得滤液可循环使用;
故答案为:提高砷的回收率.
故答案为:+3;As2S3+6OH-=AsO33-+AsS33-+3H2O;
(2)根据流程可知氧化脱硫过程中,Na3AsS3、Na3AsO3生成Na3AsO4溶液和S单质,其中硫元素、砷元素化合价升高,发生氧化反应,故被氧化的元素为As、S;
故答案为:As、S;
(3)还原过程中二氧化硫将H3AsO4转化为H3AsO3,反应为:SO2+H3AsO4+H2O=H3AsO3+H2SO4;
故答案为:SO2+H3AsO4+H2O=H3AsO3+H2SO4;
(4)c(OH-)=0.01mol•L-1,已知:Ca(OH)2(S)⇌Ca2+(aq)+2OH-(aq)Ksp=10-7,则c(Ca2+)=
| 10-7 |
| (10-2)2 |
| 3 |
| ||
故答案为:2.15×10-8mol•L-1;
(5)由图2可知:As2O3在25℃、硫酸浓度约为7 mol•L-1时的溶解度度(S)最小,故“结晶”过程应调硫酸浓度约为7 mol•L-1,冷却至温度为25℃;
故答案为:调硫酸浓度约为7 mol•L-1,冷却至温度为25℃;
(6)提高砷的回收率,在工业生产中,最后一步所得滤液可循环使用;
故答案为:提高砷的回收率.
看了 中药药剂砒霜(主要成分为As...的网友还看了以下:
算式要有得数,方程要有等式和过程和得数,谢谢红,白,黄三种玻璃珠放在一起,其中红珠占百分之25,白 2020-05-13 …
洪灾过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一.漂白粉是常用的消毒剂.(1) 2020-05-13 …
漂白粉的主要成分是CaCl2和Ca(ClO)2.工业上制取漂白粉的反应可表示为:2Cl2+2Ca( 2020-05-13 …
漂白粉的主要成分是CaCl2和Ca(ClO)2.工业上制取漂白粉的反应可表示为:2Cl2+2Ca( 2020-05-13 …
按要求写出下列方程式(1)双氧水(H2O2)和水都是极弱电解质,但H2O2溶液显酸性.若把H2O2 2020-05-13 …
某自来水厂净水流程如下所示:(1)净水过程中,在天然水中加入明矾的作用是,过滤可除去水中,而水中色 2020-05-13 …
但不能平的,为什么偏要白白走这一遭啊?(改为陈述句是下面的哪一句?)1.但不能平的,是要白白走这一 2020-07-22 …
关于平方差的数学题,会的帮下m-n=2,m+n=5,则m^2-n^2的值为?②2001^2-199 2020-07-31 …
5(x-5.5)=20.52.4(6.4+x)=19.2.25(x+48)=1750.(解方程)一筐 2020-10-29 …
有若干个蓝球和白球,蓝球个数是白球的4分之3,现在取走24个蓝球,添进12个白球后,蓝球的个数是白球 2020-10-30 …