已知烧杯中装有200g硫酸和硫酸铜混合溶液,其中含硫酸铜4.8g.向烧杯中逐渐加入氧化铜,烧杯中溶液的质量与加入氧化铜的质量关系如图所示.当恰好完全反应时,所得的溶液
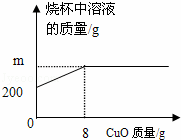
已知烧杯中装有 200g 硫酸和硫酸铜混合溶液,其中含硫酸铜 4.8g .向烧杯中逐渐加入氧化铜,烧杯中溶液的质量与加入氧化铜的质量关系如图所示.当恰好完全反应时,所得的溶液为不饱和溶液.
(提示: CuO+H 2 SO 4 =CuSO 4 +H 2 O )请计算:
( 1 ) m= g .
( 2 )原混合溶液中 H 2 SO 4 的质量分数.
( 3 )若取恰好完全反应时所得溶液 10g 配制成 20% 的硫酸铜溶液,需要 30% 的硫酸铜溶液多少克?
考点:
根据化学反应方程式的计算;有关溶质质量分数的简单计算. .
专题:
综合计算(图像型、表格型、情景型计算题).
分析:
( 1 )由图示可知氧化铜为 8g ,根据方程式可知氧化铜质量全部进入溶液;
( 2 )根据氧化铜的质量和方程式计算硫酸的质量,进一步计算原混合溶液中 H 2 SO 4 的质量分数;
( 3 )根据溶液稀释或浓缩前后溶质的质量不变分析.
( 1 )根据方程式 CuO+H 2 SO 4 =CuSO 4 +H 2 O 可知氧化铜质量全部进入溶液,所以 m=200g+8g=208g
( 2 )设混合溶液中 H 2 SO 4 的质量为 x ,生成硫酸铜的质量为 y
CuO+H 2 SO 4 =CuSO 4 +H 2 O
80 98 160
8g x y
![]() =
= ![]() =
= ![]()
x=9.8g y=16g
原混合溶液中 H 2 SO 4 的质量分数 ![]() ×100%=4.9%
×100%=4.9%
( 3 )恰好完全反应时所得溶液溶质质量分数为 ![]() ×100%=10%
×100%=10%
设需要 30% 的硫酸铜溶液 z
10g×10%+z×30%= ( 10g+z ) ×20%
z=10g
答:( 1 ) 208g
( 2 )原混合溶液中 H 2 SO 4 的质量分数 4.9%
( 3 )需要 30% 的硫酸铜溶液 10g
点评:
本题是借助于数学模型,利用图表的方式来分析和解决化学计算中的有关问题,要求学生有较强的识图能力和数据分析能力.
已知90℃时,水的离子积常数为1×10-12.在此温度下,将pH=8NaOH溶液与pH=4的H2S 2020-04-12 …
常温下,已知0.1mol·L-1HA(一元酸)溶液中c(H+):c(OH-)=1010,0.5mo 2020-05-14 …
有H2SO4和HCl的混合液20 ml,加入0.025mol/L的Ba(OH)2溶液时,生成沉淀的 2020-05-16 …
已知Fe5O7可以看作Fe2O3和Fe3O4的混合物.现有Fe、Fe5O7混合物共0.1mol,加 2020-06-23 …
已知温度T时水的离子积常数为Kw.该温度下,将浓度为a mol/L的一元酸HA与b mol/L的一 2020-06-27 …
已知硫酸溶液的浓度愈大,其密度就愈大,现将质量分数为3A%的硫酸溶液与质量分数为A%的硫酸溶液等体 2020-07-07 …
烧杯中装有一定量硫酸和硫酸铜的混合溶液,已知该溶液中含H2SO4的质量为9.8g。某同学为测定该混 2020-07-15 …
(1)欲分离出CO、CO2混合气体中的CO.将CO、CO2混合气体通过足量氢氧化钠溶液,并从所得的 2020-07-22 …
烧杯中装有一定量盐酸和硫酸铜的混合溶液,已知该溶液中含HCl的质量为3.65g.某同学为测定该混合溶 2020-11-02 …
已知:Fe5O7可以看作Fe2O3和Fe3O4的混合物.现有Fe、Fe2O3、Fe5O7混合物共0. 2020-11-03 …