早教吧作业答案频道 -->化学-->
由水钴矿[主要成分为Co2O3、Co(OH)3,还含有少量Fe2O3、Al2O3、MnO等]制取CoCl2•6H2O的工艺流程如下:已知:①浸出液中含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等.②流程中部分阳离子以氢
题目详情
由水钴矿[主要成分为Co2O3、Co(OH)3,还含有少量Fe2O3、Al2O3、MnO等]制取CoCl2•6H2O的工艺流程如下:
已知:①浸出液中含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等.
②流程中部分阳离子以氢氧化物形式沉淀时溶液的pH见下表.
③CoCl2•6H2O熔点为86℃,加热至110-120℃时,失去结晶水生成CoCl2.
回答下列问题:
(1)浸出过程中Co2O3发生反应的化学方程式为___
(2)NaClO3在浸出液中发生反应的离子方程式为___
(3)“加Na2CO3调pH至5.2”,过滤所得滤渣的主要成分为___(填化学式).
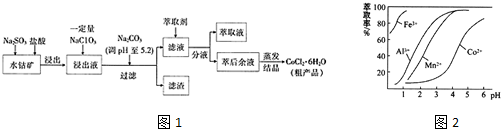
(4)萃取剂对金属离子的萃取与溶液pH的关系如图2所示,向“滤液”中加入萃取剂的目的是___,其使用的最佳pH范围是___(填选项字母)
A.2.0-2.5 B.3.0-3.5C.4.0-4.5 D.5.0-5.5
(5)制得的CoCl2•6H2O在烘干时需减压烘干的原因是___.为测定粗产品中CoCl2•6H2O含量.称取一定质量的粗产品溶于水,加入足量AgNO3溶液,过滤、洗涤,将沉淀烘干后称其质量.通过计算发现粗产品中CoCl2•6H2O的质量分数大于100%,其原因可能是(写两条):①___,②___.

已知:①浸出液中含有的阳离子主要有H+、Co2+、Fe2+、Mn2+、Al3+等.
②流程中部分阳离子以氢氧化物形式沉淀时溶液的pH见下表.
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Co(OH)2 | Al(OH)3 | Mn(OH)2 |
| 开始沉淀 | 2.7 | 7.6 | 7.6 | 4.0 | 7.7 |
| 完全沉淀 | 3.7 | 9.6 | 9.2 | 5.2 | 9.8 |
回答下列问题:
(1)浸出过程中Co2O3发生反应的化学方程式为___
(2)NaClO3在浸出液中发生反应的离子方程式为___
(3)“加Na2CO3调pH至5.2”,过滤所得滤渣的主要成分为___(填化学式).
(4)萃取剂对金属离子的萃取与溶液pH的关系如图2所示,向“滤液”中加入萃取剂的目的是___,其使用的最佳pH范围是___(填选项字母)
A.2.0-2.5 B.3.0-3.5C.4.0-4.5 D.5.0-5.5
(5)制得的CoCl2•6H2O在烘干时需减压烘干的原因是___.为测定粗产品中CoCl2•6H2O含量.称取一定质量的粗产品溶于水,加入足量AgNO3溶液,过滤、洗涤,将沉淀烘干后称其质量.通过计算发现粗产品中CoCl2•6H2O的质量分数大于100%,其原因可能是(写两条):①___,②___.
▼优质解答
答案和解析
含钴废料中加入盐酸和亚硫酸钠,Co2O3、Co(OH)3、Fe2O3、Al2O3、MnO和稀盐酸反应生成可溶性的CoCl2、AlCl3、FeCl2、MnCl2、NaCl,然后向溶液中加入氯酸钠,可得到FeCl3,然后加入Na2CO3调pH至5.2,可得到Fe(OH)3、Al(OH)3沉淀,然后过滤,向滤液中加入萃取剂,将锰离子萃取,萃取后的溶液中主要含有CoCl2,为得到CoCl2•6H2O晶体,将溶液蒸发浓缩、冷却结晶而得到粗产品,
(1)亚硫酸根离子具有还原性,Co2O3具有氧化性,浸出过程中Co2O3和亚硫酸钠发生氧化还原反应生成硫酸根离子和Co2+,化学方程式为:Co2O3+Na2SO3+4HCl=2CoCl2+Na2SO4+2H2O,
故答案为:Co2O3+Na2SO3+4HCl=2CoCl2+Na2SO4+2H2O;
(2)NaClO3具有氧化性,能氧化亚铁离子生成铁离子,氯酸根离子被还原生成氯离子,离子方程式为ClO3-+6Fe2++6H+=Cl-+6Fe3++3H2O,
故答案为:ClO3-+6Fe2++6H+=Cl-+6Fe3++3H2O;
(3)加Na2CO3调pH至5.2,铝离子能与碳酸根离子发生双水解生成氢氧化铝和二氧化碳,水解的离子方程式为:2Al3++3CO32-+3H2O=2Al(OH)3↓+3CO2↑;铁离子能与碳酸根离子发生双水解生成氢氧化铁和二氧化碳,水解的离子方程式为:2Fe3++3CO32-+3H2O=2Fe(OH)3↓+3CO2↑;
故答案为:Fe(OH)3、Al(OH)3;
(4)根据流程图可知,此时溶液中存在Mn2+、Co2+金属离子,由萃取剂对金属离子的萃取率与pH的关系可知
调节溶液PH在3.0~3.5之间,可使Mn2+完全沉淀,并防止Co2+转化为Co(OH)2沉淀,
故答案为:除去溶液中的Mn2+;B;
(5)CoCl2•6H2O熔点为86℃,加热至110-120℃时,失去结晶水生成CoCl2,制得的CoCl2•6H2O在烘干时需减压烘干的原因是降低烘干温度,防止产品分解,根据CoCl2•6H2O的组成分析,造成产品中CoCl2•6H2O的质量分数大于100%的原因可能是:1、含有含氯离子的杂质,导致氯离子含量大,2、结晶水化物失去部分水,导致相同质量的固体中氯离子含量变大,
故答案为:降低烘干温度,防止产品分解;粗产品含有可溶性氯化物;晶体失去了部分结晶水.
(1)亚硫酸根离子具有还原性,Co2O3具有氧化性,浸出过程中Co2O3和亚硫酸钠发生氧化还原反应生成硫酸根离子和Co2+,化学方程式为:Co2O3+Na2SO3+4HCl=2CoCl2+Na2SO4+2H2O,
故答案为:Co2O3+Na2SO3+4HCl=2CoCl2+Na2SO4+2H2O;
(2)NaClO3具有氧化性,能氧化亚铁离子生成铁离子,氯酸根离子被还原生成氯离子,离子方程式为ClO3-+6Fe2++6H+=Cl-+6Fe3++3H2O,
故答案为:ClO3-+6Fe2++6H+=Cl-+6Fe3++3H2O;
(3)加Na2CO3调pH至5.2,铝离子能与碳酸根离子发生双水解生成氢氧化铝和二氧化碳,水解的离子方程式为:2Al3++3CO32-+3H2O=2Al(OH)3↓+3CO2↑;铁离子能与碳酸根离子发生双水解生成氢氧化铁和二氧化碳,水解的离子方程式为:2Fe3++3CO32-+3H2O=2Fe(OH)3↓+3CO2↑;
故答案为:Fe(OH)3、Al(OH)3;
(4)根据流程图可知,此时溶液中存在Mn2+、Co2+金属离子,由萃取剂对金属离子的萃取率与pH的关系可知
调节溶液PH在3.0~3.5之间,可使Mn2+完全沉淀,并防止Co2+转化为Co(OH)2沉淀,
故答案为:除去溶液中的Mn2+;B;
(5)CoCl2•6H2O熔点为86℃,加热至110-120℃时,失去结晶水生成CoCl2,制得的CoCl2•6H2O在烘干时需减压烘干的原因是降低烘干温度,防止产品分解,根据CoCl2•6H2O的组成分析,造成产品中CoCl2•6H2O的质量分数大于100%的原因可能是:1、含有含氯离子的杂质,导致氯离子含量大,2、结晶水化物失去部分水,导致相同质量的固体中氯离子含量变大,
故答案为:降低烘干温度,防止产品分解;粗产品含有可溶性氯化物;晶体失去了部分结晶水.
看了 由水钴矿[主要成分为Co2O...的网友还看了以下:
解方程 1、x+5分之x+2=1.6+2分之x-1 2、0.3分之0.4(x-3)-0.04分之0 2020-05-16 …
数学六年级上册脱式计算.(能简算的要简算)2÷(4分之3-6分之1)x9分之517分之8÷16+1 2020-05-17 …
(1).8(a-b)^8/[3分之4(a-b)^2]为多少?(要求写出完整的过程)(2)-6(x- 2020-06-07 …
把5分之4-15分之8=15分之4,3分之2/15分之4=2分之5,25分之6*2分之5=2分之3 2020-06-21 …
计算下列式子:(1).(25r^4分之16s^2t^-6)^-2分之3(2).(2x^2分之1+3 2020-07-08 …
口算直接得出答案,1:口算1;(6-2分之1)×3分之2=2;6分之5÷7分之2÷35=3;7分之 2020-07-09 …
|-7又8分之3+4又2分之1|-18又4分之1+|-6-2分之1|=7又8分之3-4又2分之1- 2020-07-12 …
初中数学为什么有时候不能用带分数啊?曾经在网上看到过说,例如6又2分之1X,本意为6.5X,有人会错 2020-11-20 …
[2分之1-(4分之3-5分之3)除于4分之3}除于10分之7(8分之7-16分之5)x2分之1+6 2020-12-17 …
我有4到计算题不会,看看那位高人会,就帮我答吧!1,计算,能简算的要简算!(1),3乘(15分之2) 2020-12-27 …