早教吧作业答案频道 -->化学-->
已知:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)△H=-49.0kJ•mol-1.一定条件下,向体积固定为1L的密闭容器中充入1molCO2和3molH2,测得CO2和CH3OH(g)的浓度随时间变化曲线如图所示.(1)反应开
题目详情
已知:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g)△H=-49.0kJ•mol-1.一定条件下,向体积固定为1L的密闭容器中充入1mol CO2和3mol H2,测得CO2和CH3OH(g)的浓度随时间变化曲线如图所示.
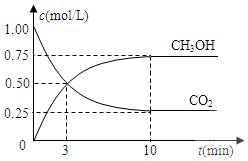
(1)反应开始至第3分钟内,CO2的反应速率v(CO2)=___mol/(L•min).
(2)该条件下,反应的平衡常数K=___;
(3)能使容器内n(CH3OH):n(CO2)增大的措施有___.
a.升高容器内温度 b.加入适当的催化剂
c.将H2O(g)从容器中分离出去 d.向容器内充入氦气增压
(4)当反应进行到10分钟时,若向该密闭容器中再充入1mol CO2和3mol H2,维持其它反应条件不变,则对体系影响的下列观点,正确的是___.
a.反应的K值增大 b.CO2的转化率增大
c.达平衡后c(CH3OH)是10分钟时的2倍d.反应继续放出热能49kJ.

(1)反应开始至第3分钟内,CO2的反应速率v(CO2)=___mol/(L•min).
(2)该条件下,反应的平衡常数K=___;
(3)能使容器内n(CH3OH):n(CO2)增大的措施有___.
a.升高容器内温度 b.加入适当的催化剂
c.将H2O(g)从容器中分离出去 d.向容器内充入氦气增压
(4)当反应进行到10分钟时,若向该密闭容器中再充入1mol CO2和3mol H2,维持其它反应条件不变,则对体系影响的下列观点,正确的是___.
a.反应的K值增大 b.CO2的转化率增大
c.达平衡后c(CH3OH)是10分钟时的2倍d.反应继续放出热能49kJ.
▼优质解答
答案和解析
(1)反应开始至第3分钟内,氢气的平均反应速率v(CO2)=
=
mol•L-1•min-1,故答案为:
;
(2)利用三段式解题法计算
CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g),
开始(mol/L):1 3 0 0
变化(mol/L):0.75 2.25 0.75 0.75
平衡(mol/L):0.25 0.75 0.75 0.75
K=
=
,故答案为:
;
(3)使n(CH3OH)/n(CO2)应采取措施,使平衡向正反应移动,注意不能增大二氧化碳或降低甲醇的量,
a、该反应正反应是放热反应,升高温度平衡向逆反应移动,n(CH3OH)/n(CO2)减小,故a错误,
b、加入适当的催化剂,平衡不移动,故b错误;
c、将H2O(g)从体系中分离,平衡向正反应移动,n(CH3OH)/n(CO2)增大,故c正确;
d、充入He(g),使体系压强增大,容器的容积不变,反应混合物的浓度不变,平衡不移动,n(CH3OH)/n(CO2)不变,故d错误;
故答案为:c;
(4)a.平衡常数K是温度的函数,温度不变平衡常数不变,故错误;
b.若向该密闭容器中再充入1mol CO2和3mol H2,相当于增大压强,平衡正向移动,CO2的转化率增大,故正确;
c.若向该密闭容器中再充入1mol CO2和3mol H2,相当于增大压强,平衡正向移动,所以达平衡后c(CH3OH)比10分钟时的2倍大,故错误;
d.不可能完全反应,所以不可能反应继续放出热能49kJ,故错误;故选b.
| 0.5mol/L |
| 3min |
| 1 |
| 6 |
| 1 |
| 6 |
(2)利用三段式解题法计算
CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g),
开始(mol/L):1 3 0 0
变化(mol/L):0.75 2.25 0.75 0.75
平衡(mol/L):0.25 0.75 0.75 0.75
K=
| 0.75×0.75 |
| 0.25×0.753 |
| 16 |
| 3 |
| 16 |
| 3 |
(3)使n(CH3OH)/n(CO2)应采取措施,使平衡向正反应移动,注意不能增大二氧化碳或降低甲醇的量,
a、该反应正反应是放热反应,升高温度平衡向逆反应移动,n(CH3OH)/n(CO2)减小,故a错误,
b、加入适当的催化剂,平衡不移动,故b错误;
c、将H2O(g)从体系中分离,平衡向正反应移动,n(CH3OH)/n(CO2)增大,故c正确;
d、充入He(g),使体系压强增大,容器的容积不变,反应混合物的浓度不变,平衡不移动,n(CH3OH)/n(CO2)不变,故d错误;
故答案为:c;
(4)a.平衡常数K是温度的函数,温度不变平衡常数不变,故错误;
b.若向该密闭容器中再充入1mol CO2和3mol H2,相当于增大压强,平衡正向移动,CO2的转化率增大,故正确;
c.若向该密闭容器中再充入1mol CO2和3mol H2,相当于增大压强,平衡正向移动,所以达平衡后c(CH3OH)比10分钟时的2倍大,故错误;
d.不可能完全反应,所以不可能反应继续放出热能49kJ,故错误;故选b.
看了 已知:CO2(g)+3H2(...的网友还看了以下:
求助:证明对任意素数p,存在正整数前n项和Sn及前m项和Sm(n,m为正整数),p=Sn/Sm证明 2020-05-17 …
(3)M和T形成的化合物在潮湿的空气中冒白色烟雾,反应的化学方程式为_____。 2020-05-25 …
如果甲数=2*3*m,乙数=3*5*m(m是自然数m不等于0),如果甲数和乙数的最大公因数是21, 2020-06-06 …
判一判.(1)两个不相等的自然数的最小公倍数一定比这两个数都大.(2)如果一个数是15的倍数,那么 2020-07-10 …
1、如果m=7n,那么m与n的最小公倍数是.2、有m、n两个正整数,如果m是n的倍数,则m和n的最 2020-07-31 …
苏教版国标本5下数学题1.连续三个奇数的和是x,它们当中最小的奇数可以表示为()A.x÷3-1B. 2020-07-31 …
是否存在整数m使得关于x的不等式1/m+3x/m²>x/m.1/m+3x/m²>x/m+3/m²与 2020-08-03 …
1.a=2*3*m,b=3*5*m,(m是自然数,且不=0),如果a和b的最大公约数是21,则m是( 2020-11-06 …
菌落中细菌被噬菌体杀死形成的透明区域称为噬菌斑.大肠杆菌的直径大小通常在0.5〜3μm.如图为分离获 2020-11-11 …
1.a与b互质,他们的最小公倍数是最大公约数的多少倍?2.a=2×3×m,b=3×5×m,(m是自然 2020-11-24 …