铵明矾是一种广泛应用于医药、食品、污水处理等多个行业的重要化工产品。以高岭土(含SiO2、Al2O3、少量Fe2O3等)为原料制备硫酸铝晶体[Al2(SO4)3·18H2O]和铵明矾[NH4Al(SO4)2·12H2O]的实验方案如
铵明矾是一种广泛应用于医药、食品、污水处理等多个行业的重要化工产品。以高岭土(含SiO2、Al2O3、少量Fe2O3等)为原料制备硫酸铝晶体[Al2(SO4)3·18H2O]和铵明矾[NH4Al(SO4)2·12H2O]的实验方案如下图所示。
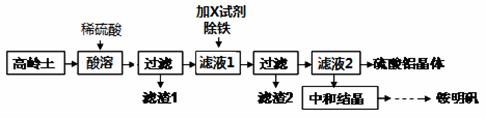
请回答下列问题:
(1)高岭土首先需要灼烧,实验室灼烧高岭土所需的实验仪器有 (填字母)。
a.蒸发皿 b.泥三角 c.漏斗 d.酒精灯 e.三脚架 f.坩埚 g.烧杯 h.试管
(2)写出酸溶过程中发生反应的离子方程式: 。
(3)检验滤液2中是否含有Fe3+的实验方法为: ;滤渣2的主要成分为: (填化学式)。
(4)滤液2→硫酸铝晶体的操作包含的实验步骤有: 、 、 、洗涤、干燥。
(5)中和结晶操作是将过滤出硫酸铝晶体后的滤液,先用硫酸调节酸铝比(溶液中游离硫酸和硫酸铝的物质的量之比),再用氨水中和至一定的pH值即可析出铵明矾晶体,写出该过程中的总反应方程式: 。
(1)bdef(2分,注:答不全给1分,全对给2分,只要多选或错选则该空为0分)
(2)Al2O3+6H+=2Al3++3H2O(2分), Fe2O3+6H+=2Fe 3++3H2O(2分)
(3)取少量滤液2于试管中,滴加几滴KSCN溶液,若溶液变为血红色则含Fe3+,否则不含Fe3+(2分); Fe(OH)3 (2分)
(4)蒸发浓缩(1分)、冷却结晶(1分)、过滤 (1分)[.
(5)Al2(SO4)3 +H2SO4 +2NH3·H2O +22H2O=2[NH4Al(SO4)2·12H2O]↓
或Al2(SO4)3 +H2SO4 +2NH3 +24H2O=2[NH4Al(SO4)2·12H2O]↓(2分)
(注:有关化学方程式或离子方程式的书写不配平不给分,漏写“↑”或“↓”等符号扣1分)
碱式碳酸盐A可用作胃药,其组成可表示为Al2Mg6(OH)x(CO3)y·zH2O。某校化学兴趣小 2020-04-11 …
药品入库验收时发现不合格药品时,负责质量查询的应是( )。A.业务进货员B.质量管理员C.药品验收员 2020-05-31 …
总装备部的国防科技重点试验和国防重点学科实验室要远远强于教育部的国家重点实验室国家级别各类重点实验 2020-06-12 …
为什么在做化学实验过程中发现药品量不够反应时要重新实验? 2020-06-18 …
如图所示,用单色光做双缝干涉实验,S1和S2为双狭缝,O为光屏上的中央亮纹,P处为O点上方的第二亮 2020-06-21 …
2015年12月7日,我国女药学家屠呦呦获诺贝尔生理学或医学奖。她一生潜心研究,大约试验了200多 2020-07-15 …
降血脂化学一类新药试验费用降血脂的化学一类新药按申报新药的要求,需要完成那些试验,每个试验需多少费用 2020-12-16 …
有十瓶药丸,其中若干瓶为超重药丸.普通药丸5g每粒,超重药丸6g每粒,每瓶药丸的数量相同.求:只用一 2020-12-22 …
活动一讨论家庭药箱中的常备药品目的:说出家庭药箱中的常备药品及其作用。指导:1.学生4人一组,列表归 2020-12-23 …
老师列举过C和O的各种划分之最,1生物体内占细胞干重最多的的元素是C,2湿重是O.3…………(我记得 2020-12-24 …