早教吧作业答案频道 -->化学-->
化学学习常用探究的方法学习常见物质的组成、性质与制取.课堂上老师引导我们回顾了几个探究实验.探究1:研究常见物质的组成.A、B、C都是研究物质组成的实验.从研究方法得
题目详情
化学学习常用探究的方法学习常见物质的组成、性质与制取.课堂上老师引导我们回顾了几个探究实验.
探究1:研究常见物质的组成.
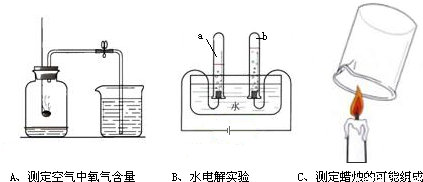
A、B、C都是研究物质组成的实验.从研究方法得知,A实验是利用可燃物消耗瓶内的______,使瓶内______减小推测空气中氧气含量的.B实验是通过证明生成物的______来推测水的组成的.而C实验与______(填实验代号)实验的方法相同.
探究2:研究常见物质的性质
根据下图所示实验,并阅读小资料,回答下列问题.
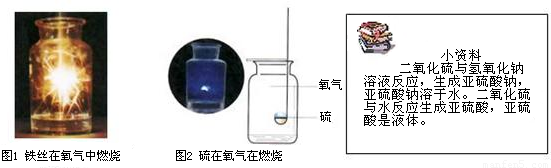
(1)图1集气瓶中加入液体的作用是______.
(2)图2集气瓶中加入的液体可能是______,其目的为______.
(3)图1和图2实验中涉及反应的共同点是______.
探究3:研究常见气体的制取
如图是实验室制取和收集气体的装置图.实验课上同学们用过氧化氢溶液和二氧化锰混合制取氧气,请回答:
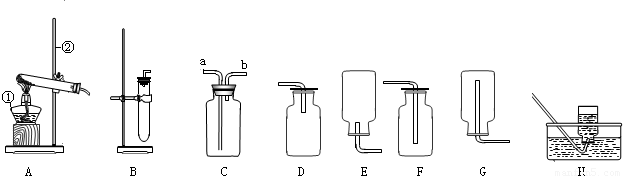
(1)写出A图中带标号仪器的名称:①______②______.
(2)用该方法制取氧气的化学方程式是______.2H 2 O+O 2 ↑
探究1:研究常见物质的组成.

A、B、C都是研究物质组成的实验.从研究方法得知,A实验是利用可燃物消耗瓶内的______,使瓶内______减小推测空气中氧气含量的.B实验是通过证明生成物的______来推测水的组成的.而C实验与______(填实验代号)实验的方法相同.
探究2:研究常见物质的性质
根据下图所示实验,并阅读小资料,回答下列问题.

(1)图1集气瓶中加入液体的作用是______.
(2)图2集气瓶中加入的液体可能是______,其目的为______.
(3)图1和图2实验中涉及反应的共同点是______.
探究3:研究常见气体的制取
如图是实验室制取和收集气体的装置图.实验课上同学们用过氧化氢溶液和二氧化锰混合制取氧气,请回答:

(1)写出A图中带标号仪器的名称:①______②______.
(2)用该方法制取氧气的化学方程式是______.2H 2 O+O 2 ↑
▼优质解答
答案和解析
分析:
从不同的方面来研究物质的组成:根据压强的变化来测定空气中氧气的含量和根据元素种类在化学反应前后不发生变化;认识铁丝和硫在氧气中燃烧的共同点:都有氧气参与,都是化合反应,都是放热反应,反应条件都是点燃等,能从不同的角度看待不同反应的共同点,一定还要注意反应操作应注意的事项;在实验室中制取氧气由于反应物的状态、反应条件的不同,选取的反应装置则不同,收集装置的选择主要和所制取气体的性质有关系.
探究一:测定空气中氧气的含量主要是利用红磷可以和空气中的氧气在点燃的条件下反应生成固态的五氧化二磷,从而导致瓶内的压强减小,从而根据进入瓶中的水的多少来推测空气中氧气的体积分数.根据元素种类在化学变化前后不发生变化,由于水在通电的条件下可以生成氢气和氧气,可推知水是由氢元素和氧元素组成;石蜡在氧气中燃烧生成二氧化碳和水,可推知石蜡中一定含有碳、氢元素,可能含有氧元素.故答案为:氧气,压强,元素种类,B探究二:(1)由于铁丝在氧气中燃烧时会生成大量的热,为防止融熔的生成物溅落时炸裂瓶底,要在瓶中放一层沙或一些水,故答案为:防止高温熔化物溅落瓶底,使集气瓶炸裂(2)由于硫在氧气中燃烧会生成有毒的二氧化硫气体,为防止二氧化硫气体排放到空气中污染空气,应在集气瓶中放一些能吸收二氧化硫的氢氧化钠溶液或其他的碱液,故答案为:氢氧化钠溶液,防止二氧化气体排放到空气中污染空气(3)由于3Fe+2O2Fe3O4,S+O2SO2,两个反应的相同点有:都有氧气参与,都是化合反应,都是放热反应,反应条件都是点燃等,故答案为:都是化合反应(合理即可)探究三:(1)酒精灯,铁架台(2)由于过氧化氢溶液在二氧化锰的催化作用下生成水和氧气,故答案为:2H2O22H2O+O2↑(3)由于该反应是固液混合且不需要加热,因此应选择B装置来制氧气,又因氧气不易溶于水而且密度比空气大,因此可以选择H或F或C来收集氧气;若采用C来收集氧气,即相当于排水法收集氧气,必须把里面的水能够排净,即必须能引起瓶内的压强增大.故答案为:B,C或F或H,b(4)由题意可知,导气管没有堵塞、弯折的情况,各小组所用过氧化氢溶液溶质的质量分数也均相同,所以首先否定甲和丙的猜想,而乙的猜想是过氧化氢溶液用量过多造成的,因此设计实验时只要控制过氧化氢溶液的量不同则可.故答案为:甲和丙,实验步骤实验现象结论取两只试管分别加入等质量的二氧化锰,再加入不同质量的过氧化氢溶液过氧化氢溶液多的反应较剧烈(或瞬间产生的气泡多)乙的猜想正确[交流反思]橡皮塞弹飞主要是因为装置内的压强过大引起的,因此可以换成容积较大的反应容器或者是可以调节装置内压强的容器或者是能够控制反应速率的容器,故答案为:换成一容积较大的反应容器(如广口瓶、锥形瓶、烧瓶等)或用长颈漏斗、分液漏斗、注射器等.(合理即可)
点评:
主要从不同的层面研究物质的组成、常见物质的性质、常见气体的制取,要求学生把握住一些规律性的东西,培养学生应用知识解决问题的能力.
分析:
从不同的方面来研究物质的组成:根据压强的变化来测定空气中氧气的含量和根据元素种类在化学反应前后不发生变化;认识铁丝和硫在氧气中燃烧的共同点:都有氧气参与,都是化合反应,都是放热反应,反应条件都是点燃等,能从不同的角度看待不同反应的共同点,一定还要注意反应操作应注意的事项;在实验室中制取氧气由于反应物的状态、反应条件的不同,选取的反应装置则不同,收集装置的选择主要和所制取气体的性质有关系.
探究一:测定空气中氧气的含量主要是利用红磷可以和空气中的氧气在点燃的条件下反应生成固态的五氧化二磷,从而导致瓶内的压强减小,从而根据进入瓶中的水的多少来推测空气中氧气的体积分数.根据元素种类在化学变化前后不发生变化,由于水在通电的条件下可以生成氢气和氧气,可推知水是由氢元素和氧元素组成;石蜡在氧气中燃烧生成二氧化碳和水,可推知石蜡中一定含有碳、氢元素,可能含有氧元素.故答案为:氧气,压强,元素种类,B探究二:(1)由于铁丝在氧气中燃烧时会生成大量的热,为防止融熔的生成物溅落时炸裂瓶底,要在瓶中放一层沙或一些水,故答案为:防止高温熔化物溅落瓶底,使集气瓶炸裂(2)由于硫在氧气中燃烧会生成有毒的二氧化硫气体,为防止二氧化硫气体排放到空气中污染空气,应在集气瓶中放一些能吸收二氧化硫的氢氧化钠溶液或其他的碱液,故答案为:氢氧化钠溶液,防止二氧化气体排放到空气中污染空气(3)由于3Fe+2O2Fe3O4,S+O2SO2,两个反应的相同点有:都有氧气参与,都是化合反应,都是放热反应,反应条件都是点燃等,故答案为:都是化合反应(合理即可)探究三:(1)酒精灯,铁架台(2)由于过氧化氢溶液在二氧化锰的催化作用下生成水和氧气,故答案为:2H2O22H2O+O2↑(3)由于该反应是固液混合且不需要加热,因此应选择B装置来制氧气,又因氧气不易溶于水而且密度比空气大,因此可以选择H或F或C来收集氧气;若采用C来收集氧气,即相当于排水法收集氧气,必须把里面的水能够排净,即必须能引起瓶内的压强增大.故答案为:B,C或F或H,b(4)由题意可知,导气管没有堵塞、弯折的情况,各小组所用过氧化氢溶液溶质的质量分数也均相同,所以首先否定甲和丙的猜想,而乙的猜想是过氧化氢溶液用量过多造成的,因此设计实验时只要控制过氧化氢溶液的量不同则可.故答案为:甲和丙,实验步骤实验现象结论取两只试管分别加入等质量的二氧化锰,再加入不同质量的过氧化氢溶液过氧化氢溶液多的反应较剧烈(或瞬间产生的气泡多)乙的猜想正确[交流反思]橡皮塞弹飞主要是因为装置内的压强过大引起的,因此可以换成容积较大的反应容器或者是可以调节装置内压强的容器或者是能够控制反应速率的容器,故答案为:换成一容积较大的反应容器(如广口瓶、锥形瓶、烧瓶等)或用长颈漏斗、分液漏斗、注射器等.(合理即可)
点评:
主要从不同的层面研究物质的组成、常见物质的性质、常见气体的制取,要求学生把握住一些规律性的东西,培养学生应用知识解决问题的能力.
看了 化学学习常用探究的方法学习常...的网友还看了以下:
某电视机厂要印制产品宣传材料.甲印刷厂提出:每份材料收1元印制费,另收1500元制版费;乙厂提出:每 2020-03-30 …
小强和几位同学在实验室用图1装置制取几种气体.(1)写出仪器名称:①③(2)小强同学想用高锰酸钾粉 2020-04-08 …
1乳酸与足量金属钠反应的化学方程式2乳酸与碳酸钠溶液反应的化学方1乳酸与足量金属钠反应的化学方程式 2020-04-08 …
设函数f(x)=(2^x)/(1+2^x)-1/2,[x]表示不超过x的最大整数,则函数y=[f( 2020-04-27 …
英语翻译1.我们将定期推出新款式的服装,以适应潮流的发展2.我们还将推出为客人量身定制的服务,客人 2020-06-17 …
金属材料在工农业生产、日常生活中有着广泛应用.(1)铁制品绣蚀的原因主要是铁与空气中的和水蒸气发生 2020-06-19 …
(2007•常德)如图1,已知四边形ABCD是菱形,G是线段CD上的任意一点时,连接BG交AC于F, 2020-11-12 …
下列事例中,运用的科学研究方法相同的是()(1)探究液体内部压强与深度的关系(2)探究串联电路中电流 2020-12-04 …
实验室需配制480mL0.1mol•L-1的Na2CO3溶液,填空并回答下列问题:(1)配制480m 2021-01-22 …
1.已知一个正方体的8个顶点都在同一个球面上,计算球的表面积和这个正方体的全面积的比.2.设计一个正 2021-02-05 …