早教吧作业答案频道 -->化学-->
合成气的主要成分是一氧化碳和氢气,可用于合成二甲醚等清洁燃料.从天然气获得合成气过程中可能发生的反应有:①CH4(g)+H2O(g)⇌CO(g)+3H2(g)△H1=+206.1kJ/mol②CH4(g)+CO2(g)⇌2C
题目详情
合成气的主要成分是一氧化碳和氢气,可用于合成二甲醚等清洁燃料.从天然气获得合成气过程中可能发生的反应有:
①CH4(g)+H2O(g)⇌CO(g)+3H2(g)△H1=+206.1kJ/mol
②CH4(g)+CO2(g)⇌2CO(g)+2H2(g)△H2=+247.3kJ/mol
③CO(g)+H2O(g)⇌CO2(g)+H2(g)△H3=c/mol•L-1
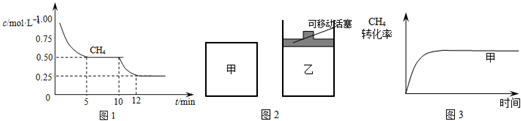
(1)在一密闭容器中进行反应①,测得CH4的物质的量浓度随反应时间的变化如图1所示.反应进行的前5min内,v(H2)=___;10min时,改变的外界条件可能是___.
(2)如图2所示,在甲、乙两容器中分别充入等物质的量的CH4和CO2,使甲、乙两容器初始容积相等.在相同温度下发生反应②,并维持反应过程中温度不变.已知甲容器中CH4的转化率随时间变化的图象如图3所示,请在图3中画出乙容器中CH4的转化率随时间变化的图象.
(3)800℃时,反应③的化学平衡常数K=1.0,某时刻测得该温度下的密闭容器中各物质的物质的量见下表:
此时反应③中正反应速率___逆反应速率(大于、小于、等于)
①CH4(g)+H2O(g)⇌CO(g)+3H2(g)△H1=+206.1kJ/mol
②CH4(g)+CO2(g)⇌2CO(g)+2H2(g)△H2=+247.3kJ/mol
③CO(g)+H2O(g)⇌CO2(g)+H2(g)△H3=c/mol•L-1

(1)在一密闭容器中进行反应①,测得CH4的物质的量浓度随反应时间的变化如图1所示.反应进行的前5min内,v(H2)=___;10min时,改变的外界条件可能是___.
(2)如图2所示,在甲、乙两容器中分别充入等物质的量的CH4和CO2,使甲、乙两容器初始容积相等.在相同温度下发生反应②,并维持反应过程中温度不变.已知甲容器中CH4的转化率随时间变化的图象如图3所示,请在图3中画出乙容器中CH4的转化率随时间变化的图象.
(3)800℃时,反应③的化学平衡常数K=1.0,某时刻测得该温度下的密闭容器中各物质的物质的量见下表:
| CO | H2O | CO2 | H2 |
| 0.5mol | 8.5mol | 2.0mol | 2.0mol |
▼优质解答
答案和解析
(1)反应进行的前5min内,甲烷浓度变化量为(1-0.5)mol/L=0.5mol/L,则v(CH4)=
=0.1mol/(L.min),速率之比等于化学计量数之比,则v(H2)=3v(CH4)=0.3mol/(L.min);
10min时瞬间甲烷浓度未变,而后浓度减小,改变条件平衡正向移动,正反应为放热反应,可能是降低温度等,
故答案为:0.3mol/(L.min);降低温度;
(2)甲为恒温恒容,随反应进行容器内压强增大,乙为恒温恒压,乙等效为在甲平衡的基础上减小压强,平衡正向移动,乙中甲烷的转化率大于甲中,减小压强反应速率减慢,到达平衡时间故甲中长,则乙容器中CH4的转化率随时间变化的图象为: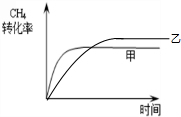 ,
,
故答案为: ;
;
(3)此时浓度商Qc=
=0.94<K=1,反应向正反应进行,故正反应速率大于逆反应速率,
故:大于.
| 0.5mol/L |
| 5min |
10min时瞬间甲烷浓度未变,而后浓度减小,改变条件平衡正向移动,正反应为放热反应,可能是降低温度等,
故答案为:0.3mol/(L.min);降低温度;
(2)甲为恒温恒容,随反应进行容器内压强增大,乙为恒温恒压,乙等效为在甲平衡的基础上减小压强,平衡正向移动,乙中甲烷的转化率大于甲中,减小压强反应速率减慢,到达平衡时间故甲中长,则乙容器中CH4的转化率随时间变化的图象为:
 ,
,故答案为:
 ;
;(3)此时浓度商Qc=
| 2×2 |
| 0.5×8.5 |
故:大于.
看了 合成气的主要成分是一氧化碳和...的网友还看了以下:
某植株的红花(A)对白花(a)为显性,阔叶(B)对窄叶()为显性,现有基因型为AB的两个植株均自花 2020-04-27 …
下列大小关系正确的是()A.熔点:已烷>2,2一二甲基戊烷>2,3一二甲基丁烷>丙烷B.含氢量:甲 2020-05-13 …
下列关系正确的是()A.熔点:正戊烷>2,2一二甲基戊烷>2,3一二甲基丁烷>丙烷B.密度:CCl 2020-05-14 …
下列关系正确的是()A.熔、沸点:戊烷>2,2一二甲基戊烷>2,3一二甲基丁烷>丙烷B.密度:CH 2020-05-14 …
下列关系正确的是()A.沸点:戊烷>2,2一二甲基戊烷>2,3一二甲基丁烷>丙烷B.密度:CCl4 2020-05-14 …
问一道司法考试民法的题(一)甲有一块价值一万元的玉石。甲与乙订立了买卖该玉石的合同,约定价金11, 2020-06-16 …
马上就要过期不候一、1摩尔H2O含有个水分子,H2O中有个氧原子,个氢原子,1摩尔H2O含有摩尔氧 2020-06-22 …
有关糖类的说法错误的是A.糖类分子组成一定都符合通式Cn(H2O)m,符合Cn(H2O)m的物质不一 2020-11-07 …
氢气作为高效、洁净的二次能源,将成为未来社会的主要能源之一.甲烷重整是一种被广泛使用的制氢工艺.Ⅰ. 2021-01-12 …
呼吸作用的简单反应式是A.CO2+H2O──→有机物B.有机物──→CO2+H2OC.H2O+O2 2021-02-07 …